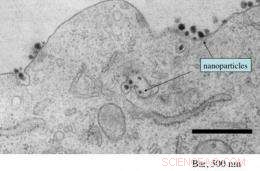
Questa micrografia elettronica mostra la presenza di numerose nanoparticelle mirate contenenti siRNA sia in entrata che all'interno di una cellula tumorale. Attestazione:Caltech/Swaroop Mishra
Un team di ricercatori e clinici guidato dal California Institute of Technology (Caltech) ha pubblicato la prima prova che una nanoparticella mirata, utilizzata come terapia sperimentale e iniettata direttamente nel flusso sanguigno di un paziente, può portare a tumori, fornire piccoli RNA interferenti a doppio filamento (siRNA), e disattivare un importante gene del cancro utilizzando un meccanismo noto come interferenza dell'RNA (RNAi). Inoltre, il team ha fornito la prima dimostrazione che questo nuovo tipo di terapia, infuso nel flusso sanguigno, può arrivare ai tumori umani in modo dose-dipendente, cioè un numero maggiore di nanoparticelle inviate nel corpo porta a un numero maggiore di nanoparticelle nelle cellule tumorali.
Questi risultati, pubblicato nell'edizione online anticipata del 21 marzo della rivista Natura , dimostrare la fattibilità dell'uso sia di nanoparticelle che di terapie a base di RNAi nei pazienti, e aprire la porta a future terapie "rivoluzionarie" che attaccano il cancro e altre malattie a livello genetico, dice Mark Davis, la Warren e Katharine Schlinger Professore di Ingegneria Chimica al Caltech, e il capo del gruppo di ricerca.
La scoperta dell'interferenza dell'RNA, il meccanismo mediante il quale i doppi filamenti di RNA silenziano i geni, ha vinto il premio Nobel 2006 per la fisiologia o la medicina ai ricercatori Andrew Fire e Craig Mello. Gli scienziati hanno riferito per la prima volta di aver scoperto questo nuovo meccanismo nei vermi in un 1998 Natura carta. Da allora, il potenziale per questo tipo di inibizione genica di portare a nuove terapie per malattie come il cancro è stato molto pubblicizzato.
"RNAi è un nuovo modo per fermare la produzione di proteine, " dice Davis. Ciò che lo rende uno strumento così potente, Aggiunge, è il fatto che il suo bersaglio non è una proteina. Le aree vulnerabili di una proteina possono essere nascoste all'interno delle sue pieghe tridimensionali, rendendo difficile per molti terapeutici raggiungerli. In contrasto, L'interferenza dell'RNA prende di mira l'RNA messaggero (mRNA) che codifica le informazioni necessarie per creare una proteina in primo luogo.
"In linea di principio, "dice Davis, "Ciò significa che ogni proteina ora è drogabile perché la sua inibizione si ottiene distruggendo l'mRNA. E possiamo perseguire gli mRNA in un modo molto progettato, dati tutti i dati genomici che sono e saranno disponibili".
Ancora, ci sono stati numerosi potenziali ostacoli all'applicazione della tecnologia RNAi come terapia negli esseri umani. Uno dei più problematici è stato trovare un modo per traghettare le terapie, che sono costituiti da fragili siRNA, nelle cellule tumorali dopo iniezione diretta nel flusso sanguigno. Davis, però, aveva una soluzione. Anche prima della scoperta dell'RNAi, lui e il suo team avevano iniziato a lavorare sui modi per fornire acidi nucleici nelle cellule tramite somministrazione sistemica. Alla fine hanno creato un sistema a quattro componenti, caratterizzato da un polimero unico, che può autoassemblarsi in un mirato, nanoparticelle contenenti siRNA. Il sistema di consegna di siRNA è in fase di sviluppo clinico da Calando Pharmaceuticals, Inc., una società di nanobiotecnologie con sede a Pasadena.
"Queste nanoparticelle sono in grado di portare gli siRNA al sito mirato all'interno del corpo, " dice Davis. Una volta raggiunto il loro obiettivo, in questo caso, le cellule cancerose all'interno dei tumori:le nanoparticelle entrano nelle cellule e rilasciano i siRNA.
I risultati scientifici descritti nel Natura gli articoli provengono da uno studio clinico di fase I su queste nanoparticelle che ha iniziato a trattare i pazienti nel maggio 2008. Gli studi di fase I sono, per definizione, prove di sicurezza; l'idea è vedere se ea quale livello il farmaco o altra terapia diventa nociva o tossica. Questi studi possono anche fornire una prova scientifica non umana del concetto, che è esattamente ciò che viene riportato nell'articolo di Nature.
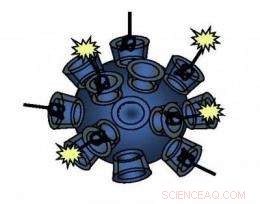
Questa nanoparticella mirata utilizzata nello studio e mostrata in questo schema è costituita da un polimero unico e può raggiungere le cellule tumorali umane in modo dose-dipendente. Credito:Caltech/Derek Bartlett
Utilizzando una nuova tecnica sviluppata al Caltech, il team è stato in grado di rilevare e visualizzare le nanoparticelle all'interno delle cellule sottoposte a biopsia dai tumori di molti dei partecipanti allo studio. Inoltre, Davis e i suoi colleghi sono stati in grado di dimostrare che maggiore è la dose di nanoparticelle somministrata al paziente, maggiore è il numero di particelle trovate all'interno delle cellule tumorali, il primo esempio di questo tipo di risposta dose-dipendente utilizzando nanoparticelle mirate.
Anche meglio, Davis dice, le prove hanno mostrato che i siRNA avevano fatto il loro lavoro. Nelle cellule tumorali analizzate dai ricercatori, l'mRNA che codifica per la ribonucleotide reduttasi della proteina di crescita cellulare era stato degradato. Questo degrado, a sua volta, portato ad una perdita della proteina.
Più precisamente, i frammenti di mRNA trovati erano esattamente della lunghezza e della sequenza che avrebbero dovuto essere se fossero stati tagliati nel punto preso di mira dal siRNA, osserva Davis. "È la prima volta che qualcuno trova un frammento di RNA dalle cellule di un paziente che mostra che l'mRNA è stato tagliato esattamente alla base giusta tramite il meccanismo dell'RNAi, " dice. "Dimostra che il meccanismo RNAi può avvenire utilizzando siRNA in un essere umano".
"Ci sono molti bersagli del cancro che possono essere efficacemente bloccati in laboratorio usando siRNA, ma bloccarli in clinica è stato elusivo, "dice Antoni Ribas, professore associato di medicina e chirurgia presso il Jonsson Comprehensive Cancer Center dell'UCLA. "Questo perché molti di questi obiettivi non sono suscettibili di essere bloccati da farmaci antitumorali progettati tradizionalmente. Questa ricerca fornisce la prima prova che ciò che funziona in laboratorio potrebbe aiutare i pazienti in futuro mediante la consegna specifica di siRNA utilizzando nanoparticelle mirate. Possiamo iniziare a pensare di prendere di mira l'indifferenziabile".
"Sebbene questi dati siano molto precoci e siano necessarie ulteriori ricerche, questo è uno studio promettente su un nuovo agente cancerogeno, e siamo orgogliosi del nostro contributo allo sviluppo clinico iniziale di siRNA per il trattamento del cancro, "dice Anthony Tolcher, direttore della ricerca clinica presso la South Texas Accelerated Research Therapeutics (START).
"I dati promettenti degli studi clinici convalidano i nostri anni di ricerca presso City of Hope sulla ribonucleotide reduttasi come bersaglio per nuove terapie genetiche per il cancro, " aggiunge il coautore Yun Yen, direttore associato per la ricerca traslazionale presso City of Hope. "Stiamo vedendo per la prima volta l'utilità del siRNA come terapia contro il cancro e come la nanotecnologia può colpire specificamente le cellule tumorali".
Lo studio di Fase I, sponsorizzato da Calando Pharmaceuticals, sta procedendo presso lo START e il Jonsson Comprehensive Cancer Center dell'UCLA, e i risultati clinici della sperimentazione saranno presentati in un secondo momento. "Proprio alla fine, abbiamo dimostrato che il meccanismo RNAi può essere utilizzato negli esseri umani per la terapia e che la consegna mirata di siRNA consente la somministrazione sistemica, "Dice Davis. "E 'un momento molto emozionante."