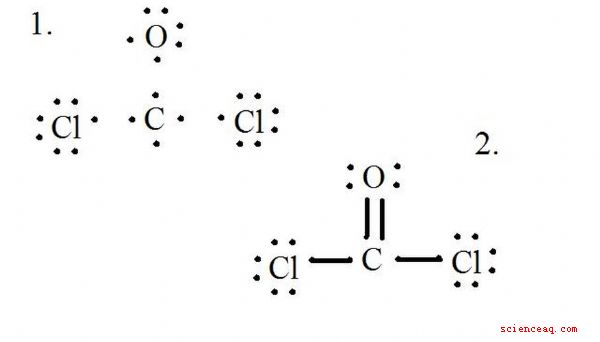
Quando si determina la carica formale di una molecola come CoCl2 (gas fosgene), è necessario conoscere il numero di elettroni di valenza per ogni atomo e la struttura di Lewis della molecola.
Numero dell'elettrone di valenza
Cerca ogni atomo nella tavola periodica degli elementi per determinare il numero di elettroni di valenza.
Ricorda che due elettroni entrano nel primo guscio, due elettroni in la seconda shell, sei elettroni nella prima shell, ecc. Come promemoria: 1s (^ 2) 2s (^ 2) 2p (^ 6) 3s (^ 2) 3p (^ 6)
Regola per la carica. Se la molecola è uno ione, aggiungere o sottrarre uno o più elettroni nel complesso per tenere conto della carica finale.
Per CoCl2 (gas di fosgene): C = 4; O = 6; Cl = 7. La molecola non è ionizzata e ha una carica neutra. Pertanto, la quantità totale di elettroni di valenza è 4 + 6 + (7x2) = 24.
Struttura di Lewis
Vedi lo schema per la struttura di Lewis di CoCl2 (gas fosgene). La struttura di Lewis rappresenta la struttura più stabile e probabile per una molecola. Gli atomi sono disegnati con elettroni di valenza accoppiati; legami si formano tra elettroni solitari per soddisfare la regola dell'ottetto.
Disegna ogni atomo e i suoi elettroni di valenza, quindi forma legami come necessario.
Gli atomi di cloruro condividono singoli legami con la molecola di carbonio, mentre l'atomo di ossigeno forma un doppio legame con il carbonio. Ogni atomo nella struttura finale soddisfa la regola dell'ottetto e ha otto elettroni di valenza che consentono la stabilità molecolare.
Carica formale di ogni atomo
Contare le coppie solitarie di ciascun atomo nella struttura di Lewis. Assegna a ogni atomo un elettrone per ogni legame a cui partecipa. Aggiungi questi numeri insieme. In CoCl2: C = 0 coppie solitarie più 4 elettroni da legami = 4 elettroni. O = 4 elettroni da coppie solitarie più 2 elettroni da legami = 6 elettroni. Cl = 6 elettroni da coppie solitarie più 1 elettrone da un legame con C = 7 elettroni.
Sottrai la somma dal numero di elettroni di valenza nell'atomo non legato. Il risultato è la carica formale per quell'atomo. In CoCl2: C = 4 elettroni di valenza (v.e.) nell'atomo non legato meno 4 elettroni assegnati nella struttura di Lewis (L.s.) = 0 carica formale O = 6 v.e. - 6 L. = 0 carica formale Cl = 7 v.e. - 7 L. = 0 carica formale
Scrivi queste accuse accanto agli atomi nella struttura di Lewis. Se la molecola complessiva ha una carica, racchiudi la struttura di Lewis tra parentesi con la carica scritta al di fuori delle parentesi nell'angolo in alto a destra.
Avviso
Il calcolo della carica formale per le molecole contenenti metalli di transizione può essere difficile Il numero di elettroni di valenza per i metalli di transizione sarà quelli al di fuori del nobile nucleo simile al gas.