Credito:Angewandte Chemie
Etilene, o etene, è una materia prima primaria per l'industria chimica, anche come materiale di partenza per la produzione di un'ampia varietà di materie plastiche. Nel diario Angewandte Chemie , gli scienziati hanno ora introdotto una nuova tecnica elettrochimica per la produzione selettiva ed efficiente dal punto di vista energetico di etilene dal monossido di carbonio, che può essere ottenuto da risorse rinnovabili e rifiuti.
Sia dal punto di vista economico che ambientale, la conversione del monossido di carbonio (CO) in etilene mediante metodi efficienti dal punto di vista energetico è un processo chiave per l'utilizzo di materie prime non petrolchimiche. Oggi, l'etilene è tipicamente prodotto dal cracking con vapore di nafta derivata dalle raffinerie di petrolio. In questo processo, gli idrocarburi a catena lunga sono suddivisi in catene più corte a 800-900 °C. In alternativa, l'etilene può essere prodotto dal gas di sintesi, una miscela di CO e idrogeno ottenuta dalla gassificazione del carbone, ma può anche essere ottenuto dal biogas, Di legno, e rifiuti come fonti di carbonio.
Il processo Fischer-Tropsch può essere utilizzato per convertire il gas di sintesi in una miscela di idrocarburi, compreso l'etilene. Gli svantaggi di questo metodo sono le condizioni ad alta intensità energetica da 200 a 250 °C, da 5 a 50 bar di pressione, e il consumo di prezioso idrogeno. Inoltre, un massimo del 30% dei prodotti sono gli idrocarburi C2 preferiti (etilene ed etano). Non è possibile prevenire la formazione di catene più lunghe, il processo per separare l'etilene è complesso, e 30-50% CO 2 si produce anche, che è un'emissione indesiderata e rappresenta uno spreco di carbonio.
I ricercatori che lavorano con Dehui Deng presso l'Università di Xiamen e il Dalian Institute of Chemical Physics dell'Accademia cinese delle scienze hanno ora introdotto un nuovo approccio per un processo elettrocatalitico diretto per la produzione altamente selettiva di etilene. In questo metodo, La CO viene ridotta con acqua a temperatura ambiente e pressione standard, utilizzando un catalizzatore di rame e corrente elettrica.
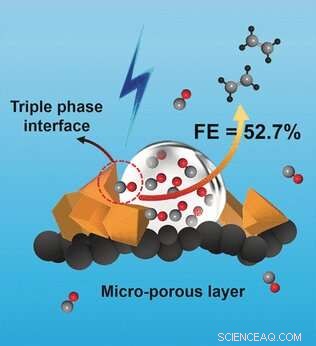
Ottimizzando la struttura del loro elettrodo a diffusione di gas, i ricercatori sono stati in grado di raggiungere un'efficienza faradaica senza pari (efficienza di trasferimento di carica all'interno di una reazione elettrochimica) del 52,7% e hanno superato il limite del 30% per il C 2 selettività. Niente CO 2 avviene l'emissione. Il successo dell'approccio dipende da uno strato microporoso di fibre di carbonio con un'idrofobicità ottimizzata, che funge da supporto per particelle di rame cataliticamente attive, e una concentrazione ottimizzata di idrossido di potassio nella fase acquosa. Ciò aumenta la concentrazione di CO all'elettrodo e aumenta l'accoppiamento tra gli atomi di carbonio. I prodotti collaterali di questa reazione, etanolo, n-propanolo, e acido acetico, sono liquidi, consentendo una facile separazione dell'etilene gassoso.