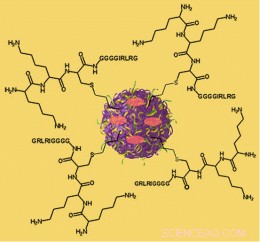
Illustrazione di una particella di nanospugna. Gli ovali rossi rappresentano il carico di farmaci che trasporta e i peptidi attaccati alla superficie che collegano la particella alla superficie di un tumore sono rappresentati in notazione chimica.
(PhysOrg.com) -- Quando viene caricato con un farmaco antitumorale, un sistema di somministrazione basato su un nuovo materiale chiamato nanospugna è da tre a cinque volte più efficace nel ridurre la crescita del tumore rispetto all'iniezione diretta.
Questa è la conclusione di un articolo pubblicato nel numero del 1 giugno della rivista Ricerca sul cancro .
"Sistemi efficaci di somministrazione mirata di farmaci sono stati un sogno per molto tempo ormai, ma sono stati ampiamente frustrati dalla complessa chimica che è coinvolta, "dice Eva Harth, assistente professore di chimica alla Vanderbilt, che ha sviluppato il sistema di consegna nanospugna. "Abbiamo fatto un passo significativo verso il superamento di questi ostacoli".
Lo studio è stato una collaborazione tra il laboratorio di Harth e quello di Dennis E. Hallahan, un ex professore di oncologia delle radiazioni alla Vanderbilt che ora è alla Washington University School of Medicine. Gli autori corrispondenti sono Harth e Roberto Diaz della Emory University, che stava lavorando nel laboratorio di Hallahan al termine degli studi.
Per visualizzare il sistema di consegna di Harth, immagina di creare minuscole spugne delle dimensioni di un virus, riempiendoli con un farmaco e attaccando speciali "linker" chimici che si legano preferenzialmente a una caratteristica che si trova solo sulla superficie delle cellule tumorali e quindi iniettandole nel corpo. Le minuscole spugne circolano intorno al corpo fino a quando non incontrano la superficie di una cellula tumorale dove si attaccano alla superficie (o vengono risucchiate nella cellula) e iniziano a rilasciare il loro potente carico in modo controllabile e prevedibile.
I sistemi di somministrazione mirati di questo tipo hanno diversi vantaggi fondamentali:poiché il farmaco viene rilasciato nel tumore invece di circolare ampiamente attraverso il corpo, dovrebbe essere più efficace per un dato dosaggio. Dovrebbe anche avere meno effetti collaterali dannosi perché quantità minori del farmaco entrano in contatto con i tessuti sani.
"Chiamiamo il materiale nanospugna, ma in realtà è più simile a una rete tridimensionale o a un'impalcatura, " dice Harth. La spina dorsale è un lungo pezzo di poliestere. È mescolato in soluzione con piccole molecole chiamate reticolanti che agiscono come minuscoli rampini per fissare insieme diverse parti del polimero. L'effetto finale è quello di formare particelle di forma sferica riempite con cavità dove possono essere immagazzinate molecole di farmaco.Il poliestere è biodegradabile, quindi si scompone gradualmente nel corpo. Come fa, rilascia il farmaco che trasporta in modo prevedibile.
"Il rilascio prevedibile è uno dei principali vantaggi di questo sistema rispetto ad altri sistemi di rilascio di nanoparticelle in fase di sviluppo, " dice Harth. Quando raggiungono il loro obiettivo, molti altri sistemi scaricano la maggior parte del loro farmaco in modo rapido e incontrollabile. Questo è chiamato effetto burst e rende difficile determinare i livelli di dosaggio efficaci.
Un altro grande vantaggio è che le particelle di nanospugna sono solubili in acqua. L'incapsulamento del farmaco antitumorale nella nanospugna consente l'uso di farmaci idrofobici che non si dissolvono facilmente in acqua. Attualmente, questi farmaci devono essere mescolati con un'altra sostanza chimica, chiamato reagente adiuvante, che riduce l'efficacia del farmaco e può avere effetti collaterali negativi.
È anche possibile controllare la dimensione delle particelle di nanospugna. Variando la proporzione di reticolante rispetto al polimero, le particelle di nanospugna possono essere rese più grandi o più piccole. Questo è importante perché la ricerca ha dimostrato che i sistemi di somministrazione dei farmaci funzionano meglio quando sono inferiori a 100 nanometri, circa la profondità delle fosse sulla superficie di un compact disc. Le particelle di nanospugna utilizzate nel presente studio avevano una dimensione di 50 nanometri. "La relazione tra la dimensione delle particelle e l'efficacia di questi sistemi di somministrazione dei farmaci è oggetto di indagine attiva, "dice Harth.
L'altro grande vantaggio del sistema di Harth è la semplice chimica richiesta. I ricercatori hanno sviluppato semplici, metodi "click chemistry" ad alto rendimento per realizzare le particelle di nanospugna e per attaccare i linker, che sono costituiti da peptidi, molecole biologiche relativamente piccole costruite legando amminoacidi. "Molti altri sistemi di somministrazione di farmaci richiedono una chimica complicata che sarà difficile da scalare per la produzione commerciale, ma questo lo abbiamo sempre tenuto presente, "Dice Harth.
Il peptide mirato utilizzato negli studi sugli animali è stato sviluppato dal laboratorio Hallahan, che ha anche testato l'efficacia del sistema nei topi portatori di tumore. Il peptide utilizzato nello studio è uno che si lega selettivamente ai tumori che sono stati trattati con radiazioni.
Il farmaco utilizzato per gli studi sugli animali era paclitaxel (il nome generico del farmaco Taxol) utilizzato nella chemioterapia antitumorale. I ricercatori hanno registrato la risposta di due diversi tipi di tumore - cancro al seno umano a crescita lenta e glioma di topo ad azione rapida - a singole iniezioni. In entrambi i casi hanno scoperto che aumentava la morte delle cellule tumorali e ritardava la crescita del tumore "in un modo superiore agli approcci chemioterapici conosciuti".
Il prossimo passo è eseguire un esperimento con iniezioni ripetute per vedere se il sistema di nanospugne può fermare e invertire la crescita del tumore. Harth sta anche pianificando di eseguire studi di tossicità più completi sul suo sistema di rilascio di nanoparticelle che sono necessari prima che possa essere utilizzato negli studi clinici.