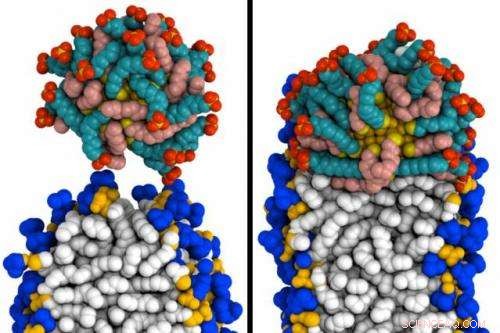
Gli ingegneri del MIT hanno creato simulazioni di come una nanoparticella d'oro ricoperta di molecole speciali può penetrare in una membrana. A sinistra, la particella (in alto) entra in contatto con la membrana. A destra, si è fuso con la membrana. Credito:Reid Van Lehn
Una classe speciale di minuscole particelle d'oro può facilmente scivolare attraverso le membrane cellulari, rendendoli buoni candidati per somministrare farmaci direttamente alle cellule bersaglio.
Un nuovo studio degli scienziati dei materiali del MIT rivela che queste nanoparticelle entrano nelle cellule sfruttando un percorso normalmente utilizzato nella fusione vescicola-vescicola, un processo cruciale che consente la trasmissione del segnale tra i neuroni. Nel numero del 21 luglio di Comunicazioni sulla natura , i ricercatori descrivono in dettaglio il meccanismo con cui queste nanoparticelle sono in grado di fondersi con una membrana.
I risultati suggeriscono possibili strategie per la progettazione di nanoparticelle, realizzate con oro o altri materiali, che potrebbero entrare nelle cellule ancora più facilmente.
"Abbiamo identificato un tipo di meccanismo che potrebbe essere più diffuso di quanto sia attualmente noto, "dice Reid Van Lehn, uno studente laureato del MIT in scienza e ingegneria dei materiali e uno degli autori principali dell'articolo. "Identificando questo percorso per la prima volta suggerisce anche non solo come progettare questa particolare classe di nanoparticelle, ma che questo percorso potrebbe essere attivo anche in altri sistemi".
L'altra autrice principale del documento è Maria Ricci dell'École Polytechnique Fédérale de Lausanne (EPFL) in Svizzera. Il gruppo di ricerca, guidato da Alfredo Alexander-Katz, professore associato di scienza e ingegneria dei materiali, e Francesco Stellacci dell'EPFL, includevano anche scienziati del Carlos Besta Institute of Neurology in Italia e della Durham University nel Regno Unito.
La maggior parte delle nanoparticelle entra nelle cellule attraverso l'endocitosi, un processo che intrappola le particelle in compartimenti intracellulari, che possono danneggiare la membrana cellulare e causare la fuoriuscita del contenuto cellulare. Però, nel 2008, Stellacci, che allora era al MIT, e Darrell Irvine, un professore di scienza e ingegneria dei materiali e di ingegneria biologica, hanno scoperto che una classe speciale di nanoparticelle d'oro rivestite con un mix di molecole potrebbe entrare nelle cellule senza alcuna interruzione.
"Perché questo stava accadendo, o come stava accadendo, era un mistero completo, "Dice Van Lehn.
L'anno scorso, Alexander-Katz, Van Lehn, Stellacci, e altri scoprirono che le particelle si stavano in qualche modo fondendo con le membrane cellulari e venivano assorbite nelle cellule. Nel loro nuovo studio, hanno creato simulazioni atomistiche dettagliate per modellare come ciò accade, e ha eseguito esperimenti che hanno confermato le previsioni del modello.
Entrata invisibile
Le nanoparticelle d'oro utilizzate per la somministrazione dei farmaci sono solitamente rivestite con un sottile strato di molecole che aiutano a regolare le loro proprietà chimiche. Alcune di queste molecole, o ligandi, sono carichi negativamente e idrofili, mentre il resto è idrofobo. I ricercatori hanno scoperto che la capacità delle particelle di entrare nelle cellule dipende dalle interazioni tra ligandi idrofobici e lipidi presenti nella membrana cellulare.
Le membrane cellulari sono costituite da un doppio strato di molecole fosfolipidiche, che hanno code lipidiche idrofobe e teste idrofile. Le code lipidiche sono rivolte l'una verso l'altra, mentre le teste idrofile sono rivolte verso l'esterno.
Nelle loro simulazioni al computer, i ricercatori hanno prima creato quello che chiamano un "doppio strato perfetto, " in cui tutte le code lipidiche rimangono al loro posto all'interno della membrana. In queste condizioni, i ricercatori hanno scoperto che le nanoparticelle d'oro non potevano fondersi con la membrana cellulare.
Però, se la membrana modello include un "difetto" - un'apertura attraverso la quale le code lipidiche possono scivolare fuori - le nanoparticelle iniziano a entrare nella membrana. Quando si verificano queste protrusioni lipidiche, i lipidi e le particelle si aggrappano l'uno all'altro perché sono entrambi idrofobici, e le particelle vengono inghiottite dalla membrana senza danneggiarla.
Nelle membrane cellulari reali, queste sporgenze si verificano casualmente, specialmente vicino a siti in cui le proteine sono incorporate nella membrana. Si verificano anche più spesso nelle sezioni curve della membrana, perché è più difficile per le testine idrofile coprire completamente un'area curva rispetto a una piatta, lasciando spazi vuoti per far sporgere le code lipidiche.
"È un problema di imballaggio, " dice Alexander-Katz. "C'è uno spazio aperto dove possono uscire le code, e ci sarà contatto con l'acqua. Rende solo 100 volte più probabile che una di queste sporgenze fuoriesca in regioni altamente curve della membrana".
Imitando la natura
Questo fenomeno sembra imitare un processo che si verifica naturalmente nelle cellule:la fusione delle vescicole con la membrana cellulare. Le vescicole sono piccole sfere di materiale simile a una membrana che trasportano carichi come neurotrasmettitori o ormoni.
La somiglianza tra l'assorbimento delle vescicole e l'ingresso delle nanoparticelle suggerisce che le cellule in cui si verifica naturalmente molta fusione delle vescicole potrebbero essere buoni bersagli per la somministrazione di farmaci da parte delle nanoparticelle d'oro. I ricercatori intendono analizzare ulteriormente come la composizione delle membrane e le proteine incorporate in esse influenzano il processo di assorbimento in diversi tipi di cellule. "Vogliamo capire davvero tutti i vincoli e determinare come possiamo progettare al meglio le nanoparticelle per colpire particolari tipi di cellule, o regioni di una cellula, "Dice Van Lehn.
"Si potrebbero utilizzare i risultati di questo documento per pensare a come sfruttare questi risultati in veicoli di consegna di nanoparticelle migliorati, ad esempio, forse nuovi ligandi di superficie per nanoparticelle potrebbero essere progettati per avere una migliore affinità sia per i gruppi di superficie che per le code lipidiche, "dice Catherine Murphy, un professore di chimica presso l'Università dell'Illinois a Urbana-Champaign che non è stato coinvolto nello studio.
Questa storia è stata ripubblicata per gentile concessione di MIT News (web.mit.edu/newsoffice/), un popolare sito che copre notizie sulla ricerca del MIT, innovazione e didattica.