
Anastasia Ilgen, ricercatrice dei Sandia National Laboratories, conduce esperimenti in un vano portaoggetti anaerobico. Credito:Randy Montoya
I ricercatori dei Sandia National Laboratories hanno scoperto il meccanismo per "accendere" il ferro che risiede nelle strutture minerali argillose, portando alla comprensione di come rendere reattivo il ferro in condizioni di assenza di ossigeno.
Questa ricerca aiuterà gli scienziati a capire e prevedere come i contaminanti, come l'arsenico, selenio e cromo, muoversi attraverso l'ambiente ed entrare nei corsi d'acqua. Questi principi chimici possono essere applicati per sviluppare barriere naturali del suolo per rimuovere questi contaminanti dall'acqua e creare membrane reattive, che possono trasformare i contaminanti durante il processo di filtrazione dell'acqua.
L'opera è presente sulla copertina di un recente numero di Scienze ambientali:nano in un documento intitolato, "'Accendendo' il ferro nei minerali argillosi, " della ricercatrice Sandia Anastasia Ilgen, Kevin Leung e Rachel Washington e Ravi Kukkadapu del Pacific Northwest National Laboratory. Il lavoro è stato finanziato dal programma di Scienze Energetiche di Base del Dipartimento dell'Energia.
Capire le reazioni del ferro
"Nelle geoscienze, abbiamo riconosciuto da decenni che capire come reagisce il ferro è fondamentale per capire come i contaminanti si muovono e si trasformano nell'ambiente, " ha detto l'autore principale Ilgen.
Il ferro è un costituente chiave della crosta terrestre e il quarto elemento più comune. I minerali contenenti ferro costituiscono gran parte dei suoli e delle rocce sedimentarie. L'adsorbimento e le trasformazioni chimiche su superfici minerali contenenti ferro definiscono il destino e il trasporto delle sostanze chimiche nell'ambiente. Adsorbimento, che è l'attaccamento di contaminanti su superfici minerali, e le reazioni chimiche su queste superfici minerali regolano il modo in cui queste sostanze chimiche si muovono attraverso l'ambiente.
Ilgen spiega che il ferro nei suoli può esistere in due stati di ossidazione:ridotto e ossidato. Questo è importante, perché il ferro si alterna costantemente tra queste forme in risposta a lievi cambiamenti nelle condizioni del suolo.
"I minerali argillosi sono estremamente comuni nei terreni e spesso contengono ferro nelle loro strutture, " disse. "Le superfici dei minerali argillosi, che contengono solo ferro ossidato, non sono reattivi. Assorbono l'arsenico, ma non trasformarlo chimicamente. Però, queste stesse superfici diventano reattive non appena una minore quantità di ferro ridotto viene introdotta nella struttura del minerale argilloso."
Fino ad ora, non era noto come e perché i minerali argillosi con tracce di ferro ridotto reagissero in assenza di ossigeno.
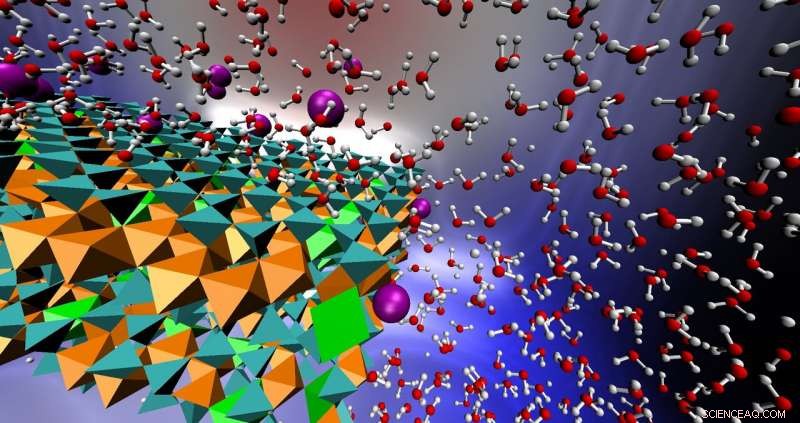
Questo grafico rappresenta il sistema reattivo descritto nel documento, che mostra la struttura del minerale argilloso nontronite con ferro ossidato (arancione) e ferro ridotto (verde brillante) circondato da acqua e ioni di arsenico (viola). Credito:Tuan Ho
"Abbiamo scoperto il meccanismo con cui il ferro ossidato nelle strutture minerali argillose reagisce in condizioni di assenza di ossigeno, e perché sono necessarie tracce di ferro ridotto affinché le reazioni abbiano luogo, " ha detto Ilgen.
Il team conduce il lavoro utilizzando vari strumenti, metodi
Utilizzando strumenti sperimentali, il team ha individuato i siti chimici esatti nei minerali argillosi che hanno reagito con l'arsenico. Il team ha dimostrato che gli atomi di ferro situati ai bordi dei minerali argillosi erano reattivi, e affinché le reazioni abbiano luogo questi siti devono contenere sia ferro ridotto che ferro ossidato.
Il team ha utilizzato metodi computazionali per calcolare l'energia necessaria per ossidare l'arsenico, che viene adsorbito su un sito contenente esclusivamente ferro ossidato rispetto a un sito con ferro sia ossidato che ridotto. Questi calcoli hanno mostrato che l'aggiunta termodinamica di un ferro ridotto accanto a un ferro ossidato non rende più favorevole l'ossidazione dell'arsenico.
Quindi, la domanda diventa perché i siti sono reattivi nell'ambiente? Utilizzando l'analisi spettroscopica, il team ha dimostrato che per un contaminante, come l'arsenico, ossidarsi sulla superficie di un minerale argilloso, deve spostare le molecole d'acqua dalla superficie di quel minerale argilloso. Il distacco di una molecola d'acqua è un passaggio chimico necessario per attaccare l'arsenico, per poterlo ossidare sulla superficie del minerale argilloso.
I calcoli mostrano che la rimozione dell'acqua da un sito con ferro sia ridotto che ossidato utilizza meno energia rispetto a un sito che contiene solo ferro ossidato. Perché consuma meno energia, è più facile attaccare e poi ossidare l'arsenico su questo tipo di sito chimico sulla superficie del minerale argilloso ed è per questo che avviene la reazione.
Comprendere questo meccanismo aiuta a spiegare il destino e il trasporto di nutrienti e contaminanti sensibili all'ossidoriduzione nell'ambiente, e perché alcuni di questi persistono in forme ossidate anche in assenza di ossigeno disciolto.
Continua ricerca sul ferro in diversi minerali naturali
Ilgen ha affermato che il team continuerà a ricercare i meccanismi chimici che regolano la reattività del ferro in diversi minerali naturali ed esplorerà le condizioni necessarie affinché il ferro sia reattivo nei suoli e nelle rocce sedimentarie.
Il team utilizzerà queste conoscenze per comprendere meglio il destino ambientale e il trasporto di contaminanti e nutrienti, e potenzialmente progettare barriere reattive per impedire ai contaminanti di entrare nei corsi d'acqua.