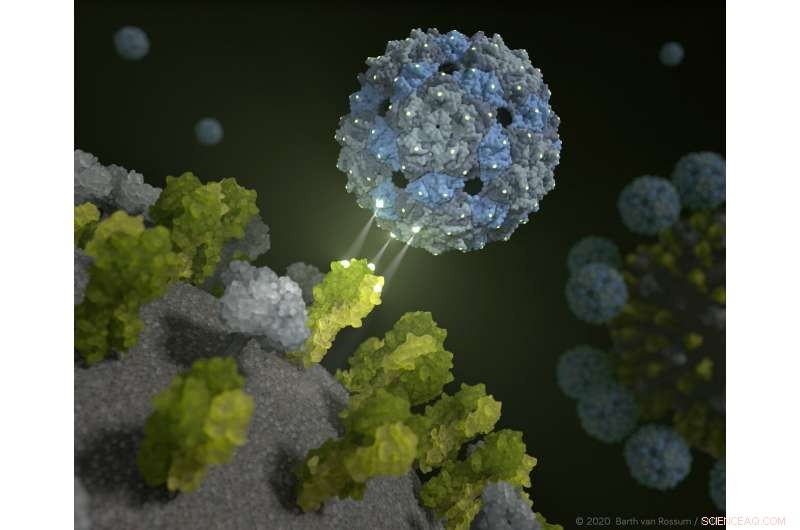
Il guscio fagico si aggancia e inibisce il virus dell'influenza. Credito:Barth van Rossum / FMP
Un nuovo approccio porta la speranza di nuove opzioni terapeutiche per sopprimere l'influenza stagionale e l'influenza aviaria. Sulla base di un guscio vuoto e quindi non infettivo di un virus fago, ricercatori di Berlino hanno sviluppato un capside fagico chimicamente modificato che soffoca i virus dell'influenza.
I siti di legame perfettamente adattati fanno sì che i virus dell'influenza siano avvolti dai capsidi fagici in modo tale che è praticamente impossibile per loro infettare le cellule polmonari. Questo fenomeno è stato dimostrato in studi preclinici utilizzando tessuto polmonare umano. Ricercatori del Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP), Freie Universität di Berlino, Technische Universität Berlino (TU), Humboldt-Universität (HU), il Robert Koch Institute (RKI) e la Charité-Universitätsmedizin Berlin riferiscono che i risultati vengono utilizzati anche per l'indagine immediata sul coronavirus. I risultati sono stati ora pubblicati in Nanotecnologia della natura .
I virus dell'influenza sono ancora molto pericolosi. L'Organizzazione Mondiale della Sanità (OMS) stima che l'influenza sia responsabile fino a 650, 000 decessi all'anno in tutto il mondo. Gli attuali farmaci antivirali sono solo parzialmente efficaci perché attaccano il virus dell'influenza dopo che le cellule polmonari sono state infettate. Sarebbe auspicabile, e molto più efficace, prevenire l'infezione in primo luogo.
Questo è esattamente ciò che promette il nuovo approccio di Berlino. Il capside fagico, sviluppato da un team multidisciplinare di ricercatori, avvolge i virus dell'influenza in modo così perfetto che non possono più infettare le cellule. "Gli studi preclinici dimostrano che siamo in grado di rendere innocui sia i virus dell'influenza stagionale che i virus dell'influenza aviaria con il nostro guscio fago modificato chimicamente, " ha spiegato il professor Dr. Christian Hackenberger, Capo del dipartimento di biologia chimica del Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP) e professore di biologia chimica di Leibniz Humboldt all'HU di Berlino. "Si tratta di un grande successo che offre prospettive completamente nuove per lo sviluppo di farmaci antivirali innovativi".
Legami multipli si adattano come il velcro
Il nuovo inibitore fa uso di recettori trivalenti sulla superficie del virus dell'influenza, denominata proteina emoagglutinina, che si attaccano alle molecole di zucchero (acidi sialici) sulle superfici cellulari del tessuto polmonare. In caso di infezione, i virus si agganciano alla loro vittima, in questo caso, cellule polmonari, come una chiusura a strappo. Il principio fondamentale è che queste interazioni si verificano a causa di più legami, piuttosto che singole obbligazioni.
È stata la struttura superficiale dei virus influenzali che ha ispirato i ricercatori a porre la seguente domanda iniziale più di sei anni fa:non sarebbe possibile sviluppare un inibitore che si leghi ai recettori trivalenti con una perfetta aderenza, simulando la superficie delle cellule del tessuto polmonare?
Hanno scoperto che questo è davvero possibile con l'aiuto di un innocuo abitante intestinale:il fago Q-beta ha le proprietà superficiali ideali ed è particolarmente adatto per dotarlo di ligandi, in questo caso, molecole di zucchero, come "esca". Un guscio fago vuoto fa perfettamente il lavoro. "La nostra molecola multivalente dell'impalcatura non è infettiva, e comprende 180 proteine identiche che sono distanziate esattamente come i recettori trivalenti dell'emoagglutinina sulla superficie del virus, " ha spiegato il dottor Daniel Lauster, un ex dottorato di ricerca studente nel Gruppo di Biofisica Molecolare (HU) e ora postdoc alla Freie Universität Berlin. "Ha quindi le condizioni di partenza ideali per ingannare il virus dell'influenza, o, per essere più precisi, per attaccarlo con un perfetto adattamento spaziale. In altre parole, usiamo un virus fago per disabilitare il virus dell'influenza!"
Per consentire allo scaffold Q-beta di svolgere la funzione desiderata, deve prima essere modificato chimicamente. Prodotto da batteri E. coli presso TU Berlin, Il gruppo di ricerca del professor Hackenberger presso FMP e HU Berlin utilizza la chimica sintetica per attaccare le molecole di zucchero alle posizioni definite del guscio del virus.
Il virus è ingannato e avvolto
Diversi studi che utilizzano modelli animali e colture cellulari hanno dimostrato che la struttura sferica opportunamente modificata possiede una notevole forza di legame e un potenziale di inibizione. Lo studio ha anche permesso al Robert Koch Institute di esaminare il potenziale antivirale dei capsidi fagici contro molti ceppi di virus influenzali attuali, e anche contro i virus dell'influenza aviaria. Il suo potenziale terapeutico è stato anche dimostrato sul tessuto polmonare umano, come colleghi ricercatori del Dipartimento di Medicina, Divisione di Infettivologia e Pneumologia, di Charité sono stati in grado di dimostrare:quando il tessuto infetto da virus influenzali è stato trattato con il capside fagico, i virus influenzali non erano praticamente più in grado di riprodursi.
I risultati sono supportati da prove strutturali da parte degli scienziati FU del Centro di ricerca di microscopia elettronica (FZEM):la microscopia crioelettronica ad alta risoluzione e la microscopia crioelettronica mostrano direttamente e spazialmente che l'inibitore incapsula completamente il virus. Inoltre, sono stati utilizzati modelli matematico-fisici per simulare l'interazione tra i virus dell'influenza e il capside fagico al computer. "I nostri calcoli computerizzati mostrano che l'inibitore progettato razionalmente si lega davvero all'emoagglutinina, e avvolge completamente il virus dell'influenza, " ha confermato la dott.ssa Susanne Liese dell'AG Netz della Freie Universität di Berlino. "È stato quindi anche possibile descrivere e spiegare matematicamente l'elevata forza di adesione".
Il potenziale terapeutico richiede ulteriori ricerche
Questi risultati devono ora essere seguiti da ulteriori studi preclinici. Non è ancora noto, Per esempio, se il capside fagico provoca una risposta immunitaria nei mammiferi. Idealmente, questa risposta potrebbe anche aumentare l'effetto dell'inibitore. Però, potrebbe anche essere il caso che una risposta immunitaria riduca l'efficacia dei capsidi fagici in caso di esposizione a dosi ripetute, o che i virus influenzali sviluppano resistenze. E, Certo, deve ancora essere dimostrato che l'inibitore sia efficace anche nell'uomo.
Ciò nonostante, l'alleanza dei ricercatori berlinesi è certa che l'approccio abbia un grande potenziale. "Il nostro razionalmente sviluppato, tridimensionale, l'inibitore multivalente indica una nuova direzione nello sviluppo di leganti del virus dell'influenza strutturalmente adattabili. Questo è il primo risultato del suo genere nella ricerca multivalenza, " ha sottolineato il professor Hackenberger. Il chimico ritiene che questo approccio, che è biodegradabile, non tossico e non immunogeno negli studi sulle colture cellulari, può in linea di principio essere applicato anche ad altri virus, e forse anche ai batteri. È evidente che gli autori considerano l'applicazione del loro approccio all'attuale coronavirus come una delle loro nuove sfide. L'idea è di sviluppare un farmaco che impedisca ai coronavirus di legarsi alle cellule ospiti situate nella gola e nelle successive vie aeree, prevenendo così l'infezione.