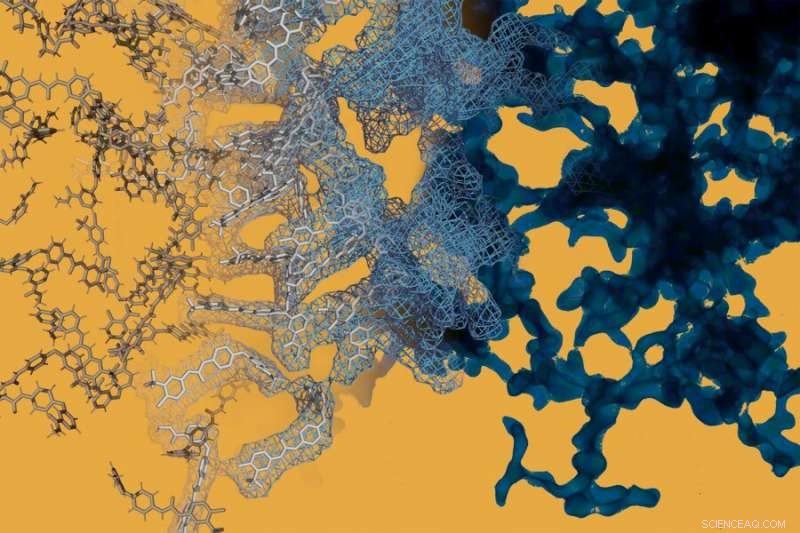
Una simulazione di dinamica molecolare (a sinistra) è giustapposta a un'immagine al microscopio elettronico (a destra) del farmaco antitumorale sorafenib. Sorafenib, come molti altri farmaci a piccole molecole, possono formare spontaneamente intricate strutture su nanoscala che modificano il comportamento del farmaco. Credito:Daniel Reker
Le terapie a piccole molecole trattano un'ampia varietà di malattie, ma la loro efficacia è spesso ridotta a causa della loro farmacocinetica, ovvero ciò che il corpo fa a un farmaco. Dopo la somministrazione, il corpo determina quanto del farmaco viene assorbito, in quali organi entra il farmaco, e quanto velocemente il corpo metabolizza ed espelle nuovamente il farmaco.
Nanoparticelle, generalmente costituito da lipidi, polimeri, o entrambi, può migliorare la farmacocinetica, ma possono essere complessi da produrre e spesso trasportano molto poco del farmaco.
È stato dimostrato che alcune combinazioni di farmaci antitumorali a piccole molecole e due coloranti a piccole molecole si autoassemblano in nanoparticelle con carichi utili estremamente elevati di farmaci, ma è difficile prevedere quali partner di piccole molecole formeranno nanoparticelle tra i milioni di possibili accoppiamenti.
I ricercatori del MIT hanno sviluppato una piattaforma di screening che combina l'apprendimento automatico con la sperimentazione ad alto rendimento per identificare rapidamente le nanoparticelle autoassemblanti. In uno studio pubblicato su Nanotecnologia della natura , i ricercatori hanno esaminato 2,1 milioni di accoppiamenti di farmaci a piccole molecole e ingredienti di farmaci "inattivi", identificare 100 nuove nanoparticelle con potenziali applicazioni che includono il trattamento del cancro, asma, malaria, e infezioni virali e fungine.
"Abbiamo precedentemente descritto alcuni degli effetti negativi e positivi che gli ingredienti inattivi possono avere sui farmaci, e qui, attraverso una collaborazione concertata tra i nostri laboratori e le strutture principali, descrivere un approccio incentrato sui potenziali effetti positivi che questi possono avere sulla nanoformulazione, "dice Giovanni Traverso, il Karl Van Tassel (1925) Professore di sviluppo professionale di ingegneria meccanica, e autore corrispondente senior dello studio.
Le loro scoperte indicano una strategia che risolve sia la complessità della produzione di nanoparticelle che la difficoltà di caricare su di esse grandi quantità di farmaci.
"Così tanti farmaci là fuori non sono all'altezza del loro pieno potenziale a causa di un targeting insufficiente, bassa biodisponibilità, o un rapido metabolismo dei farmaci, "dice Daniel Reker, autore principale dello studio ed ex postdoc nel laboratorio di Robert Langer. "Lavorando all'interfaccia della scienza dei dati, apprendimento automatico, e consegna di farmaci, la nostra speranza è quella di espandere rapidamente il nostro set di strumenti per assicurarci che un farmaco arrivi dove deve essere e possa effettivamente curare e aiutare un essere umano".
Langer, il David H. Koch Institute Professor al MIT e membro del Koch Institute for Integrative Cancer Research, è anche un autore senior del documento.
Una terapia contro il cancro incontra la sua partita
Al fine di sviluppare un algoritmo di apprendimento automatico in grado di identificare nanoparticelle autoassemblanti, i ricercatori avevano prima bisogno di creare un set di dati su cui addestrare l'algoritmo. Hanno selezionato 16 farmaci a piccole molecole autoaggreganti con una varietà di strutture chimiche e applicazioni terapeutiche e un insieme diversificato di 90 composti ampiamente disponibili, compresi gli ingredienti che sono già stati aggiunti ai farmaci per migliorarne il sapore, durare più a lungo, o renderli più stabili. Poiché sia i farmaci che gli ingredienti inattivi sono già approvati dalla FDA, le nanoparticelle risultanti saranno probabilmente più sicure e passeranno più rapidamente attraverso il processo di approvazione della FDA.
Il team ha quindi testato ogni combinazione di farmaco a piccola molecola e ingrediente inattivo, abilitato dal Swanson Biotechnology Center, una serie di strutture principali che forniscono servizi tecnici avanzati all'interno del Koch Institute. Dopo aver miscelato gli accoppiamenti e caricato 384 campioni alla volta su piastre a nanopozzetti utilizzando la robotica nel nucleo High Throughput Sciences, i ricercatori hanno camminato sui piatti, spesso con campioni in rapida degradazione, accanto al nucleo di Peterson (1957) Nanotechnology Materials Core Facility per misurare la dimensione delle particelle con diffusione dinamica della luce ad alto rendimento.
Ora addestrato su 1, 440 punti dati (con 94 nanoparticelle già identificate), la piattaforma di apprendimento automatico potrebbe essere attivata su una libreria di composti molto più ampia. Screening di 788 farmaci a piccole molecole contro più di 2, 600 ingredienti farmacologici inattivi, la piattaforma individuata 38, 464 potenziali nanoparticelle autoassemblanti da 2,1 milioni di possibili combinazioni.
I ricercatori hanno selezionato sei nanoparticelle per un'ulteriore convalida, compreso uno composto da sorafenib, un trattamento comunemente usato per il fegato avanzato e altri tumori, e glicirrizina, un composto frequentemente usato sia come additivo alimentare che farmacologico e più comunemente noto come aroma di liquirizia. Sebbene il sorafenib sia lo standard di cura per il carcinoma epatico avanzato, la sua efficacia è limitata.
Nelle colture cellulari di cancro al fegato umano, le nanoparticelle di sorafenib-glicirrizina hanno funzionato due volte meglio del sorafenib da solo perché più del farmaco potrebbe entrare nelle cellule. Lavorare con la modellazione preclinica, Imaging and Testing facility presso il Koch Institute, i ricercatori hanno trattato modelli murini di cancro al fegato per confrontare gli effetti delle nanoparticelle di sorafenib-glicirrizina rispetto a entrambi i composti da soli. Hanno scoperto che la nanoparticella ha ridotto significativamente i livelli di un marker associato alla progressione del cancro al fegato rispetto ai topi a cui era stato somministrato solo sorafenib, e ha vissuto più a lungo dei topi a cui era stato somministrato solo sorafenib o glicirrizina. La nanoparticella sorafenib-glicirrizina ha anche mostrato un migliore targeting per il fegato rispetto alla somministrazione orale di sorafenib, lo standard attuale nella clinica, o quando si inietta sorafenib dopo che è stato combinato con cremoforo, un veicolo farmacologico comunemente usato che migliora la solubilità in acqua ma ha effetti collaterali tossici.
Consegna personalizzata dei farmaci
La nuova piattaforma potrebbe avere applicazioni utili oltre all'ottimizzazione dell'efficienza dei farmaci attivi:potrebbe essere utilizzata per personalizzare i composti inattivi in base alle esigenze dei singoli pazienti. In lavori precedenti, i membri del team hanno scoperto che gli ingredienti inattivi potrebbero provocare reazioni allergiche avverse in alcuni pazienti. Ora, con il toolbox ampliato di machine learning, potrebbero essere generate più opzioni per fornire alternative a questi pazienti.
"Abbiamo l'opportunità di pensare ad abbinare il sistema di consegna al paziente, " spiega Reker, ora assistente professore di ingegneria biomedica alla Duke University. "Possiamo spiegare cose come l'assorbimento dei farmaci, genetica, anche le allergie per ridurre gli effetti collaterali al momento del parto. Qualunque sia la mutazione o la condizione medica, il farmaco giusto è il farmaco giusto solo se funziona davvero per il paziente".
Gli strumenti per la sicurezza, esiste un'efficace somministrazione di farmaci, ma mettere insieme tutti gli ingredienti può essere un processo lento. La combinazione di apprendimento automatico, screening rapido, e la capacità di prevedere le interazioni tra diverse combinazioni di materiali accelererà la progettazione di farmaci e le nanoparticelle utilizzate per distribuirli in tutto il corpo.
Nei lavori in corso, il team sta cercando non solo di migliorare la somministrazione efficace dei farmaci, ma anche di creare opportunità per creare farmaci per le persone per le quali le formulazioni standard non sono una buona opzione, utilizzare i big data per risolvere problemi in piccole popolazioni esaminando la storia genetica, allergie, e reazioni alimentari.
Questa storia è stata ripubblicata per gentile concessione di MIT News (web.mit.edu/newsoffice/), un popolare sito che copre notizie sulla ricerca del MIT, innovazione e didattica.