Astratto grafico. Credito:DOI:10.1038/s41565-021-00976-3
Il professor Kevin Braeckmans dell'Università di Gand ha concentrato gli ultimi 10 anni su un metodo per l'ingegneria sicura di cellule terapeutiche con nanofibre fototermiche. Oggi, Natura Nanotecnologia fornisce informazioni su come sono state sviluppate queste nanofibre fototermiche biocompatibili e su come, dopo l'irradiazione laser, le cellule che entrano in contatto con tali nanofibre diventano permeabili e possono essere trasfettate con una varietà di molecole effettrici, inclusi i complessi ribonucleoproteici CRISPR/Cas9 e siRNA. Il professor Braeckmans e il suo team hanno dimostrato che le cellule, come le cellule staminali embrionali e le cellule T umane, trasfettate con tali nanofibre sono in ottima salute e mantengono la loro funzionalità terapeutica.
Nuova base per le terapie cellulari
Le terapie cellulari costituiscono una nuova forma di trattamento in cui cellule geneticamente modificate vengono iniettate nel paziente per prevenire o curare malattie. Un esempio ben noto è l'uso delle cellule immunitarie di un malato di cancro che possono essere isolate, geneticamente modificate ed espanse in un ambiente di laboratorio e reinfuse nel paziente per attaccare le cellule tumorali. La modificazione genetica delle cellule dipende dalle tecnologie di somministrazione intracellulare che spesso lottano per ottenere un'efficienza sufficiente pur avendo un impatto minimo sulla salute e sul funzionamento della cellula.
La fotoporazione sensibilizzata alle nanoparticelle è particolarmente promettente a questo proposito in quanto fornisce in genere alta efficienza, elevata produttività e bassa tossicità. Si basa sull'uso di nanoparticelle sensibili alla luce, come le nanoparticelle d'oro (NP), che possono formare nanobolle esplosive dopo l'irradiazione laser pulsata. Quelle minuscole esplosioni possono indurre piccoli pori nelle membrane cellulari, consentendo alle molecole effettrici esterne integrate nel mezzo cellulare di entrare nelle cellule. Tuttavia, la traduzione della fotoporazione sensibilizzata alle nanoparticelle alle applicazioni cliniche è ostacolata dal fatto che le cellule sono state in contatto con nanoparticelle (non degradabili), ponendo problemi tossicologici e normativi.
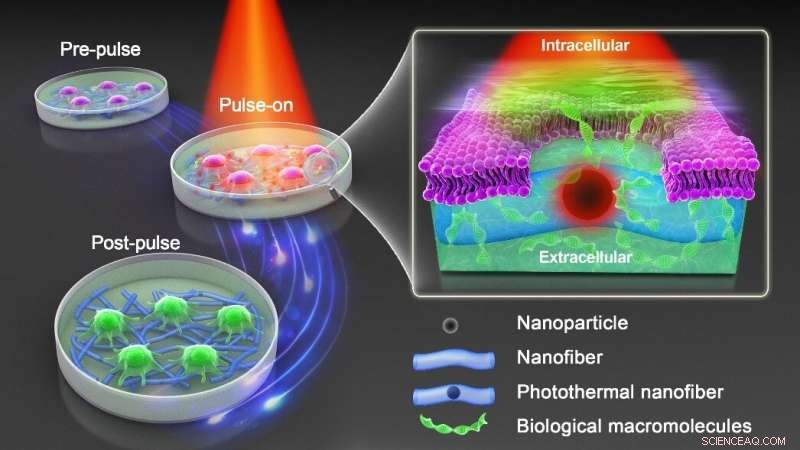
Pertanto, è necessario un nuovo approccio che mantenga il vantaggio della fotoporazione sensibilizzata alle nanoparticelle evitando il contatto diretto di nanoparticelle e cellule. Come mostrato nella figura sopra, il professor Braeckmans e il suo team hanno incorporato nanoparticelle fototermiche di ossido di ferro (IONP) in nanofibre polimeriche biocompatibili che sono state prodotte mediante elettrofilatura. Il policaprolattone (PCL) è un polimero biocompatibile ampiamente utilizzato nelle applicazioni biomediche, mentre gli IONP sono economici e hanno un ampio spettro di assorbimento della luce.
Dimostrano che sia le cellule aderenti che quelle in sospensione possono essere trasfettate in modo sicuro ed efficiente con una gamma di macromolecole dopo l'irradiazione con impulsi laser di nanosecondi. Eseguendo l'analisi elementare tramite spettrometria di massa plasma-tandem accoppiata induttivamente (ICP-MS/MS), confermano che gli IONP rimangono incorporati in modo sicuro nelle nanofibre dopo l'irradiazione laser in modo che le cellule trattate siano effettivamente libere dall'esposizione diretta alle nanoparticelle. Sono state eseguite simulazioni numeriche sul trasferimento di calore da IONP incorporati in fibra alle cellule vicine per comprendere meglio come la fluenza dell'impulso laser, la distribuzione IONP e lo stato di aggregazione influenzano la permeabilità della membrana cellulare.
Sperimentalmente il team ha dimostrato che la fotoporazione con nanofibre fototermali potrebbe fornire con successo molecole biologiche funzionali, tra cui siRNA o ribonucleoproteine (RNPs) CRISP-Cas9, sia alle cellule aderenti che in sospensione, comprese le cellule staminali embrionali umane (hESC) e le cellule T umane primarie. Come benchmark è stato eseguito un confronto con l'elettroporazione all'avanguardia. Mentre le cellule elettroporate hanno subito modifiche al loro fenotipo e funzionalità, questo non è stato il caso delle cellule fotoporate che hanno mantenuto la loro capacità di proliferare e, nel caso delle cellule CAR-T, di uccidere le cellule tumorali. Infine, la fotoporazione PEN è stata utilizzata per trasfettare le cellule CAR-T con siRNA mirato al recettore PD1, un noto inibitore del checkpoint immunitario. È stato confermato che le cellule trattate con siPD1 hanno una maggiore capacità di uccidere il tumore in vivo.
Insieme, mostra che la fotoporazione con nanofibre fototermiche consente la consegna intracellulare efficiente e sicura di un'ampia gamma di molecole effettrici in una varietà di tipi cellulari senza contatto con nanoparticelle fototermali potenzialmente tossiche. "Riteniamo che questo sia un passo importante verso l'uso della fotoporazione per la produzione sicura ed efficiente di terapie cellulari modificate geneticamente", afferma il professor Braeckmans. + Esplora ulteriormente