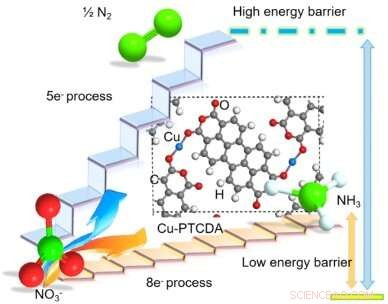
Struttura proposta di PTCDA con Cu-incorporato e diagramma schematico che illustra il vantaggio di ridurre selettivamente NO3− in NH3 tramite trasferimento diretto di 8 elettroni. Rosso, bianco, grigio, blu brillante, e le sfere verdi rappresentano la O, H, C, Cu, e N atomi, rispettivamente. Credito:Chen et al.
ammoniaca (NH 3 ) è un incolore, composto gassoso e idrosolubile utilizzato in diversi settori, compresa l'agricoltura, il settore energetico, e una varietà di industrie. Da oltre un secolo, il modo principale per produrre grandi quantità di ammoniaca è stato il processo Haber-Bosch, che prevede l'uso dell'alta pressione per produrre una reazione chimica che consente la sintesi diretta di ammoniaca da idrogeno e azoto.
Mentre il processo Haber-Bosch consente la produzione di massa di ammoniaca, è noto per essere dannoso sia per l'uomo che per l'ambiente, in quanto comporta il consumo di combustibili fossili e quindi aggrava l'effetto serra. A causa di questi effetti indesiderati, i ricercatori hanno cercato metodi alternativi per produrre ammoniaca tramite N 2 −H 2 O reazioni chimiche in condizioni ambientali, alcuni dei quali utilizzano fonti energetiche rinnovabili.
Alcune di queste nuove tecniche per la produzione di ammoniaca si sono rivelate efficaci e relativamente poco costose. Ciò nonostante, in genere consentivano ai ricercatori solo di produrre quantità limitate di ammoniaca e mostravano una scarsa selettività, grazie al legame inerte N≡N e alla bassissima solubilità di N 2 in acqua.
I ricercatori della South China University of Technology e dell'Argonne National Laboratory hanno recentemente ideato una nuova strategia elettrochimica per produrre ammoniaca attraverso la riduzione dei nitrati. Il loro metodo, introdotto in un articolo pubblicato in Energia della natura , si basa sull'uso di un catalizzatore solido rame-molecolare.
"Ottenendo NH 3 direttamente da non−N 2 è considerata una strategia rivoluzionaria per affrontare le preoccupazioni associate ai precedenti processi di produzione dell'ammoniaca, "Haihui Wang, uno dei ricercatori che ha condotto lo studio, ha detto a Phys.org. "Nella ricerca di alternative contenenti azoto diverse dal N 2 sintetizzare NH 3 , l'anione nitrato (NO 3 - ) si distingue per il fatto che la minore energia di dissociazione del legame N=O (204 kJ mol -1 ) rispetto al triplo legame N-N (941 kJ mol -1 ), e l'arricchimento di NO 3 - nelle risorse idriche causa inquinamento ambientale e minaccia la salute umana".
Conversione selettiva di NO 3 - a NH 3 in condizioni ambientali e in un H 2 Il sistema basato su O potrebbe essere un'alternativa più ecologica per la produzione di massa di NH 3 . Questa conversione alternativa allevierebbe i problemi ambientali associati agli attuali metodi per la produzione di ammoniaca su larga scala, riducendo anche il consumo di energia.
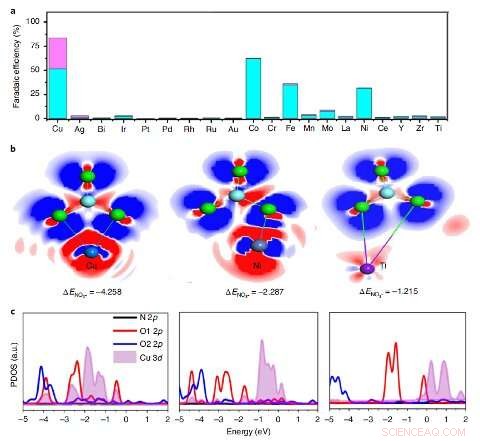
Screening dell'elemento con la più alta attività. un, L'efficienza faradaica di NH3 (blu) e NO2− (malva) di vari elementi incorporati in PTCDA sotto un potenziale di -0,4 V rispetto a RHE. B, L'EDD di NO3– su 1Cu–PTCDA(¬103) (a sinistra), 1Ni–PTCDA(¬103) (al centro) e 1Ti–PTCDA(¬103) (a destra). Blu, blu scuro, viola, le sfere azzurre e verdi rappresentano il Cu, Ni, Ti, atomi di N e O, rispettivamente. La nuvola elettronica blu indica l'accumulo di carica e la nuvola elettronica rossa indica l'esaurimento della carica. C, La densità di stati proiettata (PDOS) di *NO3 su 1Cu–PTCDA (¬103) (a sinistra), 1Ni–PTCDA(¬103) (al centro) e 1Ti–PTCDA(¬103) (a destra). Credito:Chen et al.
"Convertire NO 3 − in NH 3 è tutt'altro che un compito facile, poiché richiede una reazione di trasferimento di otto elettroni e un potenziale di reazione leggermente inferiore (cioè, 1,20 V rispetto all'elettrodo a idrogeno reversibile o RHE) rispetto a quello della conversione a cinque elettroni di NO 3 − tonnellata 2 (1,25 V rispetto a RHE), " Wang ha spiegato. "Vari sistemi elettrocatalitici con diversi catalizzatori eterogenei (come Cu, Ag, Au, e così via) sono stati proposti in passato, ma la maggior parte di essi tende a produrre N 2 tramite riduzione a cinque elettroni di NO 3 - piuttosto che la riduzione a otto elettroni desiderata."
Il potenziale pratico della conversione di NO 3 - a NH 3 è inferiore a quello che è noto come potenziale di reazione di evoluzione dell'idrogeno (HER), che porta alla generazione di H 2 . Ciò può ridurre l'efficienza complessiva della produzione di NH 3 .
Nel loro studio, Wang e i suoi colleghi sono stati in grado di ottenere la riduzione diretta di otto elettroni di NO 3 - a NH 3, catalizzato da Cu-incorporato cristallino 3, 4, 9, Dianidride 10-perilentetracarbossilica (PTCDA) con una via di barriera a bassa energia. Il catalizzatore che hanno usato ha mostrato un alto tasso di resa e un'eccezionale selettività, sopprimendo efficacemente LEI.
"Abbiamo vagliato i catalizzatori con la preparazione di una serie di metalli incorporati in PTCDA, come Cu, Ag, Au, Ru, RH, io, Pd, pt, Bi, Ti, Cr, mn, Fe, Co, Ni, si, Zr, Mo, La e Ce, " ha spiegato Wang. "Abbiamo scoperto che le elevate prestazioni del nostro catalizzatore possono essere attribuite alla configurazione elettronica unica di Cu 3 D orbitale che mostra una maggiore sovrapposizione con nitrato O 2 P orbitali per migliorare il trasferimento di carica, così come la struttura di PTCDA, che aiuta a regolare il trasferimento di protoni ed elettroni ai centri Cu attivi e quindi a inibire HER e promuovere il legame H-N."
Il metodo elettrochimico introdotto da Wang e dai suoi colleghi potrebbe affrontare le sfide attualmente associate all'NH . di massa 3 produzione. Nelle prove iniziali, questo metodo ha raggiunto efficienze faradaiche tra il 60% e l'86% e NH 3 tassi di produzione tra circa 400 e 900 μg h –1 cm –2 a potenziali applicati da -0,4 a -0,6 V rispetto a RHE.
I risultati sono significativamente migliori di quelli ottenuti utilizzando altri metodi per la riduzione elettrochimica di N 2 a NH 3 . Per esempio, metodi mediati dal litio, che sono i più noti per ottenere tassi di rendimento relativamente elevati nell'elettroriduzione di N 2 -to-NH 3 , raggiunto un tasso di produzione inferiore a 36 μg h -1 cm.
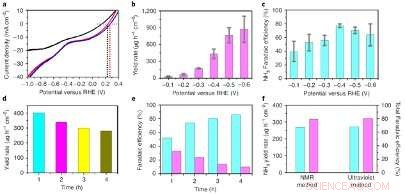
Prestazioni elettrocatalitiche di O-Cu-PTCDA. un, Curve voltammetriche a scansione lineare di O-Cu-PTCDA testate in 0,1 M PBS (nero), 0,1 M PBS che conteneva NO2- (rosso) e 0,1 M PBS che conteneva NO3- (blu). B, Resa di NH3 a diversi potenziali alla seconda ora. C, NH3 Efficienza faradaica a diversi potenziali alla seconda ora. D, Tasso di resa NH3 in tempi diversi a -0,4 V rispetto a RHE fino a 4 h. e, NH3 (blue) and NO2− (mauve) Faradaic efficiencies at different times at −0.4 V versus RHE up to 4 h. f, The overall NH3 yield rate (blue) and total Faradaic efficiency (mauve) detected by 1H NMR spectroscopy and an indophenol blue method after the 4-h experiment. Credito:Chen et al.
The recent study by Wang and his colleagues also opens up new possibilities for the recycling of nitrogen (NO 3 - ) in wastewater. For several years, NO 3 - was considered to be a toxic water contaminant and was usually transferred into gaseous nitrogen and returned to the air. Recent studies, però, suggest that the high amount of nitrogen in wastewater could in fact be recycled for fertilization.
"The total nitrogen discharged into the water per year is 14.5 ± 3.1 million tons in China, which is about 50% of the annual consumption of synthetic nitrogen (300.5 million tons in 2016), " Wang said. "In 2016, the United States planted 94 million acres of corn, using about 8.9 billion kilograms of nitrogen annually, which accounts for 40% of the annual nitrogen use in the United States. Però, it is worth noting that 2.4 billion kilograms of nitrogen is available in wastewater each year. The statistics prove that nitrogen in wastewaters could be a valuable resource."
In addition to allowing the large-scale production of ammonia in ways that are more environmentally friendly, the recent work by Wang and his colleagues could pave the way toward the development of wastewater management systems with nitrogen conversion capabilities. These systems would enable the recycling of large quantities of nitrogen, ultimately optimizing the use of global resources and protecting the environment.
While the results are promising, the researchers still need to overcome two technical challenges before their method can be applied in real-world settings. These challenges will be the main focus of their next set of studies.
"Da una parte, our future studies will be aimed at enhancing the catalyst's structure to further improve its long-term stability, " Wang said. "In this work, the NH 3 yield rate decreased from 337.8 μg h -1 cm -2 to 140.3 μg h -1 cm -2 after 15 hours, after which it was substantially stable and maintained an NH 3 yield rate of 130.8 μg h -1 cm -2 after 40 hours. D'altra parte, we will work on the large-scale application of NH 3 electrosynthesis, developing an electric-driving flow device for the direct and continuous mass production of high-purity liquid ammonia or ammonium salt. We plan to devise a simple method for the direct purification and collection of the products, which removes the need for additional purification, transportation and other procedures."
© 2020 Scienza X Rete