
Sooyeon Hwang (seduto), Dong Su (a sinistra, in piedi, e Shuang Li al Centro per i nanomateriali funzionali di Brookhaven Lab, dove hanno usato microscopi elettronici per vedere come la struttura cristallina e la natura chimica di un elettrodo della batteria fatto di un materiale di ossido di ferro chiamato magnetite si è evoluta quando il litio è stato inserito ed estratto oltre 100 cicli di carica e scarica. Credito:Brookhaven National Laboratory
A causa della loro elevata densità di accumulo di energia, materiali come ossidi metallici, solfuri, e i fluoruri sono promettenti materiali per elettrodi per batterie agli ioni di litio nei veicoli elettrici e altre tecnologie. Però, la loro capacità svanisce molto rapidamente. Ora, gli scienziati che studiano un elettrodo fatto di un materiale di ossido di ferro economico e non tossico chiamato magnetite hanno proposto uno scenario, descritto nel numero online del 20 maggio di Comunicazioni sulla natura -questo spiega perché.
"Magnetite, tra gli altri materiali per elettrodi di conversione (cioè, materiali che vengono convertiti in prodotti completamente nuovi quando reagiscono con il litio), possono immagazzinare più energia rispetto ai materiali degli elettrodi di oggi perché possono ospitare più ioni di litio, " ha detto il capo dello studio Dong Su, leader del gruppo di microscopia elettronica presso il Center for Functional Nanomaterials (CFN), una struttura per gli utenti dell'Office of Science del Dipartimento dell'energia degli Stati Uniti (DOE) presso il Brookhaven National Laboratory. "Però, la capacità di questi materiali si degrada molto rapidamente e dipende dalla densità di corrente. Per esempio, i nostri test elettrochimici sulla magnetite hanno rivelato che la sua capacità diminuisce molto rapidamente entro i primi 10 cicli di carica e scarica ad alta velocità".
Per scoprire cosa c'è dietro questa scarsa stabilità ciclistica, gli scienziati hanno caratterizzato il modo in cui la struttura cristallina e la natura chimica della magnetite si sono evolute quando la batteria ha completato 100 cicli. Per questi studi di caratterizzazione, hanno combinato la microscopia elettronica a trasmissione (TEM) presso il CFN e la spettroscopia di assorbimento dei raggi X di sincrotrone (XAS) presso l'Advanced Photon Source (APS), una struttura per gli utenti dell'Office of Science del DOE presso l'Argonne National Lab. In TEM, un fascio di elettroni viene trasmesso attraverso un campione per produrre un'immagine o un modello di diffrazione caratteristico della struttura del materiale; XAS utilizza invece un raggio di raggi X per sondare la chimica del materiale.
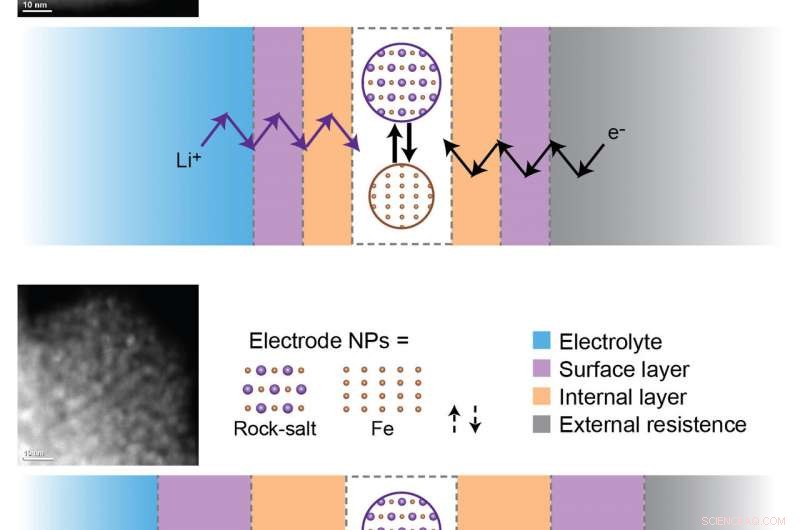
La diminuzione della capacità della batteria è dovuta alla formazione e all'ispessimento degli strati di passivazione interni e superficiali durante i cicli di carica e scarica. Affinché avvengano le reazioni elettrochimiche, gli ioni di litio (Li+) e gli elettroni (e-) devono viaggiare attraverso tutti questi strati per raggiungere le nanoparticelle attive (NP) all'elettrodo. In alto:campione di Fe3O4 (ossido di ferro) dopo tre cicli. In basso:campione Fe3O4 dopo 100 cicli. Lo sviluppo di barriere cinetiche durante i cicli a lungo termine limita le reazioni elettrochimiche in misura tale che dopo 100 cicli non si verificano reazioni di riduzione-ossidazione sui materiali degli elettrodi. Credito:Brookhaven National Laboratory
Utilizzando queste tecniche, gli scienziati hanno scoperto che la magnetite si decompone completamente in nanoparticelle di ferro metallico e ossido di litio durante la prima scarica. Nella carica successiva, questa reazione di conversione non è completamente reversibile:rimangono residui di ferro metallico e ossido di litio. Inoltre, l'originale struttura a "spinello" della magnetite evolve in una struttura a "salgemma" (la posizione degli atomi di ferro non è del tutto identica nelle due strutture) allo stato di carica. Con successivi cicli di carica e scarica, l'ossido di ferro salgemma interagisce con il litio per formare un composto di ossido di litio e nanoparticelle di ferro metallico. Poiché la reazione di conversione non è completamente reversibile, questi prodotti residui si accumulano. Gli scienziati hanno anche scoperto che l'elettrolita (il mezzo chimico che consente agli ioni di litio di fluire tra i due elettrodi) si decompone in cicli successivi.
"I nostri studi TEM in tempo reale nel vuoto ultraelevato ci hanno permesso di vedere come cambia la struttura dell'ossido di ferro salgemma quando il litio viene introdotto dopo i cicli iniziali, " ha detto Su. "Questo studio rappresenta in modo univoco la litiazione in situ di un campione preciclato. Precedenti studi in situ hanno esaminato solo i cicli di carica e scarica iniziali. Però, abbiamo bisogno di sapere cosa succede nel corso di molti cicli per progettare batterie di maggiore durata perché la struttura dell'elettrodo carico è diversa da quella dello stato originario".
Sulla base dei loro risultati, gli scienziati hanno proposto una spiegazione per la dissolvenza della capacità.
"Poiché l'ossido di litio ha una bassa conduttività elettronica, il suo accumulo crea una barriera agli elettroni che fanno la spola avanti e indietro tra l'elettrodo positivo e negativo della batteria, " ha spiegato il co-autore Sooyeon Hwang, uno scienziato del personale del CFN Electron Microscopy Group. "Chiamiamo questa barriera uno strato di passivazione interna. Allo stesso modo, la decomposizione elettrolitica ostacola la conduzione ionica formando uno strato di passivazione superficiale. Questo accumulo di ostacoli impedisce agli elettroni e agli ioni di litio di raggiungere i materiali degli elettrodi attivi, dove avvengono le reazioni elettrochimiche."
Gli scienziati hanno notato che il funzionamento della batteria a bassa corrente può recuperare parte di questa capacità rallentando la velocità di carica per fornire un tempo sufficiente per il trasporto degli elettroni; però, sono necessarie altre soluzioni per risolvere definitivamente il problema. Ritengono che l'aggiunta di altri elementi al materiale dell'elettrodo e la modifica dell'elettrolita potrebbe migliorare la diminuzione della capacità.
"La conoscenza che abbiamo acquisito può essere generalmente applicata ad altri composti di conversione, che affrontano lo stesso problema anche con strati di passivazione interni ed esterni, ", ha detto l'autore corrispondente Zhongwei Chen, un professore all'Università di Waterloo, Canada. "Speriamo che questo studio possa aiutare a guidare la futura ricerca fondamentale su questi promettenti materiali per elettrodi di conversione".