
Boccette contenenti il catalizzatore al titanio e il colorante rosso, che vengono irradiati con luce verde nel laboratorio dell'Istituto di chimica organica e biochimica di Kekulé dell'Università di Bonn. Credito:Zhenhua Zhang
Per la prima volta, i chimici dell'Università di Bonn e della Lehigh University negli Stati Uniti hanno sviluppato un catalizzatore al titanio che rende la luce utilizzabile per reazioni chimiche selettive. Fornisce un'alternativa economica e non tossica ai catalizzatori di rutenio e iridio utilizzati attualmente, che si basano su metalli molto costosi e tossici. Il nuovo catalizzatore può essere utilizzato per produrre prodotti chimici altamente selettivi che possono fornire la base per farmaci antivirali o coloranti luminescenti, Per esempio. I risultati sono stati pubblicati nell'edizione internazionale della rivista Angewandte Chemie .
Gli elettroni nelle molecole chimiche sono riluttanti a condurre una sola vita; di solito si verificano in coppia. Poi sono particolarmente stabili e non tendono a stringere nuove partnership sotto forma di nuovi legami. Però, se alcuni degli elettroni vengono portati a un livello energetico superiore con l'aiuto della luce (fotoni), le cose iniziano a sembrare diverse quando si tratta di questa "monogamia":in uno stato così eccitato, le molecole amano donare o accettare un elettrone. Questo crea i cosiddetti 'radicali, ' che hanno elettroni, sono altamente reattivi e possono essere utilizzati per formare nuovi legami.
Irradiazione con luce verde
Questo nuovo catalizzatore si basa su questo principio:il suo nucleo è il titanio, che è collegato ad un anello di carbonio in cui gli elettroni sono particolarmente mobili e possono essere facilmente eccitati. La luce verde è sufficiente per utilizzare il catalizzatore per il trasferimento di elettroni per produrre intermedi organici reattivi che altrimenti non sarebbero facilmente ottenibili. "In laboratorio, abbiamo irradiato un pallone di reazione contenente il catalizzatore di titanio che può essere visto come un "colorante rosso" con luce verde, " riferisce il Prof. Dr. Andreas Gansäuer del Kekulé Institute of Organic Chemistry and Biochemistry presso l'Università di Bonn. "E ha funzionato subito." La miscela genera radicali da molecole organiche che avviano molti cicli di reazione da cui un'ampia varietà di sostanze chimiche prodotti possono essere prodotti.
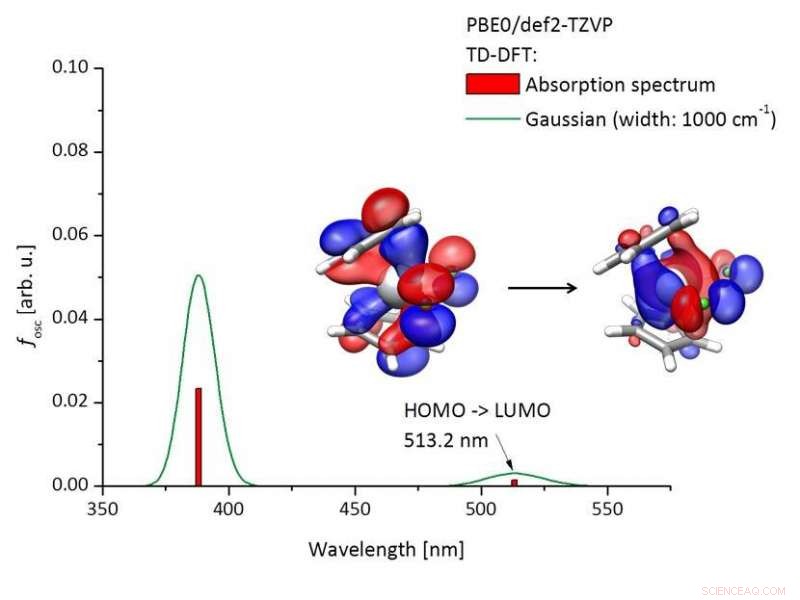
Spettro di assorbimento calcolato del Titanocendicloruro [(C5H4)2TiCl2)] e degli orbitali molecolari coinvolti nell'eccitazione. Attestazione:Tobias Hilche
Un fattore chiave nelle reazioni con questo catalizzatore fotoredox è la lunghezza d'onda della luce utilizzata per l'irradiazione. "La radiazione ultravioletta non è adatta perché è troppo ricca di energia e distruggerebbe i composti organici, " dice Gansäuer. La luce verde delle lampade a LED è sia mite che abbastanza ricca di energia da innescare la reazione.
I catalizzatori sono sostanze che aumentano la velocità delle reazioni chimiche e riducono l'energia di attivazione senza consumarsi. Ciò significa che sono disponibili continuamente e possono innescare reazioni che altrimenti non si verificherebbero in questa forma. Il catalizzatore può essere adattato ai prodotti desiderati a seconda della molecola organica con cui è legato il titanio.
Elementi costitutivi per farmaci antivirali o coloranti luminescenti
Il nuovo catalizzatore al titanio facilita le reazioni degli epossidi, un gruppo di sostanze chimiche da cui sono fatte le resine epossidiche. Questi sono usati come adesivi o per compositi. Però, gli scienziati non mirano a questo prodotto di massa, ma per la sintesi di prodotti della chimica fine molto più preziosi. "La base di titanio, catalizzatori fotoredox su misura possono ad esempio essere utilizzati per produrre elementi costitutivi per farmaci antivirali o coloranti luminescenti, " afferma Gansäuer. È fiducioso che questi nuovi catalizzatori forniscano un'alternativa economica e più sostenibile ai catalizzatori di rutenio e iridio utilizzati finora, che si basano su metalli molto costosi e tossici.
Lo sviluppo è uno sforzo collaborativo internazionale di Zhenhua Zhang, Tobias Hilche, Daniel Slak, Niels Rietdijk e Andreas Gansäuer dell'Università di Bonn e Ugochinyere N. Oloyede e Robert A. Flowers II della Lehigh University (USA). Mentre gli scienziati dell'Università di Bonn hanno studiato il modo migliore per sintetizzare i composti desiderati con il nuovo catalizzatore, i loro colleghi degli Stati Uniti hanno effettuato misurazioni per dimostrare i percorsi di reazione. "Il fenomeno della luminescenza apre davvero uno spazio interessante per considerare la progettazione di nuove reazioni sostenibili che procedano attraverso intermedi di radicali liberi, " dice il prof. Robert Flowers della Lehigh University.