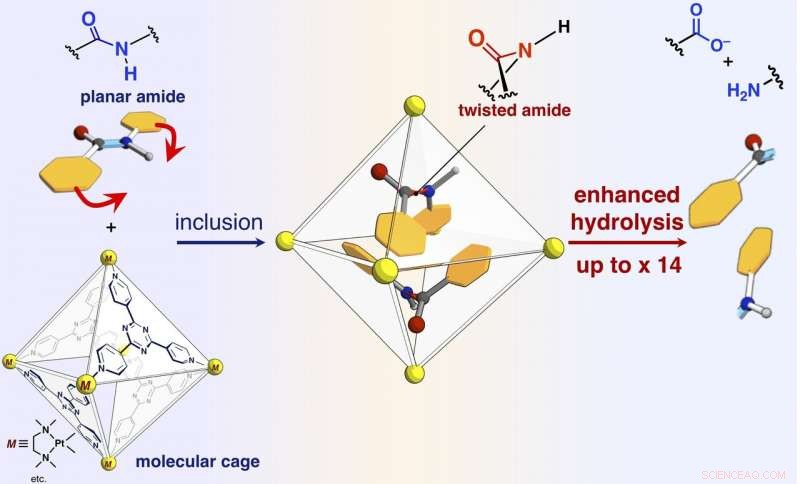
Uno schema di accelerazione della velocità di reazione dell'idrolisi dell'ammide mediante inclusione nella gabbia molecolare autoassemblata. Credito:NINS/IMS
Le proteine sono composte da amminoacidi collegati da legami ammidici. Il legame ammidico presenta un'elevata stabilità chimica e ha una struttura planare attorno al legame. Sebbene l'elevata stabilità del legame ammidico sia indispensabile per il mantenimento delle funzioni proteiche, è problematico convertire il blocco costitutivo in alcune altre specie molecolari mediante dissociazione selettiva di un legame ammidico rilevante.
Ci sono stati tentativi di controllare la reattività di un legame ammidico specifico tramite torsione selettiva mediante complicate modifiche chimiche. Alcuni composti modello con legami ammidici intrecciati sono stati prodotti mediante sintesi organica in più fasi, ed è stata dimostrata la loro elevata reattività. Si presume che l'elevata reattività di questi legami ammidici attorcigliati venga utilizzata anche in vivo. Alcune proteine sembrano essere scisse selettivamente ruotando specifici legami ammidici durante l'autolisi e lo splicing. Queste proteine, a differenza dei composti modello sintetizzati artificialmente, dovrebbero usare interazioni non covalenti per torcere i loro legami ammidici. Per molti anni, i ricercatori dell'Università di Tokyo e dell'Istituto per le scienze molecolari hanno fabbricato gabbie molecolari autoassemblate da interazioni non covalenti. Hanno applicato le loro gabbie molecolari per confinare le molecole di ammide, che possono essere considerati analoghi di piccoli pezzi di proteine, e strinse i legami ammidici pressurizzandoli all'interno della loro gabbia.
I ricercatori hanno riportato nel presente documento che i legami ammidici, che hanno strutture planari e sono inerti nello spazio libero, può essere attorcigliato, ed i composti ammidici possono essere attivati confinandoli nella loro gabbia molecolare (mostrata in figura). Quando i composti ammidici bersaglio e la gabbia molecolare vengono miscelati e riscaldati in una soluzione acquosa, la gabbia confina i composti ammidici. L'analisi della struttura a raggi X a cristallo singolo ha rivelato che due composti ammidici con strutture attorcigliate sono confinati nella gabbia. L'angolo di torsione attorno ai legami ammidici è risultato raggiungere i 34 gradi. La velocità di reazione dell'idrolisi del bersaglio attorcigliato è stata accelerata di un fattore cinque. I ricercatori sono riusciti a creare un nuovo enzima artificiale di un meccanismo precedentemente non sfruttato che confina e torce le molecole bersaglio per attivare uno specifico legame chimico.
I ricercatori sono anche riusciti ad alterare la reattività delle molecole bersaglio confinando "molecole di riempimento, "che non sono coinvolti nella reazione, insieme ai bersagli nella gabbia, controllando in tal modo con precisione il grado di torsione dei legami ammidici. Senza la molecola del ripieno, le due ammidi bersaglio sono confinate in una gabbia. Uno dei due bersagli è distorto e l'altro rimane planare. In contrasto, quando il ripieno conico viene mescolato e poi coinvolto insieme al bersaglio in una gabbia, il bersaglio rimane planare. Quando una molecola di riempimento planare è coinvolta con il bersaglio, il ripieno cambia la forma del bersaglio in una struttura attorcigliata. I ricercatori hanno studiato le velocità di reazione dell'idrolisi nei due casi e hanno scoperto che l'imbottitura planare (bersaglio attorcigliato) accelera la velocità di 14 volte, mentre l'imbottitura conica (target planare) ha accelerato la velocità di tre volte. Le molecole di riempimento consentono ai ricercatori di regolare con precisione la velocità di reazione. Questo è un risultato senza precedenti che non è mai stato trovato in studi precedenti. Questa ricerca offre un nuovo metodo per l'attivazione di molecole inerti e può essere applicato a una varietà di reazioni organiche.
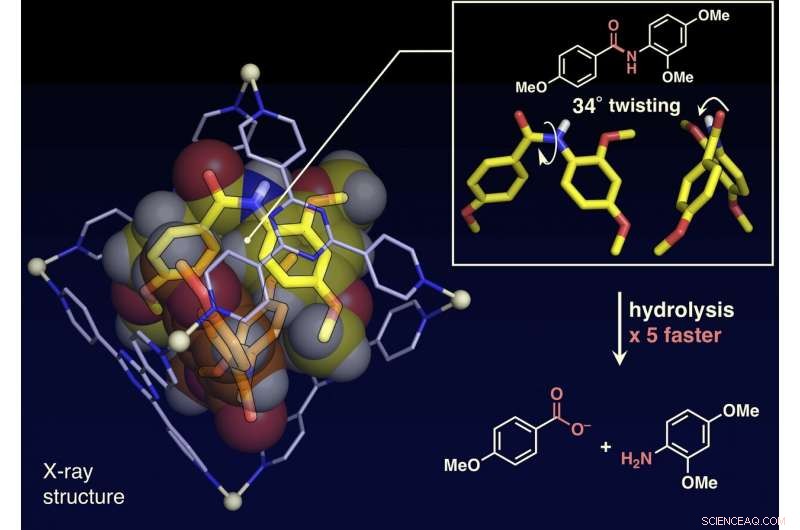
L'analisi della struttura a cristallo singolo ha mostrato che le molecole di ammide planare erano attorcigliate fino a 34 gradi all'interno della gabbia. La velocità di idrolisi di una base è stata accelerata di un fattore cinque. Credito:NINS/IMS
I ricercatori hanno dimostrato che le molecole di ammide possono essere attivate ruotando all'interno della gabbia senza complicati processi di modificazione chimica. "Stiamo cercando un nuovo tipo di gabbia in grado di attivare i bersagli con maggiore efficienza e applicarli ad altre categorie di molecole bersaglio. Con le nostre nuove gabbie, svilupperemo il nuovo metodo di attivazione delle molecole inerti. Nel futuro, le nostre gabbie saranno usate come catalizzatori, che comprimono e attivano selettivamente un legame specifico di una molecola bersaglio e anche come agenti di attivazione per profarmaci che lavorano nel corpo, " disse Fujita.
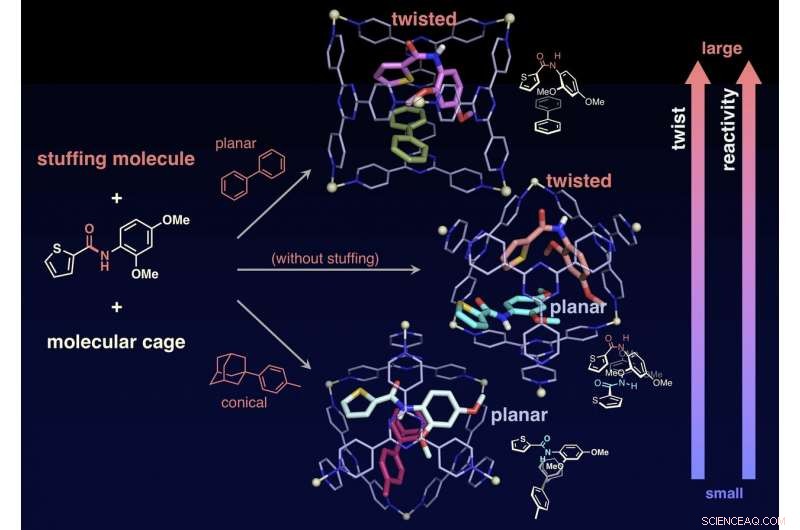
L'angolo di torsione, e poi la reattività verso l'idrolisi, può essere controllato confinando la molecola del ripieno insieme all'ammide bersaglio nella gabbia. Credito:NINS/IMS