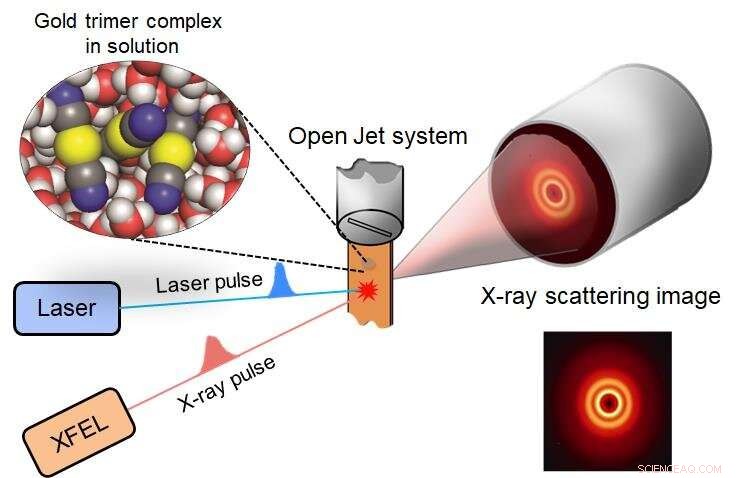
La reazione di formazione del legame in un complesso trimero d'oro è iniziata da un impulso laser, e una struttura tridimensionale dopo un certo ritardo di tempo viene rilevata da un'immagine di diffusione di raggi x. Credito:IBS
I farmaci antitumorali mirati agiscono creando uno stretto legame tra le cellule tumorali e specifici bersagli molecolari coinvolti nella crescita e nella diffusione del cancro. Immagini dettagliate di tali siti o percorsi di legame chimico possono fornire informazioni chiave necessarie per massimizzare l'efficacia dei trattamenti oncogeni. Però, i movimenti atomici in una molecola non sono mai stati catturati nel mezzo dell'azione, nemmeno per una molecola estremamente semplice come una molecola triatomica, composto da soli tre atomi.
Un gruppo di ricerca guidato da Ihee Hyotcherl dell'Institute for Basic Science (IBS, Corea del Sud) (professore, Dipartimento di Chimica, KAIST), in collaborazione con scienziati dell'Institute of Materials Structure Science di KEK (KEK IMSS, Giappone), RIKEN (Giappone) e Pohang Accelerator Laboratory (PAL, Corea del Sud), ha riportato l'osservazione diretta del momento di nascita dei legami chimici tracciando in tempo reale le posizioni atomiche nella molecola.
"Siamo finalmente riusciti a catturare il processo di reazione in corso della formazione del legame chimico nel trimero d'oro. Le immagini a risoluzione di femtosecondi hanno rivelato che tali eventi molecolari hanno avuto luogo in due fasi separate, non contemporaneamente a quanto precedentemente ipotizzato, " afferma il direttore associato Ihee Hyotcherl, il corrispondente autore dello studio. "Gli atomi nel complesso del trimero d'oro rimangono in movimento anche dopo che il legame chimico è completo. La distanza tra gli atomi aumenta e diminuisce periodicamente, esibendo la vibrazione molecolare. Queste vibrazioni molecolari visualizzate ci hanno permesso di nominare il movimento caratteristico di ciascun modo vibrazionale osservato, "aggiunge Ihee.
Gli atomi si muovono estremamente velocemente su una scala di femtosecondi (fs), quadrilionesimi di secondo. Il movimento è minuto al livello degli angstrom, pari a un decimiliardesimo di metro. Sono particolarmente sfuggenti durante lo stato di transizione in cui gli intermedi di reazione passano dai reagenti ai prodotti in un lampo. Il team di ricerca ha reso possibile questo compito sperimentalmente impegnativo utilizzando la liquidografia a raggi X a femtosecondi (scattering della soluzione).
Questa tecnica sperimentale combina la fotolisi laser e le tecniche di diffusione dei raggi X. Quando un impulso laser colpisce il campione, I raggi X si diffondono e avviano la reazione di formazione del legame chimico nel complesso del trimero d'oro. Per interrogare il processo di formazione del legame sono stati utilizzati impulsi a raggi X a femtosecondi ottenuti da una sorgente di luce speciale chiamata laser a elettroni liberi a raggi X (XFEL). Gli esperimenti sono stati eseguiti presso due strutture XFEL (acceleratore lineare di quarta generazione), PAL-XFEL in Corea del Sud e SACLA in Giappone, e questo studio è stato condotto in collaborazione con ricercatori di KEK IMSS, Laboratorio dell'acceleratore Pohang (PAL), RIKEN, e il Japan Synchrotron Radiation Research Institute (JASRI).
Le onde diffuse da ciascun atomo interferiscono tra loro e quindi le loro immagini di diffusione dei raggi X sono caratterizzate da direzioni di viaggio specifiche. Il team di ricerca dell'IBS ha tracciato le posizioni in tempo reale dei tre atomi d'oro nel tempo analizzando le immagini di dispersione dei raggi X, che sono determinati da una struttura tridimensionale di una molecola. I cambiamenti strutturali nel complesso della molecola hanno portato a molteplici immagini di dispersione caratteristiche nel tempo. Quando una molecola viene eccitata da un impulso laser, più stati quantistici vibrazionali sono simultaneamente eccitati. La sovrapposizione di diversi stati quantistici vibrazionali eccitati è chiamata pacchetto d'onda. I ricercatori hanno tracciato il pacchetto d'onda in coordinate nucleari tridimensionali e hanno scoperto che il primo mezzo giro di legame chimico si è formato entro 35 fs dopo la fotoeccitazione. La seconda metà della reazione è seguita entro 360 fs per completare l'intera dinamica di reazione.
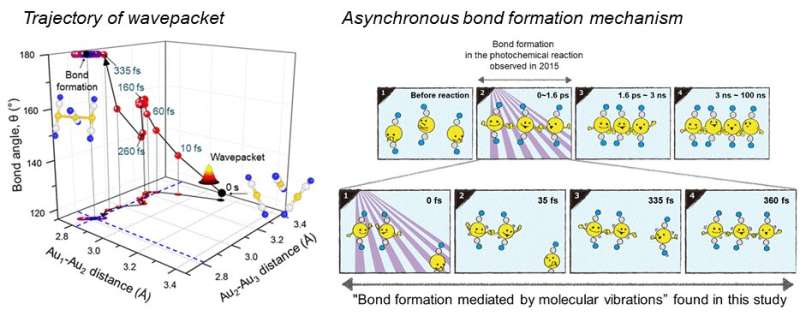
(a sinistra) Le posizioni dipendenti dal tempo del pacchetto d'onda nelle coordinate nucleari multidimensionali sono state ottenute dall'esperimento di diffusione di raggi X a femtosecondi su un complesso di trimero d'oro. (Credit:Nature &IBS) (a destra) Ispezionando il movimento del pacchetto d'onde, è stato rivelato che la reazione di formazione del legame nel complesso del trimero d'oro avviene attraverso un meccanismo di formazione del legame asincrono. (Giallo:atomi d'oro, grigio:atomo di carbonio, blu:atomo di azoto, 1000 volte 1 fs è 1 picosecondo (ps), 1000 volte 1 ps è 1 nanosecondo (ns)) Credito:(a sinistra) Natura e IBS, (a destra) KEK IMSS
I ricercatori hanno anche illustrato accuratamente i movimenti delle vibrazioni molecolari sia temporalmente che spazialmente. Questa è un'impresa piuttosto notevole considerando che una velocità così ultraveloce e una lunghezza minima di movimento sono condizioni molto impegnative per l'acquisizione di dati sperimentali precisi.
In questo studio, il team di ricerca IBS ha migliorato lo studio del 2015 pubblicato da Natura . Nello studio precedente del 2015, la velocità della telecamera a raggi X (risoluzione temporale) era limitata a 500 fs, e la struttura molecolare era già cambiata per essere lineare con due legami chimici entro 500 fs. (Figura 2, in alto a destra) In questo studio, l'andamento della formazione del legame e della trasformazione strutturale da curva a lineare potrebbe essere osservato in tempo reale, grazie al miglioramento dei tempi di risoluzione fino a 100 fs. In tal modo, il meccanismo di formazione del legame asincrono in cui si formano due legami chimici in 35 fs e 360 fs, rispettivamente, e sono state visualizzate la trasformazione piegata-lineare completata in 335 fs (Figura 2, in basso a destra). In breve, oltre a osservare l'inizio e la fine delle reazioni chimiche, hanno riportato ogni passaggio dell'intermedio, riarrangiamento in corso delle configurazioni nucleari con metodi sperimentali e analitici notevolmente migliorati.
Il team di ricerca promuoverà questo metodo di "monitoraggio in tempo reale delle posizioni atomiche in una molecola e della vibrazione molecolare utilizzando la diffusione di raggi X a femtosecondi" per rivelare i meccanismi delle reazioni catalitiche organiche e inorganiche e delle reazioni che coinvolgono le proteine nel corpo umano. "Tracciando direttamente le vibrazioni molecolari e le posizioni in tempo reale di tutti gli atomi in una molecola nel mezzo della reazione, saremo in grado di scoprire i meccanismi di varie reazioni catalitiche organiche e inorganiche sconosciute e reazioni biochimiche, " dice il dottor KIM Jong Goo, il primo autore dello studio.
Lo studio è pubblicato su Natura .