
Micrografia elettronica dell'impalcatura "vuota" (senza idrogel) che un team di ricerca internazionale ha utilizzato per deformare le singole cellule. Credito:Marc Hippler, KIT
Il comportamento delle cellule è controllato dal loro ambiente. Oltre a fattori biologici o sostanze chimiche, sono coinvolte anche forze fisiche come pressione o tensione. I ricercatori del Karlsruhe Institute of Technology (KIT) e dell'Università di Heidelberg hanno sviluppato un metodo che consente loro di analizzare l'influenza delle forze esterne sulle singole cellule. Utilizzando un processo di stampa 3D, hanno prodotto micro-impalcature, ognuno dei quali ha quattro pilastri su cui si trova una cella. Attivato da un segnale esterno, un idrogel all'interno dell'impalcatura si gonfia e allontana i pilastri, in modo che la cellula debba "allungarsi". L'opera fa parte del Cluster di Eccellenza "3-D Matter Made to Order" (3DMM2O). I ricercatori riferiscono sui loro risultati in Progressi scientifici .
Molti processi biologici cellulari, come la guarigione delle ferite o lo sviluppo di tessuti, sono fortemente influenzati dalle proprietà del loro ambiente. Le cellule reagiscono, Per esempio, a fattori biologici o sostanze chimiche. Però, la ricerca si sta sempre più concentrando sulle forze fisiche che agiscono sulle cellule:come si adattano esattamente le cellule a queste forze?
Nell'ambito del consorzio universitario tedesco-giapponese HeKKSaGOn e in collaborazione con scienziati australiani, il team di 3DMM2O ha adottato un approccio particolarmente ingegnoso a questa domanda. Per la produzione delle loro celle "rastrelliere" hanno usato "scrittura laser diretta, " uno speciale processo di stampa 3D in cui un raggio laser controllato da computer viene focalizzato in uno speciale inchiostro liquido per stampante. Le sue molecole reagiscono solo nelle aree esposte e lì formano un materiale solido. Tutte le altre aree rimangono liquide e possono essere lavate via "Questo è un metodo consolidato nel nostro Cluster of Excellence per la costruzione di strutture tridimensionali, su scala micrometrica e inferiore, " spiega Marc Hippler del KIT Institute of Applied Physics, autore principale della pubblicazione.
Nel caso attuale, i ricercatori hanno utilizzato tre diversi inchiostri per stampanti:il primo inchiostro, realizzato in materiale repellente alle proteine, è stato utilizzato per formare il vero e proprio micro-scaffold. Usando un secondo inchiostro di materiale che attrae le proteine, hanno quindi prodotto quattro barre orizzontali che sono collegate ciascuna a uno dei pilastri dell'impalcatura. La cella è ancorata a queste quattro barre. Il vero spettacolo, però, è il terzo inchiostro:gli scienziati lo hanno usato per "stampare" una massa all'interno dell'impalcatura. Se poi aggiungono un liquido speciale, l'idrogel si gonfia. Sviluppa così una forza sufficiente a muovere i pilastri, e con essi le sbarre. Questo, a sua volta, ha l'effetto di allungare la cella che è fissata alle sbarre.
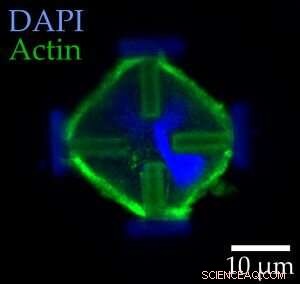
Immagini al microscopio ottico di cellule embrionali di topo colorate nel loro stato normale (a sinistra) e allungato (a destra). Le frecce rosse indicano le forze che agiscono sulle cellule. Credito:Marc Hippler
Le cellule contrastano la deformazione
Gli scienziati del Cluster of Excellence hanno posizionato due tipi di cellule completamente diversi sul loro rack per lo stretching:cellule tumorali ossee umane e cellule embrionali di topo. Hanno scoperto che le cellule contrastano le forze esterne con proteine motorie e quindi aumentano notevolmente le loro forze di trazione. Quando la forza di stiramento esterna viene rimossa, le cellule si rilassano e ritornano al loro stato originale. "Questo comportamento è un'impressionante dimostrazione della capacità di adattarsi a un ambiente dinamico. Se le cellule non fossero in grado di riprendersi, non avrebbero più adempiuto alla loro funzione originale, ad esempio chiusura della ferita, " afferma il professor Martin Bastmeyer dell'Istituto zoologico di KIT.
Come il team ha ulteriormente scoperto, una proteina chiamata NM2A (miosina 2A non muscolare) svolge un ruolo decisivo nella risposta delle cellule alla stimolazione meccanica:le cellule tumorali ossee geneticamente modificate che non sono in grado di produrre NM2A sono state a malapena in grado di contrastare la deformazione esterna.
Il lavoro nel cluster di eccellenza è stato svolto da scienziati di Heidelberg del campo della chimica biofisica, della fisica e della neurobiologia cellulare e del KIT. I membri del consorzio universitario tedesco-giapponese HeKKSaGOn includono, tra gli altri, Università di Heidelberg, Istituto di tecnologia di Karlsruhe e Università di Osaka.