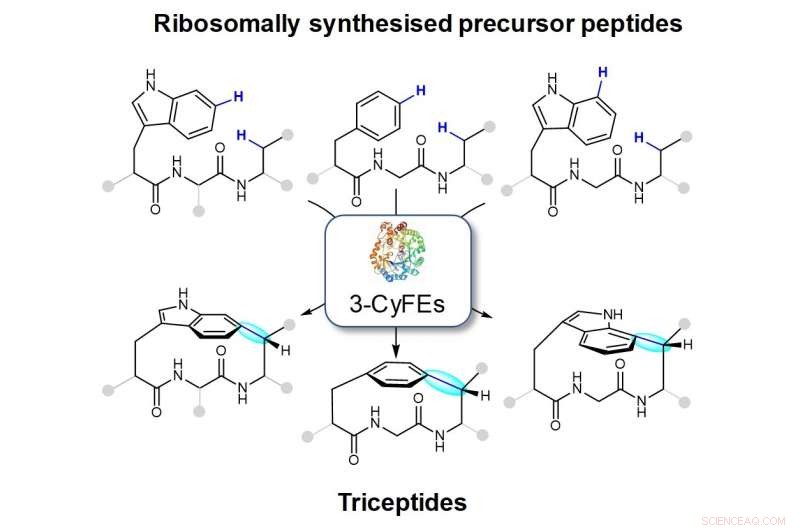
La figura mostra i macrocicli creati dagli enzimi che formano il ciclofano a tre residui (3-CyFE). Il nuovo legame è mostrato in blu ed evidenziato in ciano. La famiglia di prodotti naturali prodotti dai 3-CyFE è indicata come triciptidi.
I ricercatori del NUS hanno identificato enzimi modificanti post-traduzionali nei batteri che possono creare una nuova famiglia di peptidi ciclici per nuove terapie.
I peptidi ciclici sono una classe ben nota di molecole che possiedono una gamma di attività biologiche tra cui antibatterica, proprietà immunosoppressive e antitumorali. La sfida alla creazione di nuovi tipi di peptidi ciclici risiede nella scoperta di nuove reazioni catalitiche mediante sintesi chimica o utilizzando enzimi. Una strategia per raggiungere questo obiettivo prevede la formazione di legami carbonio-carbonio (C-C). Però, Le reazioni di formazione del legame C-C ai legami carbonio-idrogeno (C-H) inattivati sono difficili perché queste posizioni sono inerti, e la selettività non è facile da controllare. Il superamento di queste barriere consentirà la creazione di una nuova gamma di peptidi ciclici in modo efficiente e prevedibile.
Il team di ricerca guidato dal Prof Brandon Morinaka del Dipartimento di Farmacia, NUS ha trovato reazioni catalizzate da una serie di enzimi modificanti post-traduzionali di vari batteri che possono essere potenzialmente utilizzati per sviluppare importanti molecole di farmaci. Questi enzimi possono catalizzare la formazione di un C(aril)-C( sp 3 ) legame tra le catene laterali di due amminoacidi. Questa disposizione molecolare è la caratteristica distintiva di una classe di prodotti naturali denominati triciptidi (tre residui nei peptidi ciclofanici) (vedi figura). La reazione di chiusura dell'anello porta alla formazione di ciclofani peptidici tesi. Sebbene questi enzimi siano codificati in diverse centinaia di genomi batterici, la loro funzione e i loro prodotti finali sono rimasti in gran parte sconosciuti.
Questi enzimi offrono una nuova strategia per la modifica dei peptidi e possono essere applicati per generare peptidi terapeutici che mostrano un legame unico con bersagli molecolari. La ciclizzazione dei peptidi è una strategia generale utilizzata in natura e nella chimica di sintesi per prevenire la degradazione da parte degli enzimi digestivi. La prevenzione della degradazione è un attributo essenziale necessario affinché i farmaci raggiungano il loro obiettivo e rappresenta un ostacolo all'utilizzo dei peptidi come farmaci.
Questi enzimi sono in grado di installare gli anelli in una varietà di modelli con diversi amminoacidi. Ciò significa che l'ampiezza dei prodotti è potenzialmente ampia e può essere applicata a diversi obiettivi nella scoperta di farmaci. È stato scoperto che diversi batteri provenienti da una vasta gamma di microbiomi codificano per gli enzimi che formano il ciclofano. La diversità dei prodotti suggerisce che i ciclofani peptidici sono più diffusi di quanto precedentemente noto e possono conferire un uso o una funzione generale a questa classe di prodotti naturali.
Il team prevede di produrre ulteriori prodotti naturali a base di triciptidi e di comprendere il meccanismo enzimatico. I loro obiettivi a lungo termine sono generare una gamma diversificata di prodotti peptidici ciclofanici che possono essere utilizzati come punto di partenza per individuare malattie di interesse.
Il professor Morinaka ha detto, "Gli enzimi che formano il ciclofano post-traduzionali offrono un nuovo metodo per creare diversi peptidi ciclici che offrono nuove opportunità nell'ingegneria dei peptidi e nella scoperta di farmaci".