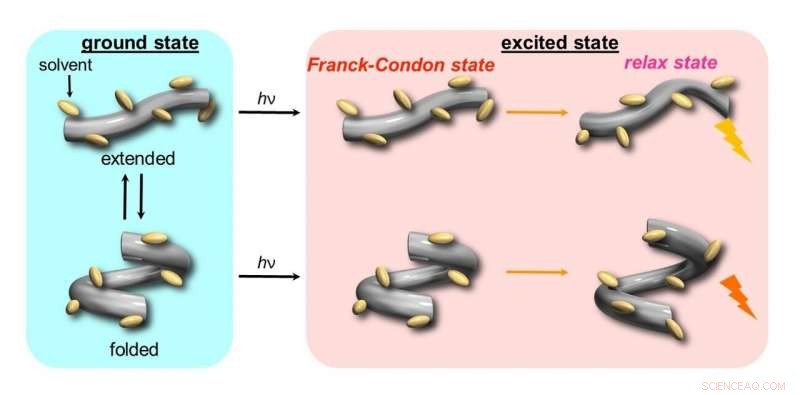
Nello stato fondamentale, l'ospite adotta due conformeri, uno esteso e uno piegato, e si sposta gradualmente verso uno "stato di ricchezza estesa" dopo la pressurizzazione. Quindi, allo stato eccitato (hυ), questi due conformeri emettono fluorescenza diversa. Credito:Scienze chimiche
Strutture supramolecolari sensibili allo stimolo sono emerse come alternativa a quelle convenzionali, a causa delle loro applicazioni nel rilevamento, consegna farmaci, e sistemi di memoria commutabili. Ora, gli scienziati del Tokyo Institute of Technology esplorano la risposta alla pressione idrostatica dei "foldameri", molecole artificiali che imitano il ripiegamento delle proteine, e segnalano un cambiamento nella loro conformazione preferita con il cambiamento della pressione, dimostrando il controllo dinamico abilitato dalla pressione idrostatica. La scoperta apre le porte allo sviluppo futuro di pieghevoli sensibili alla pressione e materiali artificiali.
Maggior parte, se non tutto, i sistemi biologici sono estremamente complessi e spesso si basano su interazioni su cui la chimica tradizionale non si concentra. Un intero campo di ricerca chiamato chimica supramolecolare è stato ispirato per studiare esattamente quelle interazioni che governano i processi biologici, basato su un approccio basato su macchine molecolari artificiali per imitare funzioni biologiche. Queste macchine molecolari rispondono a un'ampia gamma di stimoli esterni, come la temperatura, mezzi di comunicazione circostanti, eccitazione con la luce, e di conseguenza trovano applicazioni nel rilevamento, consegna farmaci, imaging molecolare, e tecnologia di memoria commutabile.
Però, uno stimolo particolare, vale a dire, pressione idrostatica - è stato a lungo di moda per il fatto notevole che consente di studiare un materiale supramolecolare sia nel suo stato imperturbato che in pressione. Infatti, un gruppo di ricerca con sede in Giappone, composto da scienziati del Tokyo Institute of Technology (Tokyo Tech), hanno recentemente dimostrato che le proprietà ottiche ei processi chimici in soluzioni di materiali supramolecolari possono essere regolati con precisione dalla pressione idrostatica.
Ispirato dalle loro scoperte, il gruppo, guidato dal Prof. Gaku Fukuhara della Tokyo Tech e dal Prof. Hiromitsu Maeda della Ritsumeikan University, è passato allo studio degli effetti della pressione sui "foldameri", molecole artificiali che imitano le proteine. I loro risultati sono stati pubblicati sulla rivista Scienze chimiche . Il nome foldamer deriva dal fatto che questi sistemi possono replicare proteine ripiegandosi in schemi ben definiti. Il prof. Gaku Fukuhara spiega la motivazione del loro studio:"Il comportamento allo stato di soluzione dei foldameri sotto pressione idrostatica non è stato esaminato in dettaglio, che rappresenta una sfida per ulteriori progressi nella chimica supramolecolare".
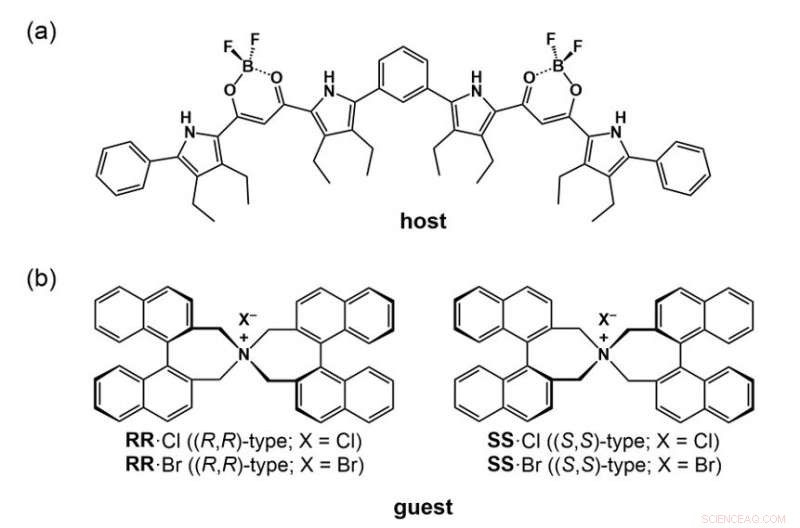
Gli scienziati hanno scelto un foldamer fluorescente di un recettore di ioni negativi, chiamato "ospite", e coppie di ioni chirali contenenti cloruro e bromuro come "ospiti" per esplorare le proprietà ottiche della soluzione ospite sotto pressione idrostatica. Credito:Scienze chimiche
Affinché un foldamer si pieghi in una conformazione specifica, deve prima legarsi a uno ione ospite caricato negativamente che forma lo stato racemico (uguale quantità) delle strutture elicoidali. La chiralità (o la proprietà di essere distinta dalla sua immagine speculare) della struttura risultante può quindi essere indotta introducendo uno ione contro positivo asimmetrico, un processo noto come accoppiamento ionico. L'accoppiamento ionico, però, dipende dalle condizioni di solvatazione per il foldamer, quale, a sua volta, può essere influenzato dalla pressione idrostatica. Di conseguenza, gli scienziati hanno scelto un foldamer fluorescente come recettore di ioni negativi, chiamato un ospite, e coppie di ioni chirali (come cloruro e bromuro) come ospiti per esplorare le proprietà ottiche della soluzione ospite sotto pressione idrostatica.
Gli scienziati hanno iniziato esaminando i cambiamenti negli spettri di fluorescenza e assorbimento (negli UV e nel visibile) per l'ospite in vari solventi organici sotto pressione e hanno osservato uno spostamento graduale della banda spettrale a lunghezze d'onda più lunghe, nonché un aumento dell'assorbanza con l'aumento della pressione. Lo hanno attribuito al fatto che l'ospite adotta inizialmente due conformeri, uno esteso e uno piegato, e si sposta gradualmente a uno stato di ricchezza estesa dopo la pressurizzazione. Quindi, dopo eccitazione elettronica (hυ), da questi conformeri sono stati osservati due diversi stati di fluorescenza.
"Il nostro studio mostra chiaramente che le conformazioni nell'host flessibile foldamer possono essere controllate dinamicamente, sia nello stato fondamentale che in quello eccitato, semplicemente modificando la pressione idrostatica, " commenta entusiasta il Prof. Fukuhara. "Infatti, questa strategia può essere estesa anche ad altre combinazioni foldamer e guest che hanno difficoltà a rilevarsi a vicenda o non mostrano una chimica host-guest, " Aggiunge.
Gli sforzi del team per decifrare meglio i foldameri ci portano sicuramente un passo più vicino alla comprensione della complessità delle proteine.