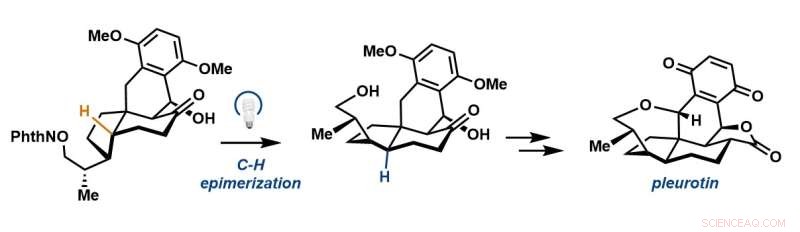
Un'epimerizzazione radicale fotoredox genera lo scheletro tetraciclico della pleurotina. Credito:The Sorensen Lab
Dal punto di vista dei chimici, la pleurotina è una molecola intrigante.
Vi sono forti prove di proprietà terapeutiche non sfruttate come inibitore del tumore e antibiotico. Ha un'affascinante struttura complessa (sei anelli! otto stereocentri!). Ed è stato difficile da sintetizzare nel corso dei decenni. L'ultima volta che i chimici sono riusciti a farlo, era l'anno 1988 e avevano bisogno di 26 passaggi per farlo.
Per il Sorensen Lab di Princeton Chemistry, queste qualità erano parte dell'attrazione per un investimento a lungo termine di tempo ed energia che si è concretizzato.
Il laboratorio riporta una sintesi concisa della pleurotina attraverso la reazione di Diels-Alder e un'epimerizzazione radicale che trasforma un cis-idrindano nel desiderato trans-idrindano. Il loro intermedio avanzato interseca la sintesi fondamentale del 1988 verso la fine del processo, riducendo così di tredici il numero totale di passaggi necessari per la sintesi.
Il processo del laboratorio potrebbe produrre una famiglia allargata di candidati allo screening antitumorale simile alla pleurotina che, in futuro, potrebbero essere utili per le aziende farmaceutiche che cercano di sfruttare la promessa della pleurotina come farmaco di prossima generazione.
"La pleurotina è una molecola molto sensibile, è molto reattiva. Ma non ha ancora funzionato come farmaco, in parte perché non è molto solubile in acqua", ha detto lo studente del terzo anno John Hoskin, autore principale dell'articolo. "Idealmente vuoi modificarne la struttura:modifica qui, cambia qui, metti un idrossi qui o un fosfato là, apporta delle modifiche molto attente."
"E poiché non puoi davvero farlo a partire dalla pleurotina stessa, il nostro approccio sarà quello di incorporare i cambiamenti da una sintesi dal basso, il che è possibile solo a causa della brevità del percorso. Quindi ti ritroverai con i cosiddetti analoghi che sono molto simili a questo prodotto naturale ma che hanno questi cambiamenti strategici."
"A Concise Synthesis of Pleurotin Enabled by a Nontraditional CH Epimerization" è stato pubblicato il mese scorso nel Journal of the American Chemical Society di Hoskin e P.I. Erik Sorensen, Arthur Allan Patchett Professore di Chimica Organica presso il Dipartimento di Chimica.
"Quando un chimico osserva una struttura come questa, non ci sono strategie ovvie che si dovrebbero adottare per crearla da composti semplici", ha detto Sorensen. Il suo laboratorio ha iniziato a lavorare sulla pleurotina nel 2008 solo per incontrare una serie di delusioni. Fino ad ora.
"Se prendi la pleurotina e dici, voglio fare una chimica sito-selettiva alla sua periferia in modo da poter costruire nuove molecole con proprietà migliorate, allora forse ci saranno agenti antitumorali migliori", ha aggiunto. "Quindi John ed io siamo stati attratti dalla sfida di sviluppare un approccio chimico per costruire quella struttura nel minor numero di passaggi possibile."
"Otto passaggi sono un numero piuttosto piccolo di passaggi per una molecola di quella complessità", ha affermato Sorensen. "Questa ricerca testimonia l'abilità di John come progettista ed esecutore di sintesi organica."
Promessa non sfruttata dal 1947
La pleurotina deriva dal fungo Pleurotus griseus. I ricercatori hanno descritto per la prima volta la molecola in un articolo pubblicato nel 1947 come inibente la crescita dello Staphylococcus aureus, la fonte delle infezioni da stafilococco. Erano passati 41 anni dalla sintesi fondamentale della pleurotina da parte di David Hart, ora professore emerito alla Ohio State University.
Ma a causa dell'incapacità di sintetizzarlo facilmente, la pleurotina non è stata studiata al massimo delle sue potenzialità. Fu allora che intervenne il Sorensen Lab.
Per ridurre i passaggi verso la sintesi, i ricercatori hanno utilizzato una tattica collaudata nella sintesi organica chiamata trasferimento di atomi di idrogeno 1,5, in cui un radicale reattivo centrato sull'ossigeno essenzialmente "raggiunge" e strappa un idrogeno da un carbonio che fa parte della struttura della pleurotina per creare un nuovo radicale. I ricercatori hanno quindi utilizzato quel radicale per ricevere idrogeno da un tiolo esogeno che consentirebbe allo stereocentro di passare a una configurazione alternativa o trans.
"Abbiamo provato molte strategie diverse e alla fine ciò che ha funzionato è stato questo passaggio di inversione per passare da questo cis-idrindano al trans-idrindano. Questa è l'intuizione chiave", ha affermato Hoskin. "Utilizzando la funzionalità inerente alla molecola - questo ossigeno - potremmo, come se stessimo usando un paio di pinzette microscopiche, strappare questo idrogeno e capovolgere quel carbonio per ottenere il trans-idrindano necessario".
Il processo genera un prodotto finale racemico, realizzando sia la versione sinistra che quella destra in proporzioni uguali. È probabile che solo uno di loro sia bioattivo. Ora che la sintesi formale è stata completata in modo più conciso, ha affermato Hoskin, la prossima sfida sarà produrre solo una versione speculare della molecola e dei suoi analoghi.
"Questa ricerca mostra il potere di una breve sintesi", ha detto Hoskin. "Ci vuole solo una settimana per completare l'intero percorso."
Sorensen ha aggiunto:"Penso che questo lavoro ci metta in una posizione favorevole verso il nostro obiettivo più ampio di espandere la classe degli agenti antitumorali a base di pleurotina". + Esplora ulteriormente