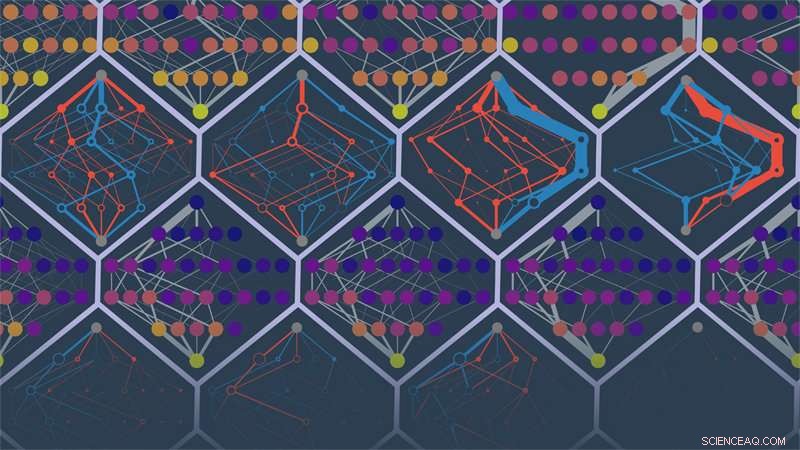
I ricercatori del laboratorio dell'Università dell'Oregon di Michael Harms hanno previsto i percorsi evolutivi di diverse proteine simulate. I punti nell'immagine sono sequenze proteiche. I bordi indicano le probabilità delle traiettorie. I colori indicano una forma fisica da bassa ad alta (dal viola al giallo) o percorsi falsamente inaccessibili o falsamente accessibili (rosso e blu). Credito:Michael Harms e Zach Sailer
Gli scienziati dell'Università dell'Oregon hanno teorizzato di poter manipolare una proteina una mutazione alla volta e prevederne l'evoluzione. Hanno cercato di dimostrarlo. E fallito.
pensano, però, che hanno trovato una verità fondamentale alla base dell'imprevedibilità in un sistema biologico. Le limitazioni fisiche di base rendono l'incertezza la norma, hanno riportato in un articolo pubblicato online il 23 ottobre su Atti dell'Accademia Nazionale delle Scienze .
"Mentre abbiamo ottenuto un sorprendente risultato negativo, siamo stati in grado di dire perché, " ha detto Michael J. Harms, professore presso il Dipartimento di Chimica e Biochimica dell'UO e scienziato presso l'Istituto di Biologia Molecolare. "Questo è positivo. Il nostro semplice studio fornisce conferma di ciò che molte persone nel campo hanno osservato ripetutamente:l'imprevedibilità. Sembra che sia universale".
La ricerca era un affare digitale, realizzato con simulazioni al computer progettate dal dottorando dell'UO Zachary R. Sailer. Lui e Harms hanno creato una semplice proteina reticolare, utilizzando un approccio precedentemente creato nel laboratorio Harms, con una sequenza casuale di 12 amminoacidi. Hanno quindi eseguito simulazioni evolutive per ottimizzare la stabilità, una proprietà fisica della proteina.
L'obiettivo era utilizzare gli effetti di tutte le 228 mutazioni note per essere associate alla proteina di partenza per prevedere queste traiettorie simulate:quale mutazione si sarebbe verificata, quando, col tempo. La capacità di proiettarsi in avanti è svanita rapidamente dopo le prime due mutazioni. Dopo di che, le traiettorie previste si sono smarrite in mezzo a un numero crescente di probabilità di reindirizzamento.
"La qualità delle tue informazioni in realtà decade nel tempo, " Sailer ha detto. "Mentre le mutazioni si accumulano, gli effetti delle mutazioni che hai misurato iniziano a cambiare in modo che tu non possa prevedere dove stai andando".
Nella loro carta, Sailer e Harms suggeriscono che la fisica, in particolare termodinamica, è in gioco. Ogni mutazione altera la proteina in un piccolo, ma in modo non lineare. Ciò significa che l'effetto di ogni mutazione dipende da tutte le mutazioni che si sono verificate prima.
"Penso che quello che abbiamo mostrato, fondamentalmente, è che anche se sai molto su un sistema, su una proteina, non puoi prevedere come si evolve a causa della fisica del sistema, "Ha detto Harms. "Ci sono regole fisiche che limitano l'evoluzione e la sua prevedibilità".
Come si evolvono le proteine è una questione fondamentale nella biologia evolutiva, sia dal punto di vista filosofico, per saperne di più sui macchinari dei sistemi biologici, e per indizi che potrebbero portare a farmaci migliorati o migliori.
"In pratica, "Danni ha detto, "la nostra ricerca può aiutarci a imparare come prevenire l'evoluzione della resistenza agli antibiotici nei batteri". Quasi tutte le infezioni trasmesse da batteri stanno sviluppando resistenza agli antibiotici, creando una delle principali preoccupazioni per la salute pubblica in tutto il mondo.
"Piuttosto che studiare gli effetti di tutte le mutazioni individuali, "Il marinaio ha aggiunto, "forse dovremmo studiare combinazioni casuali di molte mutazioni. Un tale approccio potrebbe aiutarci a prevedere l'evoluzione della resistenza".
Nel laboratorio Harms sono in corso lavori per testare questa possibilità su proteine reali. "Stiamo costruendo strumenti computazionali che ci consentono di analizzare set di dati sulla resistenza agli antibiotici, e stiamo ricevendo suggerimenti sul fatto che un approccio combinatorio funziona, "Ha detto Harms. "È più complicato che studiare le singole mutazioni, ma il nostro lavoro mostra che è improbabile che l'approccio individuale funzioni".