Credito:ACS
Per la prima volta, un chimico dell'Università del Michigan ha utilizzato l'entanglement quantistico per esaminare le strutture proteiche, un processo che richiede solo un numero molto piccolo di fotoni di luce.
Tradizionalmente, gli scienziati hanno utilizzato potenti microscopi a scansione laser per studiare le proteine su scala molecolare. Ma i laser tradizionali presentano due problemi. Primo, l'intensità del laser può danneggiare il campione esaminato. Secondo, il laser fa esplodere il campione con fotoni, che poi si disperdono lontano dal bersaglio.
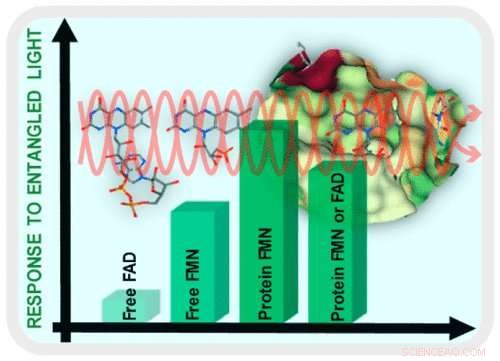
Anziché, Theodore Goodson, professore di chimica della UM, e il metodo del suo team di utilizzare l'entanglement quantistico utilizza solo un piccolo numero di fotoni per conoscere le molecole. In questo caso, il team ha studiato i flavini, un gruppo di enzimi fondamentali per il metabolismo energetico nel corpo.
L'entanglement quantistico è l'idea che le proprietà di una coppia o di un gruppo di particelle dipendono l'una dall'altra, anche se le particelle sono separate da grandi distanze. Per esempio, se una particella ruota in senso orario, l'altro nella sua coppia girerà al contrario, se sono impigliati. Questa relazione persiste anche se le particelle sono a migliaia di chilometri di distanza, Goodson ha detto.
"Si scopre che se hai fotoni che sono entangled, quell'alto grado di correlazione può interagire con le molecole delle proteine in un modo diverso rispetto a se non sono entangled, " ha detto Goodson. "Siamo in grado di sondare le proprietà delle proteine con un numero estremamente piccolo di fotoni".
I fotoni entangled vengono prodotti inviando luce laser attraverso un cristallo non più grande della punta di un'unghia. Quando la luce attraversa il cristallo in un certo modo, alcuni dei fotoni diventano entangled. Queste coppie entangled vengono quindi utilizzate per esaminare le molecole bersaglio.
Questi fotoni eccitano stati elettronici nella proteina. In base alla radiazione elettromagnetica che la molecola emette quando viene eccitata dai fotoni, Goodson può determinare proprietà specifiche sulla molecola, un metodo chiamato spettroscopia.
Il numero di fotoni necessari per la spettroscopia di fotoni entangled è straordinariamente basso rispetto ai metodi spettroscopici laser tradizionali.
"Riesci a immaginare di fare un'indagine in cui puoi usare 10 ordini di grandezza in meno di fotoni per sondare la caratteristica particolare di un materiale, campione biologico, o una quantità molto piccola di una sostanza chimica su una superficie?" ha detto Goodson.
Usando questo metodo, Goodson e il suo team sono stati in grado di vedere una nuova interazione all'interno di una proteina flavina. Guardando le flavoproteine, il team è stato in grado di vedere le differenze nella loro spettroscopia utilizzando l'entanglement quantistico rispetto all'utilizzo della luce classica.
Il metodo apre nuove strade per la microscopia a immagini, Goodson ha detto. Guardare i fotoni entangled interagire con le molecole nelle proteine può insegnare agli scienziati qualcosa di nuovo sugli stati elettronici di queste molecole.
"Per esempio, nella fotosintesi, quando i fotoni forniscono energia per il centro di reazione fotosintetica, il meccanismo di questo effetto potrebbe essere potenziato utilizzando la luce quantistica, " ha detto. "Con un processo di eccitazione del fotone entangled, potrebbe essere possibile ottimizzare e potenziare i processi di trasferimento di energia nei sistemi biologici. Ciò potrebbe portare a nuove informazioni sui processi chimici e biologici in questi complessi biologici naturali".
Prossimo, il gruppo spera di studiare le proprietà delle molecole organiche e biologiche utilizzando fotoni entangled in un microscopio. I coautori dello studio includono Juan Villabona-Monsalve e Oleg Varnavski del Dipartimento di Chimica dell'U-M e Bruce Palfey del Dipartimento di Chimica Biologica dell'U-M.