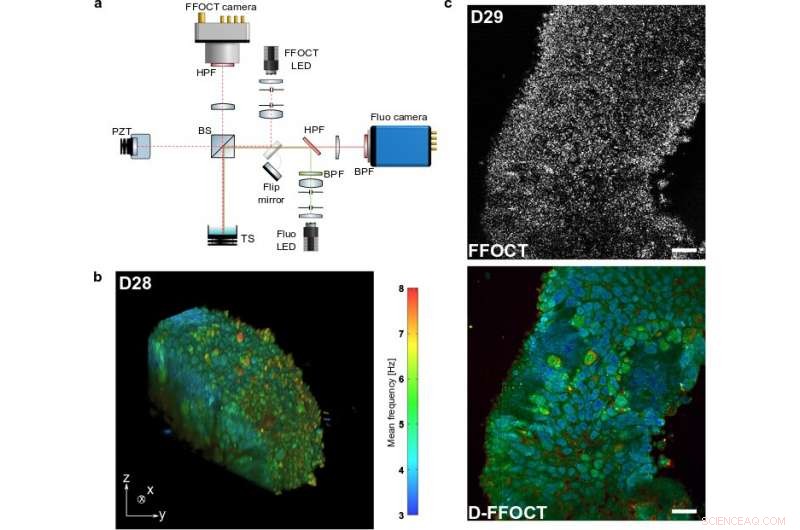
un, Configurazione per creare immagini FFOCT e D-FFOCT, combinato con fluorescenza per la convalida. B, Rappresentazione 3D di una porzione di un organoide retinico di 28 giorni (D28) derivato da hiPSC catturato con D-FFOCT, con la barra dei colori corrispondente. C, Confronto delle immagini FFOCT e D-FFOCT di un organoide retinico D29:l'immagine FFOCT mostra la struttura globale del campione, considerando che l'immagine D-FFOCT rivela le diverse cellule che costituiscono il campione, con un contrasto molto più alto. Barra di scala:20 μm. Credito:Jules Scholler, Cassandra Groux, Olivier Goureau, José Alain Sahel, Mathias Fink, Sacha Reichmann, Claude Boccara e Kate Grieve
La tomografia a coerenza ottica offre straordinarie opportunità per visualizzare la complessa struttura del tessuto vivente, ma manca di informazioni funzionali. Vi presentiamo la tomografia a coerenza ottica dinamica a pieno campo come tecnica per visualizzare in modo non invasivo gli organoidi retinici derivati da cellule staminali pluripotenti indotte umane viventi (hiPSC). Vengono generate immagini colorate con un contrasto endogeno legato alla motilità degli organelli, con risoluzione spaziale submicrometrica e risoluzione temporale in millisecondi, creando un modo per identificare specifici tipi di cellule nel tessuto vivente attraverso il loro profilo dinamico.
Le attuali modalità per l'imaging di tessuti viventi e colture cellulari 3D sono invasive, lento o privo di risoluzione spaziale. La tomografia a coerenza ottica dinamica a tutto campo (D-FFOCT) è un non invasivo, tecnica quantitativa che unisce elevate risoluzioni spaziali e temporali. Questa tecnica si basa sull'interferometria a bassa coerenza per amplificare le fluttuazioni di fase e di ampiezza, creato spostando strutture di dispersione all'interno di campioni biologici, producendo un contrasto di motilità. D-FFOCT apre la possibilità di seguire lo sviluppo di complesse strutture multicellulari 3-D, come gli organoidi retinici.
In un nuovo articolo di Jules Scholler, Cassandra Groux, et al., pubblicato in Luce:scienza e applicazioni , un team di esperti di ottica (Institut Langevin, Parigi, Francia) guidato dalla dott.ssa Kate Grieve del Quinze-Vingts National Eye Hospital (Parigi, Francia), in collaborazione con biologi cellulari (Institut de la Vision, Parigi, Francia), hanno sviluppato e applicato una nuova modalità di imaging per l'imaging di organoidi retinici in fase di sviluppo.
Questi scienziati riassumono il principio di funzionamento del loro microscopio:
"Utilizziamo l'amplificazione interferometrica di un dispositivo per tomografia a coerenza ottica a campo pieno e studiamo la fluttuazione del segnale interferometrico per costruire quantitativamente volumi tomografici con un contrasto metabolico. Grazie alla nostra elevata sensibilità, siamo in grado di ricostruire immagini ad alto contrasto di campioni quasi trasparenti senza utilizzare etichette esogene".
"Grazie alla configurazione a campo pieno e all'elevata sensibilità, il nostro metodo è più veloce e richiede un'intensità di illuminazione molto inferiore rispetto alle tecniche di microscopia non lineare che possono danneggiare irreversibilmente il campione. Questo ci permette di studiare lo sviluppo dello stesso campione per periodi di diverse settimane", hanno aggiunto.
"D-FFOCT avrà molte potenziali applicazioni per i tessuti viventi in vitro, compresa la modellazione della malattia, screening del cancro, e screening dei farmaci, "predicono gli scienziati.
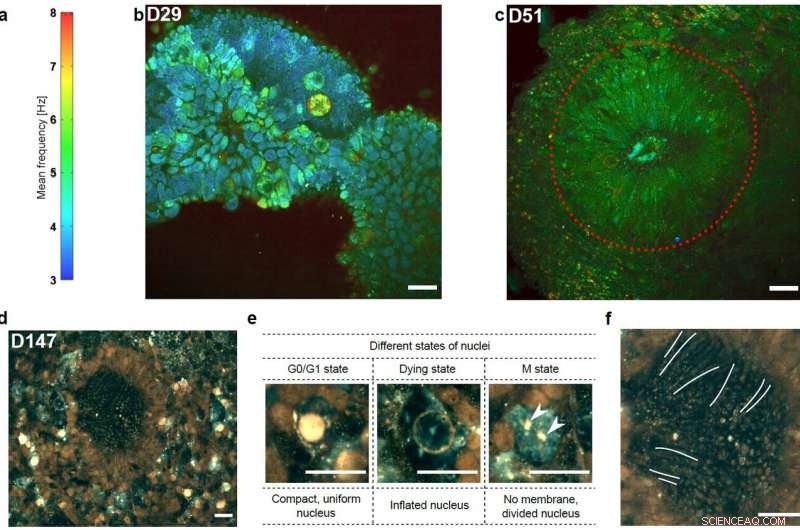
un, Barra dei colori delle immagini D-FFOCT con una mappa dei colori coerente per (b, C). B, Immagine di un organoide retinico D29, mostrando più celle con diversi profili dinamici. C, Immagine di un organoide retinico D51, dove i precursori dei fotorecettori iniziano ad apparire in una formazione a rosetta (linea rossa tratteggiata). Imaging ad alta risoluzione temporale eseguito su un organoide retinico D147. D, Parte dell'organoide retinico ha rivelato strutture fusiformi corrispondenti ai segmenti esterni emergenti dei fotorecettori al centro della rosetta. e, Vista ingrandita dei nuclei in tre diversi stati intorno alla rosetta:(i) un nucleo in uno stato normale con un compatto, forma uniforme ed è molto brillante (cioè, esibendo un'elevata attività); (ii) un apparentemente morente, nucleo gonfiato, esibendo quasi nessuna attività; e (iii) un nucleo in fase di divisione senza membrana nucleare definita nel citoplasma, e due parti distinte (frecce bianche) del contenuto di un nucleo (suggerendo la mitosi del nucleo con cromosomi già divisi, con lo stesso livello di attività subcellulare del nucleo "normale"). F, Immagine ingrandita delle strutture del tipo di segmento esterno del fotorecettore riprodotte lateralmente; tre di loro sono contrassegnati da una linea bianca. Barra della scala:20 μm. Credito:Jules Scholler, Cassandra Groux, Olivier Goureau, José Alain Sahel, Mathias Fink, Sacha Reichmann, Claude Boccara e Kate Grieve