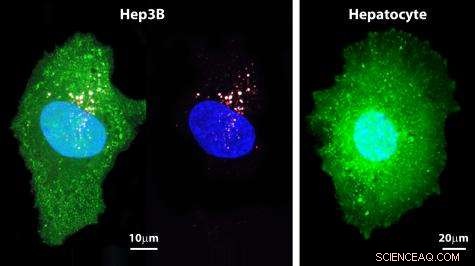
La figura a sinistra (Hep3B) mostra una cellula epatica cancerosa con fluorescenza verde penetrata da protocellule. I piccoli punti rossi sono involucri a doppio strato lipidico. Il loro carico - nanoparticelle piene di droga, i loro pori qui pieni di coloranti fluorescenti bianchi per scopi di imaging - penetrano nella cellula cancerosa. (La penetrazione è più chiaramente visibile nella seconda immagine.) La cellula normale sulla destra (epatocita) non mostra penetrazione. (Immagini per gentile concessione di Carlee Ashley)
(PhysOrg.com) -- Fusione di nanotecnologia e ricerca medica, Laboratori Nazionali Sandia, l'Università del Nuovo Messico, e il Centro per la ricerca e il trattamento del cancro dell'UNM hanno prodotto una strategia efficace che utilizza le nanoparticelle per distruggere le cellule cancerose con una miscela di farmaci killer.
Nell'articolo di copertina del numero di maggio di Materiali della natura , disponibile online il 17 aprile , i ricercatori descrivono le nanoparticelle di silice di circa 150 nanometri di diametro come a nido d'ape con cavità che possono immagazzinare grandi quantità e varietà di farmaci.
"L'enorme capacità del nucleo nanoporoso, con la sua elevata superficie, combinato con il migliore targeting di un doppio strato lipidico incapsulante [chiamato liposoma], consentire a una singola "protocella" caricata con un cocktail di farmaci di uccidere una cellula cancerosa resistente ai farmaci, " dice Jeff Brinker, ricercatore di Sandia e professore dell'UNM, il ricercatore principale. "Si tratta di un aumento di un milione di volte dell'efficienza rispetto a metodi comparabili che impiegano i soli liposomi, senza nanoparticelle, come vettori di farmaci".
Le nanoparticelle e le membrane simili a cellule circostanti formate dai liposomi insieme diventano la combinazione denominata protocella:la membrana sigilla il carico mortale e viene modificata con molecole (peptidi) che si legano specificamente ai recettori sovraespressi sulla superficie della cellula tumorale. (Troppi recettori sono un segnale che la cellula è cancerogena.) Le nanoparticelle forniscono stabilità alla membrana supportata e contengono e rilasciano il carico terapeutico all'interno della cellula.
Un'attuale strategia di consegna delle nanoparticelle approvata dalla Food and Drug Administration consiste nell'utilizzare i liposomi stessi per contenere e consegnare il carico. In un confronto diretto di liposomi e protocelle mirati con membrane e composizioni peptidiche identiche, Brinker e colleghi riferiscono che la maggiore capacità di carico, la stabilità e l'efficacia mirata delle protocellule porta a una citotossicità [distruzione] molte volte maggiore diretta specificamente verso le cellule tumorali del fegato umano.
Un altro vantaggio delle protocelle rispetto ai soli liposomi, dice l'autore principale Carlee Ashley, un borsista post-dottorato di Harry S. Truman presso la sede di Sandia in California a Livermore, è che i liposomi utilizzati come vettori necessitano di strategie di carico specializzate che rendono il processo più difficile. "Abbiamo dimostrato che possiamo semplicemente immergere le nanoparticelle per caricarle con combinazioni di farmaci uniche necessarie per la medicina personalizzata. Incapsulano efficacemente le tossine e siRNA [acido ribonucleico] che mettono a tacere le espressioni delle proteine".
RNA, il messaggero biologico che dice alle cellule quali proteine produrre, in questo caso serve per silenziare la fabbrica cellulare, un modo per provocare l'apoptosi o la morte cellulare. "Si" è l'abbreviazione di "silenzio".
I lipidi fungono anche da scudo che impedisce ai farmaci chemioterapici tossici di fuoriuscire dalla nanoparticella fino a quando la protocella non si lega e prende piede all'interno della cellula cancerosa. Ciò significa che pochi veleni penetrano nel sistema dell'ospite umano, se le protocellule non trovano cellule cancerose. Questo occultamento mitiga gli effetti collaterali tossici attesi dalla chemioterapia convenzionale.
Anziché, le particelle, realizzate abbastanza piccole da galleggiare sotto il radar del fegato e di altri organi depurativi, possono circolare innocue per giorni o settimane, a seconda della loro dimensione ingegnerizzata, cercando la loro preda.
Una libreria di fagi - virus che attaccano i batteri - è stata creata presso il centro oncologico accreditato a livello nazionale dell'UNM dal collaboratore David Peabody. Ciò ha permesso ai ricercatori di esporre i fagi a un gruppo di cellule cancerose e cellule normali, consentendo l'identificazione di peptidi che si legano specificamente alle cellule tumorali ma non alle cellule normali.
"Le proteine modificate con un peptide mirato che si lega a un particolare carcinoma mostrano un valore 10, Affinità 000 volte maggiore per quel cancro rispetto ad altre cellule non correlate, " ha detto Ashley.
Brinker aggiunge, "Una caratteristica chiave della nostra protocella è che il suo doppio strato fluido consente un legame ad alta affinità con solo alcuni di questi peptidi in generale. Ciò riduce il legame non specifico e la risposta immunitaria".
Il metodo è in fase di sperimentazione su cellule tumorali umane in vivo, e sarà presto testato sui tumori del topo presso il centro oncologico dell'UNM.
I ricercatori continuano a ottimizzare le dimensioni della particella di silice porosa, che si forma per aerosolizzazione di una soluzione precursore. Il processo di fabbricazione delle nanoparticelle porose, chiamato autoassemblaggio indotto dall'evaporazione, e pioniere nel laboratorio Brinker — produce particelle da 50 nm a diversi micron di diametro. Le dimensioni delle particelle tra 50 e 150 nanometri di diametro sono ideali per massimizzare la circolazione e l'assorbimento nelle cellule tumorali, quindi le particelle sono preselezionate per dimensione prima della loro formazione in protocelle.
"Le loro dimensioni complessive determinano quanto ampiamente saranno distribuiti nel flusso sanguigno, " ha detto Brinker. "Stiamo alterando la nostra sintesi per favorire le dimensioni più piccole".
Importanti anche per il tempo di circolazione della particella sono la sua carica elettrica e l'idrofobicità [evitare l'acqua], che può migliorare o sminuire la sua capacità di rimanere libero da intrecci molecolari o energetici indesiderati.
Il metodo può essere disponibile in commercio in cinque anni, stimano i ricercatori.