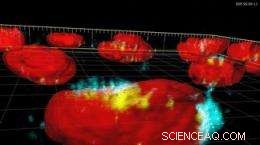
Immagine:particelle di ossido di ferro superparamagnetico (blu e giallo) assorbite in un nucleo di una cellula (nucleo in rosso).
(PhysOrg.com) -- Rilevare le cellule cancerose e distruggerle, iniettare farmaci con estrema precisione nelle cellule malate del corpo umano:questi sono solo due esempi di ciò che gli scienziati dell'EPFL stanno tentando di ottenere utilizzando nanoparticelle di ossido di ferro sviluppate nel Laboratorio di tecnologia delle polveri della scuola (LTP).
Solo 5-10 nanometri di diametro (un nanometro è un milionesimo di millimetro), le nanoparticelle di ossido di ferro superparamagnetiche studiate dal team LTP del professor Heinrich Hofmann sono promettenti, perché esibiscono proprietà magnetiche se esposte a un campo magnetico esterno. Questa caratteristica è importante per alcune applicazioni mediche, come la diagnosi di malattie come l'artrite, localizzare tumori, e distruggere le cellule tumorali nei pazienti.
Rilevare il cancro
Gli scienziati dell'EPFL stanno esaminando tre applicazioni principali:diagnostica, trattamento ed eliminazione delle cellule maligne. “In pratica, le particelle di ossido di ferro sono già utilizzate come agenti di contrasto nella risonanza magnetica (MRI) nei casi di tumore al fegato, ” nota Hofmann. “Stiamo studiando come applicare questo metodo a tutti i tipi di tumori e, se possibile, ad altre malattie, come l'artrite. Quest'ultimo è l'obiettivo di un grande progetto UE FP-7 (Nanodiara).” Ecco come funziona:le cellule cancerose hanno recettori sulla loro superficie, una sorta di ID cellulare. Il rivestimento sulle nanoparticelle viene adattato di conseguenza (tramite anticorpi, Per esempio), in modo che una volta iniettati per via endovenosa, si legheranno solo ai recettori sulle cellule tumorali. E poiché una particella di ossido di ferro altera il contrasto dei tessuti quando viene sottoposta a un campo magnetico, è quindi possibile individuare la posizione esatta delle cellule tumorali utilizzando la risonanza magnetica. “Finora questa tecnica è stata validata solo per i tumori del fegato, perché per ogni tipo di cancro, devono essere aggiunti elementi di superficie, che modificano il comportamento delle particelle. Eppure è abbastanza difficile capire il comportamento delle nanoparticelle in un fluido complesso, come il sangue, " spiega.
Trattamento mirato
Un aspetto della ricerca si concentra su una nuova entusiasmante applicazione:la somministrazione mirata di farmaci a cellule specifiche. “È possibile che le nanoparticelle di ossido di ferro penetrino direttamente negli organelli di una cellula. Questa proprietà apre la possibilità di somministrare un farmaco direttamente all'interno di una cellula, ” spiega Hofmann. Ciò presenta chiari vantaggi rispetto ai metodi di somministrazione dei farmaci esistenti. Il professore di radiologia dell'Università di Ginevra Jean-Paul Vallée afferma:
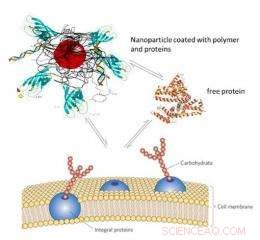
“Negli attuali trattamenti farmacologici sistemici, il farmaco non viene somministrato selettivamente nel corpo, ma assorbito ampiamente. Con questo nuovo metodo, potremmo evitare certi effetti collaterali e somministrare il farmaco solo alle cellule che necessitano di essere trattate”.
Distruggere i tumori con il calore
Oltre a rilevare cellule specifiche e somministrare farmaci direttamente in esse, le particelle di ossido di ferro hanno anche la capacità di distruggere ipertermicamente i tumori ossei. Nel cancro alle ossa, le metastasi si sviluppano spesso nella colonna vertebrale. Un trattamento attuale prevede l'iniezione di una sostanza simile al cemento nei corpi delle vertebre. Una volta che questa sostanza a base di polimeri è nel corpo, si solidifica e quindi stabilizza le vertebre. Secondo i ricercatori, se particelle superparamagnetiche sono state aggiunte al cemento prima dell'iniezione, sarebbe possibile trasferire energia applicando un campo magnetico alternato esterno, riscaldando così l'impianto fino a 46°C. Questa procedura distruggerebbe selettivamente le cellule tumorali nelle vicinanze, perché sono meno tolleranti al calore rispetto ai tessuti normali. “Questo metodo sarebbe meno aggressivo dei laser, che bruciano anche cellule sane e lasciano dietro di sé materiali di scarto, ” aggiunge Hofmann.
Per il momento, queste tre applicazioni sono in fase preclinica, e fanno parte di diversi progetti che coinvolgono numerosi partner, come gli ospedali universitari di Losanna (CHUV), l'Università di Ginevra e il Centro svizzero di elettronica e microtecnologia (CSEM), così come aziende come ANTIA o MERCK-Serono.