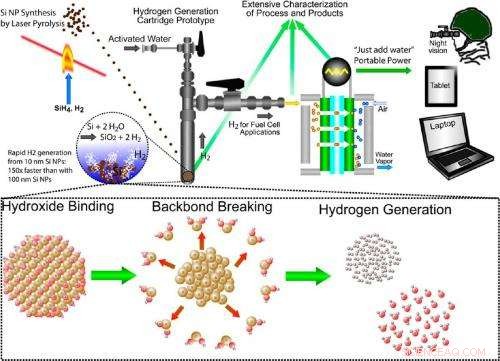
Illustrazione dell'approccio multidisciplinare per la produzione di idrogeno attraverso l'ossidazione del silicio. L'approccio prevede la sintesi di nanoparticelle di silicio, la reazione silicio-acqua che genera idrogeno su richiesta, e utilizzando l'idrogeno in una cella a combustibile per l'energia portatile. Credito:Folarin Erogbogbo, et al. ©2013 American Chemical Society
(Phys.org) — Sebbene gli scienziati sappiano che quando il silicio si mescola con l'acqua, l'idrogeno viene prodotto per ossidazione, nessuno si aspettava quanto velocemente le nanoparticelle di silicio potessero svolgere questo compito. Come ha rivelato un nuovo studio, Le nanoparticelle di silicio da 10 nm possono generare idrogeno 150 volte più velocemente delle nanoparticelle di silicio da 100 nm, e 1, 000 volte più veloce del silicio sfuso. La scoperta potrebbe aprire la strada a tecnologie rapide di generazione di idrogeno "basta aggiungere acqua" per dispositivi portatili senza bisogno di luce, calore, o elettricità.
I ricercatori, Folarin Erogbogbo presso l'Università di Buffalo e coautori, hanno pubblicato il loro articolo sull'uso del nanosilicio per generare idrogeno in un recente numero di Nano lettere .
Se l'idrogeno dovesse mai essere utilizzato per fornire energia per ampie applicazioni commerciali, uno dei requisiti è trovare un veloce, modo economico per produrre idrogeno. Una delle tecniche di produzione dell'idrogeno più comuni è la scissione dell'acqua in idrogeno e ossigeno. Ci sono diversi modi per dividere l'acqua, come con una corrente elettrica (elettrolisi), calore, luce del sole, o una sostanza che reagisce chimicamente con l'acqua. Tali sostanze includono alluminio, zinco, e silicio.
Come hanno spiegato gli scienziati, le reazioni di ossidazione silicio-acqua sono state finora lente e non competitive con altre tecniche di scissione dell'acqua. Però, il silicio ha alcuni vantaggi teorici, come essere abbondanti, essendo facile da trasportare, e ad alta densità di energia. Ulteriore, per ossidazione con acqua, il silicio può teoricamente rilasciare due moli di idrogeno per mole di silicio, o il 14% della propria massa in idrogeno.
Per queste ragioni, gli scienziati hanno deciso di dare un'occhiata più da vicino al silicio, in particolare nanoparticelle di silicio, che non sono stati precedentemente studiati per la generazione di idrogeno. Poiché le nanoparticelle di silicio hanno una superficie maggiore rispetto alle particelle più grandi o al silicio sfuso, ci si aspetterebbe che le nanoparticelle possano generare idrogeno più rapidamente dei pezzi di silicio più grandi.
Ma i miglioramenti che gli scienziati hanno scoperto con le nanoparticelle di silicio hanno superato di gran lunga le loro aspettative. La reazione di particelle di silicio da 10 nm con acqua ha prodotto un totale di 2,58 moli di idrogeno per mole di silicio (anche superando le aspettative teoriche), impiegando 5 secondi per produrre 1 mmol di idrogeno. In confronto, la reazione con particelle di silicio da 100 nm ha prodotto un totale di 1,25 moli di idrogeno per mole di silicio, impiegando 811 secondi per produrre ogni mmol di idrogeno. Per il silicio sfuso, la produzione totale era solo di 1,03 mol di idrogeno per mole di silicio, impiegando ben 12,5 ore per produrre ogni mmol di idrogeno. Per un confronto tariffario, il silicio a 10 nm ha generato idrogeno 150 volte più velocemente del silicio a 100 nm e 1, 000 volte più veloce del silicio sfuso.
"Credo che il più grande significato di questo lavoro sia la dimostrazione che il silicio può reagire con l'acqua abbastanza rapidamente da essere di uso pratico per la generazione di idrogeno su richiesta, " coautore Mark Swihart, Professore di Ingegneria Chimica e Biologica presso l'Università di Buffalo, detto Phys.org . "Questo risultato è stato sia inaspettato che di potenziale importanza pratica. Anche se non credo che l'ossidazione delle nanoparticelle di silicio diventerà un metodo fattibile per la generazione di idrogeno su larga scala in tempi brevi, questo processo potrebbe essere piuttosto interessante per applicazioni portatili su piccola scala in cui è disponibile acqua".

Un confronto dei tassi di generazione di idrogeno per diverse forme di silicio. Le tariffe massime sono nella colonna di sinistra con le immagini dei campioni su di esse. Le tariffe medie sono nella colonna di destra. La linea rossa indica il tasso massimo riportato per l'idrogeno generato dall'alluminio. Credito:Folarin Erogbogbo, et al. ©2013 American Chemical Society
Oltre a produrre idrogeno più velocemente di pezzi di silicio più grandi, il silicio a 10 nm produce anche idrogeno significativamente più velocemente delle nanoparticelle di alluminio e zinco. Come ha spiegato Swihart, la spiegazione di questa disuguaglianza differisce per i due materiali.
"Rispetto all'alluminio, il silicio reagisce più velocemente perché l'alluminio forma un ossido più denso e robusto (Al 2 oh 3 ) sulla sua superficie, che limita la reazione, " ha detto. "In presenza di una base come KOH [idrossido di potassio], il silicio produce principalmente acido silicico solubile (Si(OH) 4 ). Rispetto allo zinco, il silicio è semplicemente più reattivo, soprattutto a temperatura ambiente."
Sebbene la maggiore superficie del silicio da 10 nm rispetto ai pezzi di silicio più grandi contribuisca al suo rapido tasso di produzione di idrogeno, la superficie da sola non può spiegare l'enorme aumento del tasso osservato dagli scienziati. La superficie del silicio a 10 nm è di 204 m 2 /G, circa 6 volte maggiore della superficie del silicio da 100 nm, che è 32 m 2 /G.
Per capire cosa causa l'aumento molto maggiore del tasso di produzione di idrogeno, i ricercatori hanno condotto esperimenti durante il processo di incisione del silicio. Hanno scoperto che, per le particelle a 10 nm, l'attacco chimico comporta la rimozione di un numero uguale di piani reticolari in ciascuna direzione (attacco isotropo). In contrasto, per particelle e microparticelle da 100 nm, un numero disuguale di piani reticolari viene rimosso in ciascuna direzione (attacco anisotropo).
I ricercatori attribuiscono questa differenza di incisione alle diverse geometrie dei cristalli di diverse dimensioni. In conseguenza di questa differenza, le particelle più grandi adottano forme non sferiche che espongono superfici meno reattive rispetto alle particelle più piccole, che rimangono quasi sferici, esponendo tutte le sfaccettature del cristallo alla reazione. Le particelle più grandi sviluppano anche strati più spessi di sottoprodotti di silicio ossidato attraverso i quali l'acqua deve diffondersi. Entrambi questi fattori limitano la velocità della reazione su particelle più grandi.
Per confermare che la reazione silicio-acqua a 10 nm genera idrogeno senza sottoprodotti che potrebbero interferire con le applicazioni, i ricercatori hanno utilizzato l'idrogeno generato dal silicio per far funzionare una cella a combustibile. La cella a combustibile ha funzionato molto bene, producendo più corrente e tensione rispetto alla quantità teorica di idrogeno puro, il che è dovuto al fatto che le particelle da 10 nm hanno generato più idrogeno del teorico 14% in peso.
I ricercatori sperano che questa sorprendente capacità delle nanoparticelle di silicio di dividere rapidamente l'acqua e generare idrogeno possa portare allo sviluppo di una tecnologia a richiesta dell'idrogeno che potrebbe consentire l'utilizzo delle celle a combustibile in dispositivi portatili. Questa tecnologia richiederebbe una grande metodo efficiente dal punto di vista energetico per la produzione di nanoparticelle di silicio, ma potrebbe avere alcuni vantaggi rispetto ad altre tecniche di generazione dell'idrogeno.
"Il vantaggio chiave dell'ossidazione del silicio per la generazione di idrogeno è la sua semplicità, " Swihart ha detto. "Con questo approccio, l'idrogeno viene prodotto rapidamente, a temperatura ambiente, e senza bisogno di alcuna fonte di energia esterna. L'energia necessaria per la generazione di idrogeno è effettivamente immagazzinata nel silicio. Tutta l'energia necessaria per la produzione del silicio può essere fornita in una posizione centrale, e il silicio può quindi essere utilizzato in applicazioni portatili.
"Lo svantaggio principale dell'ossidazione del silicio è la sua relativa inefficienza. L'input energetico richiesto per creare le nanoparticelle di silicio è molto maggiore dell'energia disponibile dall'idrogeno che viene infine prodotto. Per applicazioni su larga scala, questo sarebbe un problema. Per applicazioni portatili, non è. Per esempio, il costo dell'elettricità fornita da una normale batteria domestica può facilmente essere da 10 a 100 volte superiore al costo dell'elettricità da un'utilità, ma le batterie svolgono ancora un ruolo importante nelle nostre vite".
Nel futuro, i ricercatori hanno in programma di aumentare ulteriormente la capacità di generazione di idrogeno dell'ossidazione del silicio sperimentando diverse miscele.
"Una direzione che stiamo attualmente perseguendo è l'uso di miscele di nanoparticelle di silicio con idruri metallici, che reagiscono anche con l'acqua per produrre idrogeno, Swihart ha detto. "Composti come l'idruro di litio e l'idruro di sodio reagiscono con l'acqua per produrre la base (LiOH o NaOH) necessaria per catalizzare l'ossidazione del silicio. Però, possono reagire troppo velocemente con l'acqua (in modo esplosivo) e non sono stabili all'aria. Mescolarli con nanoparticelle di silicio o rivestirli con nanoparticelle di silicio può servire sia a temperare la loro reattività che ad aumentare la capacità di generazione di idrogeno del sistema sostituendo la base aggiunta (ad es. KOH nel documento pubblicato) con un materiale che genera anche idrogeno."
Copyright 2013 Phys.org
Tutti i diritti riservati. Questo materiale non può essere pubblicato, trasmissione, riscritto o ridistribuito in tutto o in parte senza l'espresso permesso scritto di Phys.org.