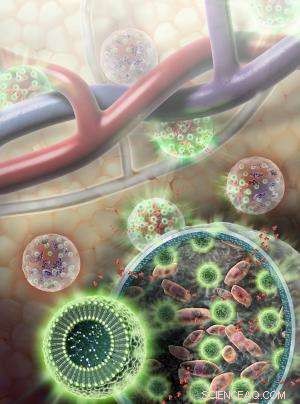
I nanosensori (sfere verdi) sono composti da molecole di grasso e L-arginina, così come molecole indicatrici separate che emettono segnali rilevabili con la risonanza magnetica e segnali luminosi quando le cellule sono vive. I nanosensori sono racchiusi in una membrana di idrogel insieme alle cellule epatiche (rosa). I nutrienti e altre molecole relativamente piccole (rosse) sono in grado di viaggiare attraverso la membrana dell'idrogel da e verso il flusso sanguigno. Credito:Sayo Studios
I ricercatori della Johns Hopkins hanno escogitato un modo per rilevare se le cellule precedentemente trapiantate in un animale vivo sono vive o morte, un'innovazione, secondo loro, potrebbe accelerare lo sviluppo di terapie di sostituzione cellulare per condizioni come l'insufficienza epatica e il diabete di tipo 1. Come riportato nel numero di marzo di Materiali della natura , lo studio ha utilizzato sensori di pH su nanoscala e macchine per la risonanza magnetica (MRI) per stabilire se le cellule epatiche iniettate nei topi sono sopravvissute nel tempo.
"Questa tecnologia ha il potenziale per trasformare il corpo umano in una scatola nera e dirci se le cellule trapiantate sono ancora vive, "dice Mike McMahon, dottorato di ricerca, un professore associato di radiologia presso la Johns Hopkins University School of Medicine che ha supervisionato lo studio. "Queste informazioni saranno preziose nella messa a punto delle terapie".
I progressi della medicina rigenerativa dipendono da mezzi affidabili per sostituire le cellule danneggiate o mancanti, come l'iniezione di cellule pancreatiche in persone con diabete le cui cellule non producono abbastanza insulina. Per proteggere le cellule trapiantate dal sistema immunitario, pur consentendo il libero flusso di nutrienti e insulina tra le cellule e il corpo, possono essere racchiusi in morbide membrane di idrogel prima del trapianto. Ma, spiega McMahon, "una volta inserite le celle, non hai davvero idea di quanto tempo sopravvivano." Tali cellule trapiantate alla fine smettono di funzionare nella maggior parte dei pazienti, chi deve riprendere l'assunzione di insulina. A quel punto, i medici possono solo presumere che le cellule siano morte, ma non sanno quando o perché, dice McMahon.
Con questo problema in mente, Il gruppo di McMahon, specializzata in metodi di rilevamento di cambiamenti chimici, collaborato con il gruppo di ricerca guidato da Jeff Bulte, dottorato di ricerca, il direttore dell'imaging cellulare presso l'Istituto di Hopkins per l'ingegneria cellulare. Il gruppo di Bulte escogita modi per tracciare le cellule impiantate attraverso il corpo usando la risonanza magnetica. Guidato dal ricercatore Kannie Chan, dottorato di ricerca, il team ha ideato un piccolissimo, o su scala nanometrica, sensore riempito con L-arginina, un integratore nutrizionale che risponde chimicamente a piccoli cambiamenti di acidità (pH) causati dalla morte delle cellule vicine. I cambiamenti nell'acidità provocherebbero a loro volta cambiamenti nelle molecole sensoriali incorporate nel sottile strato di grasso che costituisce l'esterno della nanoparticella, emettendo un segnale che potrebbe essere rilevato dalla risonanza magnetica.
Per testare come funzionerebbero questi nanosensori in un corpo vivente, il team li ha caricati in sfere di idrogel insieme a cellule epatiche, una potenziale terapia per i pazienti con insufficienza epatica, e un altro sensore che emette luce bioluminescente solo mentre le cellule sono vive. Le sfere sono state iniettate proprio sotto la pelle dei topi. Come confermato dal segnale luminoso, la risonanza magnetica ha rilevato con precisione dove si trovavano le cellule nel corpo e in quale proporzione erano ancora vive. (Tali indicatori luminosi non possono essere utilizzati per tracciare le cellule negli esseri umani perché i nostri corpi sono troppo grandi perché i segnali visibili possano passare, ma questi indicatori hanno permesso al team di verificare se i nanosensori MRI funzionavano correttamente nei topi.)
"È stato emozionante vedere che funziona così bene in un corpo vivente, " dice Chan. Il team spera che, poiché i componenti del sistema, la membrana idrogel, molecole di grasso, e L-arginina:sono sicuri per l'uomo, adattare la loro scoperta per l'uso clinico si dimostrerà relativamente semplice. "Questo dovrebbe eliminare molte congetture dal trapianto di cellule consentendo ai medici di vedere se le cellule sopravvivono, e se no, quando muoiono, " dice Chan. "In questo modo potrebbero essere in grado di capire cosa sta uccidendo le cellule, e come prevenirlo".
Le potenziali applicazioni dei sensori non si limitano alle cellule all'interno di capsule di idrogel, Note di massa. "Queste nanoparticelle funzionerebbero al di fuori delle capsule, e potrebbero essere accoppiati con molti diversi tipi di cellule. Per esempio, possono essere usati per vedere se le cellule tumorali stanno morendo in risposta alla chemioterapia, " lui dice.