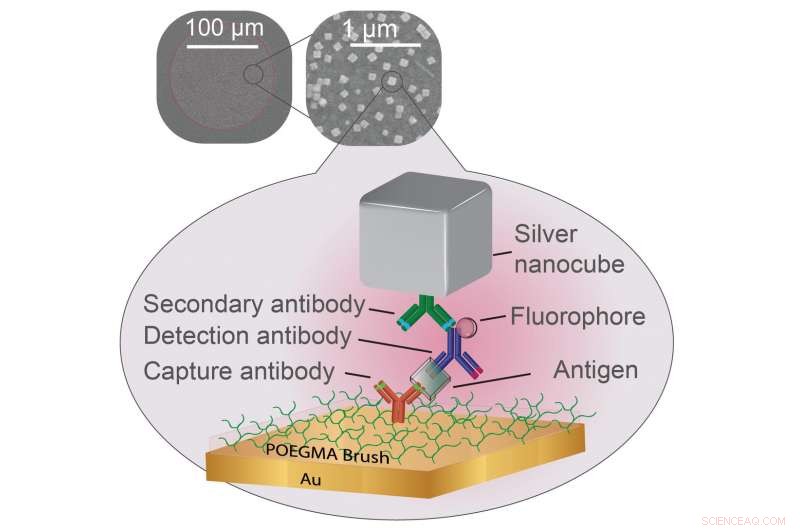
I ricercatori hanno dimostrato che la plasmonica può potenziare i marcatori fluorescenti utilizzati per segnalare campioni positivi in alcuni tipi di test per le malattie. Un rivestimento a spazzola polimerica tiene lontane le biomolecole indesiderate mentre un anticorpo di cattura (rosso) cattura i biomarcatori della malattia (trasparente). Un anticorpo di rilevamento (blu) si aggancia quindi al biomarcatore ed emette luce da un fluoroforo (sfera) attaccato. Tutto questo è racchiuso da un sottile strato di oro e un nanocubo d'argento che è attaccato da un terzo anticorpo (verde), creando le condizioni affinché il fluoroforo emetta una luce più brillante. Credito:Daniela Cruz, Duke University
Gli ingegneri della Duke University hanno dimostrato che i cubi d'argento di dimensioni nanometriche possono rendere i test diagnostici basati sulla fluorescenza più facili da leggere, rendendoli più di 150 volte più luminosi. In combinazione con una piattaforma diagnostica emergente per il punto di cura già mostrata in grado di rilevare piccole tracce di virus e altri biomarcatori, l'approccio potrebbe consentire a tali test di diventare molto più economici e più diffusi.
I risultati sono apparsi online il 6 maggio sulla rivista Nano lettere .
La plasmonica è un campo scientifico che intrappola l'energia in un circuito di feedback chiamato plasmone sulla superficie dei nanocubi d'argento. Quando le molecole fluorescenti sono inserite tra uno di questi nanocubi e una superficie metallica, l'interazione tra i loro campi elettromagnetici fa sì che le molecole emettano luce molto più vigorosamente. Maiken Mikkelsen, James N. e Elizabeth H. Barton Professore Associato di Ingegneria Elettrica e Informatica presso la Duke, ha lavorato con il suo laboratorio alla Duke per creare nuovi tipi di fotocamere iperspettrali e segnali ottici superveloci utilizzando la plasmonica per quasi un decennio.
Allo stesso tempo, ricercatori nel laboratorio di Ashutosh Chilkoti, il Professore distinto di ingegneria biomedica di Alan L. Kaganov, hanno lavorato su un autonomo, test diagnostico point-of-care in grado di rilevare tracce di biomarcatori specifici da fluidi biomedici come il sangue. Ma poiché i test si basano su marcatori fluorescenti per indicare la presenza dei biomarcatori, vedere la debole luce di un test appena positivo richiede attrezzature costose e ingombranti.
"La nostra ricerca ha già dimostrato che la plasmonica può aumentare la luminosità delle molecole fluorescenti decine di migliaia di volte, " ha detto Mikkelsen. "Utilizzarlo per migliorare i test diagnostici che sono limitati dalla loro fluorescenza è stata chiaramente un'idea molto eccitante".
"Non ci sono molti esempi di persone che usano la fluorescenza potenziata da plasmoni per la diagnostica point-of-care, e i pochi che esistono non sono stati ancora implementati nella pratica clinica, " ha aggiunto Daria Semeniak, uno studente laureato nel laboratorio di Chilkoti. "Ci sono voluti un paio d'anni, ma pensiamo di aver sviluppato un sistema che può funzionare".
Nel nuovo giornale, i ricercatori del laboratorio Chilkoti costruiscono la loro piattaforma diagnostica supersensibile chiamata D4 Assay su una sottile pellicola d'oro, lo yin preferito allo yang del nanocubo d'argento plasmonico. La piattaforma inizia con un sottile strato di rivestimento a pennello polimerico, che impedisce a qualsiasi cosa di attaccarsi alla superficie dell'oro che i ricercatori non vogliono attaccarsi lì. I ricercatori utilizzano quindi una stampante a getto d'inchiostro per collegare due gruppi di molecole su misura per attaccarsi al biomarcatore che il test sta cercando di rilevare. Un set è fissato in modo permanente alla superficie dell'oro e cattura una parte del biomarcatore. L'altro viene lavato via dalla superficie una volta iniziato il test, si attacca a un altro pezzo del biomarcatore, e lampeggia per indicare che ha trovato il suo obiettivo.
Dopo alcuni minuti passano per consentire che si verifichino le reazioni, il resto del campione viene lavato via, lasciando dietro di sé solo le molecole che sono riuscite a trovare le corrispondenze dei loro biomarcatori, fluttuanti come fari fluorescenti legati a un pavimento dorato.

Un ricercatore possiede una versione di prova del saggio D4, che ha dimostrato di essere in grado di rilevare tracce di biomarcatori di malattie. Credito:Michaela Kane, Duke University
"Il vero significato del test è il rivestimento della spazzola polimerica, " ha affermato Chilkoti. "La spazzola polimerica ci consente di memorizzare tutti gli strumenti di cui abbiamo bisogno sul chip mantenendo un design semplice".
Mentre il test D4 è molto bravo a catturare piccole tracce di specifici biomarcatori, se ci sono solo tracce, i fari fluorescenti possono essere difficili da vedere. La sfida per Mikkelsen e i suoi colleghi è stata quella di posizionare i loro nanocubi d'argento plasmonici sopra i beacon in modo tale da sovralimentare la fluorescenza dei beacon.
Ma come di solito accade, questo era più facile a dirsi che a farsi.
"La distanza tra i nanocubi d'argento e la pellicola d'oro determina quanto più luminosa diventa la molecola fluorescente, " ha detto Daniela Cruz, uno studente laureato che lavora nel laboratorio di Mikkelsen. "La nostra sfida era quella di rendere il rivestimento della spazzola polimerica abbastanza spesso da catturare i biomarcatori - e solo i biomarcatori di interesse - ma abbastanza sottile da migliorare ancora le luci diagnostiche".
I ricercatori hanno tentato due approcci per risolvere questo enigma di Riccioli d'oro. Per prima cosa hanno aggiunto uno strato elettrostatico che si lega alle molecole del rivelatore che trasportano le proteine fluorescenti, creando una sorta di "secondo piano" su cui i nanocubi d'argento potrebbero sedersi. Hanno anche provato a funzionalizzare i nanocubi d'argento in modo che si attaccassero direttamente alle singole molecole del rivelatore su base uno contro uno.
Sebbene entrambi gli approcci siano riusciti ad aumentare la quantità di luce proveniente dai fari, il primo ha mostrato il miglior miglioramento, aumentando la sua fluorescenza di oltre 150 volte. Però, questo metodo richiede anche un passaggio in più per creare un "secondo piano, " che aggiunge un altro ostacolo alla progettazione di un modo per farlo funzionare su una diagnostica commerciale point-of-care piuttosto che solo in un laboratorio. E mentre la fluorescenza non è migliorata tanto nel secondo approccio, l'accuratezza del test ha funzionato.
"Costruire dispositivi lab-on-a-chip microfluidici attraverso entrambi gli approcci richiederebbe tempo e risorse, ma sono entrambi fattibili in teoria, " disse Cassio Fontes, uno studente laureato nel laboratorio di Chilkoti. "Questo è ciò verso cui si sta muovendo il saggio D4."
E il progetto va avanti. All'inizio dell'anno, i ricercatori hanno utilizzato i risultati preliminari di questa ricerca per garantire un periodo di cinque anni, Premio per la ricerca R01 da 3,4 milioni di dollari del National Heart, Polmone, e Istituto del Sangue. I collaboratori lavoreranno per ottimizzare questi miglioramenti della fluorescenza integrando pozzi, canali microfluidici e altre soluzioni a basso costo in un dispositivo diagnostico in un unico passaggio che può eseguire automaticamente tutti questi passaggi ed essere letto da una comune fotocamera per smartphone in un dispositivo a basso costo.
"Una delle grandi sfide nei test point-of-care è la capacità di leggere i risultati, che di solito richiede rivelatori molto costosi, " ha detto Mikkelsen. "Questo è un grosso ostacolo per avere test usa e getta per consentire ai pazienti di monitorare le malattie croniche a casa o per l'uso in ambienti con poche risorse. Vediamo questa tecnologia non solo come un modo per aggirare quel collo di bottiglia, ma anche come un modo per migliorare l'accuratezza e la soglia di questi dispositivi diagnostici."