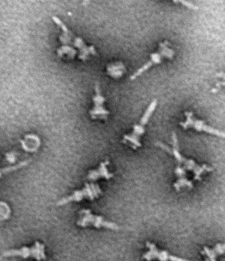
Parti di nanoiniettori da Salmonella viste al microscopio elettronico. Credito:Dr. Matthew Lefebre e Professor Jorge Galan (Yale University)
Se hai mai sofferto la miseria di un'intossicazione alimentare da un batterio come Shigella o Salmonella, allora le tue cellule sono state destinatarie di "nanoiniettori", punte microscopiche fatte di proteine attraverso le quali i patogeni secernono proteine effettrici nelle cellule ospiti umane, causando infezione.
Molti batteri usano i nanoiniettori per infettare milioni di persone in tutto il mondo ogni anno.
Oggi, Roberto De Guzman, professore associato di bioscienze molecolari presso l'Università del Kansas, sta guidando un gruppo di ricerca che sta valutando il potenziale dei nanoiniettori come bersaglio per una nuova classe di antibiotici. Il loro lavoro è finanziato da un quinquennale, Sovvenzione di 1,8 milioni di dollari dall'Istituto nazionale di allergie e malattie infettive, parte dell'Istituto Superiore di Sanità.
"Questa sovvenzione sosterrà i nostri studi sulla spiegazione di come vengono assemblati i nanoiniettori batterici, " ha detto De Guzman. "I nanoiniettori sono macchinari proteici utilizzati dai patogeni batterici per iniettare proteine di virulenza nelle cellule umane per causare malattie infettive. Sono di dimensioni nanometriche—sembrano aghi e i batteri li usano per iniettare proteine di virulenza nelle cellule ospiti—quindi li ho chiamati nanoiniettori. In microbiologia, sono conosciuti come parte del sistema di secrezione di tipo III, un macchinario per la somministrazione di proteine."
Il ricercatore della KU ha affermato che i nanoiniettori sono unici per i batteri patogeni e sono assolutamente necessari per l'infettività. La maggior parte delle persone ha sentito parlare delle malattie causate da agenti patogeni batterici che utilizzano nanoiniettori, molti dei quali hanno cambiato in peggio il corso dell'esperienza umana.
"Esempi sono Yersinia pestis, che ha causato la peste nera in Europa e ha alterato la storia del mondo, " ha detto De Guzman. "Inoltre, Pseudomonas aeruginosa, la prima causa di mortalità tra i pazienti con fibrosi cistica e una delle principali fonti di infezioni ospedaliere secondarie, e Clamidia, una delle principali fonti di malattie batteriche sessualmente trasmissibili".
Poiché un numero crescente di agenti patogeni ha sviluppato ceppi che non sono influenzati dagli antibiotici ora sul mercato, De Guzman ha affermato che sono necessari nuovi approcci nello sviluppo di farmaci e che i nanoiniettori potrebbero rappresentare un obiettivo utile.
"Il problema è che tutti questi agenti patogeni hanno sviluppato resistenza agli attuali antibiotici, " ha detto. "Inoltre, gli antibiotici non sono redditizi come altri farmaci, così le aziende farmaceutiche hanno sfavorevole svilupparli. Quindi, c'è una carenza di nuovi antibiotici in cantiere. Siamo in una tempesta perfetta quando l'età degli antibiotici non è più assicurata".
Un fattore importante nell'assegnazione di questa sovvenzione a KU da parte del NIH è uno spettrometro a risonanza magnetica nucleare o NMR da $ 1,9 milioni, essenzialmente un enorme magnete, che l'università ha acquistato nel 2004 attraverso un legame approvato dalla legislatura del Kansas.
"Abbiamo lo strumento fondamentale necessario per questa ricerca, " ha detto De Guzman. "Questa è la mia seconda borsa di studio NIH importante, più le altre sovvenzioni ricevute da KU che si basano sul magnete NMR. Penso che il Kansas abbia guadagnato molte volte in quell'investimento".
Utilizzando lo spettrometro NMR, De Guzman e il suo team sperano di comprendere meglio i processi biologici che creano i nanoiniettori.
"I nanoiniettori sono assemblati da circa 20 diversi tipi di proteine, e parti di esso, come l'ago stesso e le proteine associate all'ago, sono esposte in superficie, " ha detto De Guzman. "Il nanoiniettore è assemblato in modo preciso in cui le proteine si uniscono come blocchi di Lego aderenti. Un piccolo difetto potrebbe rendere il tutto inutile per i patogeni rendendoli non infettivi".
L'obiettivo finale è trovare o sviluppare composti che promuovono tali difetti nei nanoiniettori, rendendo gli agenti patogeni innocui per l'uomo.
"Il mio interesse è capire nei dettagli atomici come viene assemblato l'ago ed estendere tale conoscenza allo sviluppo di farmaci che interromperanno l'assemblaggio dei nanoiniettori e quindi impediranno agli agenti patogeni di infettare i loro ospiti, ", ha detto De Guzman.