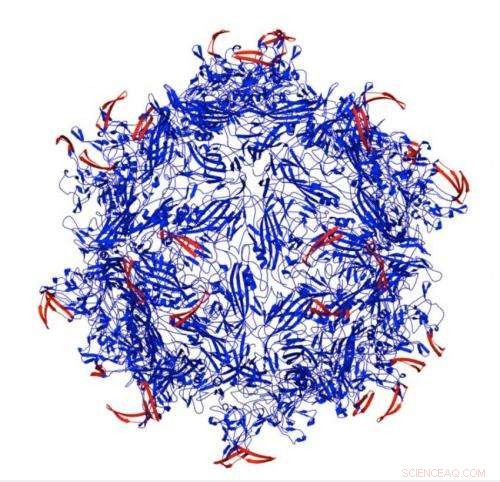
Un capside virale adeno-associato (blu) modificato da peptidi (rosso) inserito per bloccare il virus è il risultato della ricerca della Rice University su un nuovo modo per colpire le cellule cancerose e altre cellule malate. I peptidi sono vincolati alle proteasi sovraespresse nel sito dei tessuti malati; sbloccano il capside e gli permettono di consegnare il suo carico terapeutico. Credito:Junghae Suh/Rice University
Gli scienziati della Rice University hanno progettato un virus sintonizzabile che funziona come una cassetta di sicurezza. Ci vogliono due chiavi per aprirlo e rilasciare il suo carico terapeutico.
Il laboratorio Rice del bioingegnere Junghae Suh ha sviluppato un virus adeno-associato (AAV) che si sblocca solo in presenza di due proteasi selezionate, enzimi che tagliano altre proteine per lo smaltimento. Poiché alcune proteasi sono elevate nei siti tumorali, i virus possono essere progettati per colpire e distruggere le cellule tumorali.
Il lavoro appare online questa settimana sulla rivista dell'American Chemical Society ACS Nano .
Gli AAV sono abbastanza benigni e sono diventati oggetto di intensi studi come veicoli di consegna per le terapie geniche. I ricercatori spesso cercano di indirizzare gli AAV ai recettori cellulari che potrebbero essere leggermente sovraespressi sulle cellule malate.
Il laboratorio Rice ha un approccio diverso. "Stavamo cercando altri tipi di biomarcatori oltre ai recettori cellulari presenti nei siti della malattia, " Suh ha detto. "Nel cancro al seno, Per esempio, è noto che le cellule tumorali secernono proteasi extracellulari, ma forse più importanti sono le cellule immunitarie infiltranti che migrano nel microambiente tumorale e iniziano a scaricare anche un sacco di proteasi.
"Quindi è quello che stiamo cercando di fare per una consegna mirata. La nostra idea di base è creare virus che, nella configurazione bloccata, non può fare nulla. sono inerti, " ha detto. Quando gli AAV programmati incontrano le giuste chiavi di proteasi nei siti della malattia, "questi virus sbloccano, si legano alle cellule e forniscono carichi utili che uccideranno le cellule per la terapia del cancro o forniranno geni che possono ripararle per altre applicazioni della malattia".
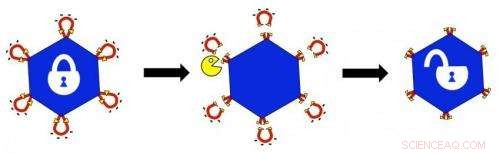
I virus adeno-associati modificati sviluppati alla Rice University sono "bloccati" da peptidi che rispondono alla presenza di due proteasi che potrebbero essere sovraespresse nel sito di tessuti cancerosi o altri tessuti malati. Le proteasi masticano i peptidi, sbloccando così il virus e permettendogli di consegnare il suo carico terapeutico. Credito:Junghae Suh/Rice University
Il laboratorio di Suh inserisce geneticamente peptidi negli AAV autoassemblanti per bloccare i capsidi, i gusci duri che proteggono i geni contenuti all'interno. Le proteasi bersaglio riconoscono i peptidi "e masticano i riccioli, "sbloccando efficacemente il virus e permettendogli di legarsi alle cellule malate.
"Se stessimo cercando solo una proteasi, potrebbe essere nel sito del cancro, ma potrebbe anche essere da qualche altra parte nel tuo corpo dove hai un'infiammazione. Questo potrebbe portare a effetti collaterali indesiderati, " ha detto. "Richiedendo due diverse proteasi - diciamo la proteasi A e la proteasi B - per aprire il virus bloccato, possiamo ottenere una maggiore specificità di somministrazione poiché la possibilità di avere entrambe le proteasi elevate in un sito si riduce".
Nel futuro, verranno utilizzati approcci di imaging molecolare per rilevare sia l'identità che la concentrazione di proteasi elevate. "Con queste informazioni, saremmo in grado di scegliere un dispositivo antivirus dal nostro gruppo di varianti ingegnerizzate che abbia le proprietà giuste per colpire quel sito di malattia. è lì che vogliamo andare, " lei disse.
Suh ha detto che le proteasi elevate si trovano intorno a molti tessuti malati. Ha suggerito che questi virus attivabili da proteasi possono essere utili per il trattamento non solo dei tumori ma anche delle malattie neurologiche, come l'ictus, Malattie di Parkinson e Alzheimer, e malattie cardiache, inclusi infarto miocardico e insufficienza cardiaca congestizia.
La visione finale di questa tecnologia è progettare virus in grado di eseguire una combinazione di passaggi per il targeting. "Per aumentare la specificità dello sblocco dei virus, puoi immaginare di creare virus che richiedono molte più chiavi per aprirsi, " ha detto. "Per esempio, potresti aver bisogno sia delle proteasi A e B che di un recettore cellulare per sbloccare il virus. Il lavoro qui riportato è un buon primo passo verso questo obiettivo".