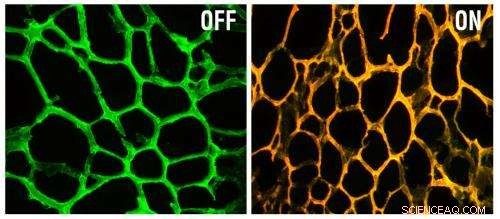
A sinistra c'è il nuovo nanodispositivo, costituito da un idrogel incorporato con nanoparticelle d'oro ricoperte di DNA mirato a un gene chiamato MRP-1. A destra, il dispositivo diventa fluorescente dopo aver incontrato la sequenza del gene bersaglio. Credito:per gentile concessione dei ricercatori
La chemioterapia spesso riduce i tumori all'inizio, ma poiché le cellule tumorali diventano resistenti al trattamento farmacologico, i tumori possono ricrescere. Un nuovo nanodispositivo sviluppato dai ricercatori del MIT può aiutare a superare questo problema bloccando prima il gene che conferisce la resistenza ai farmaci, lanciando poi un nuovo attacco chemioterapico contro i tumori disarmati.
Il dispositivo, che consiste di nanoparticelle d'oro incorporate in un idrogel che può essere iniettato o impiantato in un sito tumorale, potrebbe anche essere usato in modo più ampio per distruggere qualsiasi gene coinvolto nel cancro.
"Puoi prendere di mira qualsiasi marcatore genetico e consegnare un farmaco, compresi quelli che non implicano necessariamente percorsi di farmacoresistenza. È una piattaforma universale per la doppia terapia, "dice Natalie Artzi, un ricercatore presso l'Istituto per l'ingegneria e la scienza medica (IMES) del MIT, un assistente professore alla Harvard Medical School, e autore senior di un articolo che descrive il dispositivo nel Atti dell'Accademia Nazionale delle Scienze la settimana del 2 marzo.
Per dimostrare l'efficacia del nuovo approccio, Artzi e colleghi lo hanno testato su topi a cui era stato impiantato un tipo di tumore al seno umano noto come tumore triplo negativo. Tali tumori, che mancano di uno dei tre più comuni marcatori del cancro al seno:recettore degli estrogeni, recettore del progesterone, e Her2 sono generalmente molto difficili da trattare. Utilizzando il nuovo dispositivo per bloccare il gene per la proteina 1 multiresistente ai farmaci (MRP1) e quindi somministrare il farmaco chemioterapico 5-fluorouracile, i ricercatori sono stati in grado di ridurre i tumori del 90% in due settimane.
Superare la resistenza
MRP1 è uno dei tanti geni che possono aiutare le cellule tumorali a diventare resistenti alla chemioterapia. MRP1 codifica per una proteina che funge da pompa, eliminare i farmaci antitumorali dalle cellule tumorali e renderli inefficaci. Questa pompa agisce su diversi farmaci diversi dal 5-fluorouracile, compreso il farmaco antitumorale comunemente usato doxorubicina.
"La resistenza ai farmaci è un enorme ostacolo nella terapia del cancro e il motivo per cui la chemioterapia, in molti casi, non è molto efficace", dice João Conde, un postdoc IMES e autore principale del documento PNAS.
Per superare questo, i ricercatori hanno creato nanoparticelle d'oro rivestite con filamenti di DNA complementari alla sequenza dell'RNA messaggero MRP1, il frammento di materiale genetico che trasporta le istruzioni del DNA al resto della cellula.
Questi filamenti di DNA, che i ricercatori chiamano "nanobeacons, " si ripiegano su se stessi per formare una struttura a forcina chiusa. Tuttavia, quando il DNA incontra la corretta sequenza di mRNA all'interno di una cellula cancerosa, si dispiega e si lega all'mRNA, impedendogli di generare più molecole della proteina MRP1. Man mano che il DNA si dispiega, rilascia anche molecole di 5-fluorouracile che erano incorporate nel filamento. Questo farmaco poi attacca il DNA della cellula tumorale, poiché MRP1 non è più in giro per pomparlo fuori dalla cella.
"Quando mettiamo a tacere il gene, la cellula non è più resistente a quel farmaco, così possiamo consegnare il farmaco che ora riacquista la sua efficacia, "dice Condi.
Quando si verifica ciascuno di questi eventi, rilevando la proteina MRP1 e rilasciando 5-fluorouracile, il dispositivo emette fluorescenza di diverse lunghezze d'onda, permettendo ai ricercatori di visualizzare cosa sta succedendo all'interno delle cellule. A causa di ciò, le particelle potrebbero essere utilizzate anche per la diagnosi, in particolare, determinare se un determinato gene correlato al cancro è attivato nelle cellule tumorali.
Rilascio controllato del farmaco
Le nanoparticelle d'oro rivestite di DNA sono incorporate in un gel adesivo che rimane in posizione e ricopre il tumore dopo essere stato impiantato. Questa somministrazione locale delle particelle le protegge dalla degradazione che potrebbe verificarsi se fossero somministrate in tutto il corpo, e consente anche un rilascio prolungato di farmaci, dice Artzi.
Nei loro studi sui topi, i ricercatori hanno scoperto che le particelle potrebbero silenziare MRP1 fino a due settimane, con rilascio continuo del farmaco in quel periodo, riducendo efficacemente i tumori.
Questo approccio potrebbe essere adattato per fornire qualsiasi tipo di farmaco o terapia genica mirata a un gene specifico coinvolto nel cancro, dicono i ricercatori. Ora stanno lavorando per usarlo per silenziare un gene che stimola i tumori gastrici a metastatizzare ai polmoni.