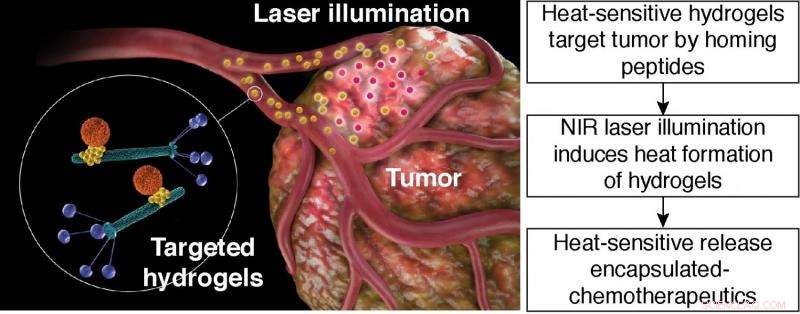
Rilascio termosensibile di chemioterapici incapsulati. Illustrazione schematica della terapia fototermica mirata con idrogel. Idrogel mirato:particella arancione, nanocarrier a base di liposomi; particella gialla, Nanoparticelle d'oro; bacchette verdi, particelle di batteriofagi con ligandi peptidici visualizzati sulla proteina di rivestimento dei fagi (blu). Credito:Hosoya, et al.
(Phys.org)—Le nanoparticelle funzionalizzate sono una via di somministrazione dei farmaci per i chemioterapici. Però, ottenere nanoparticelle per colpire il sito del tumore si è dimostrato difficile da fare. Un metodo che i ricercatori hanno usato per colpire le cellule cancerose è creare idrogel fatti di batteriofagi filamentosi (fagi) e nanoparticelle d'oro. I ligandi che legano i peptidi possono essere incorporati nella porzione fagica dell'idrogel che poi prenderà di mira le cellule di carcinoma note.
Un gruppo interdisciplinare di ricercatori provenienti da varie università del Giappone, gli Stati Uniti., e la Germania hanno sviluppato una piattaforma di idrogel in grado di colpire i tumori, fornire immagini non invasive, e rilasciare un farmaco chemioterapico. Hanno dimostrato la loro piattaforma sia in studi in vitro che in modelli murini. Inoltre, dimostrano che la loro piattaforma è generalizzabile a diversi target e chemioterapici. Il loro lavoro appare nel Atti dell'Accademia Nazionale delle Scienze .
Hosoya, La piattaforma di idrogel di et al. è costituita da batteriofagi, nanoparticelle d'oro, e vettori di dimensioni nanometriche come liposomi o particelle di silice mesopouree. In questa impostazione, le particelle fagiche sono in grado di riconoscere molecole specifiche sulle cellule tumorali. Le nanoparticelle d'oro fungono da "reporter" per la distribuzione dell'idrogel. Il nanocarrier trasporta vari prodotti chimici o merci farmaceutiche. Il nanocarrier rilascia il carico su uno stimolo specifico, come il calore.
Nel lavoro attuale, Hosoya, et al. ha dimostrato per la prima volta che i liposomi termosensibili (HSL) fungerebbero da formidabile vettore termosensibile. In teoria, mentre l'HSL inizia a sciogliersi, rilascia il farmaco che è incorporato in esso. Usando calceina, una molecola fluorescente attiva, hanno determinato che HSL rilascia calceina al raggiungimento di 40 o C, come previsto. Quando l'HSL è stato lasciato a una temperatura costante (42 o C), ha rilasciato tutta la calceina entro 10 minuti. Hosoya, et al. ha poi dimostrato che questi HSL erano ancora sensibili ai cambiamenti di temperatura quando incorporati nella piattaforma di idrogel.
Il passo successivo è stato dimostrare che gli idrogel contenenti HSL rispondevano al riscaldamento NIR mentre si trovavano all'interno di una matrice. Gli autori hanno utilizzato il gel di agarosio come sistema modello. Hanno scoperto che l'idrogel contenente HSL rispondeva al riscaldamento NIR e con l'aumentare della potenza del laser, la temperatura dell'idrogel è aumentata. Hanno quindi determinato se il riscaldamento NIR avrebbe innescato il rilascio di doxorubicina (dox), un chemioterapico. Sono stati in grado di produrre un "aumento dell'intensità di fluorescenza dipendente dalla dose di fotoni riproducibile e robusto".
Per determinare la distribuzione del calore nell'idrogel da NIR, hanno utilizzato la risonanza magnetica per immagini della temperatura sugli idrogel contenenti HSL sulla piattaforma di agarosio. Le immagini del gradiente termico hanno confermato che il calore centralizzato è stato prodotto dall'idrogel tramite il laser NIR. Hanno usato idrogel contenenti HSL incapsulati con gadolinio per confermare che il rilascio del farmaco si è verificato nella posizione del raggio laser.
Sebbene questi risultati mostrino che il rilascio del farmaco può essere controllato utilizzando il NIR, devono ancora verificare se il sistema può mirare al sito del cancro. Per fare questo, Hosoya, et al hanno incorporato un ligando che ha un peptide ciclico ben consolidato che si lega a CRKL. Le particelle fagiche che si legano al CRKL prendono di mira EF43. fgf-4 cellule di carcinoma mammario. Utilizzando idrogel contenenti HSL marcati con rodamina, hanno dimostrato che il fago ha preso di mira le cellule del carcinoma, confermando che mantiene ancora le sue proprietà vincolanti anche se incorporato nella nanopiattaforma.
Hanno quindi eseguito test in vivo sui topi. Hanno monitorato la posizione e gli effetti della loro piattaforma di idrogel contenente HSL nei topi che avevano EF43. fgf-4 carcinoma mammario. Studi di imaging a fluorescenza ottica hanno mostrato che il tumore era visibile nei topi trattati con il sistema di idrogel mirato rispetto ai controlli. L'analisi dei tumori dopo 24 ore ha rivelato che le nanoparticelle d'oro, fago mirato, e le HSL erano localizzate all'interno del tumore. Ulteriori studi per vedere se il loro sistema potrebbe quindi rilasciare un chemioterapico usando il NIR nel sito del tumore si sono rivelati efficaci. Gli autori hanno osservato una ridotta crescita del tumore nei topi con idrogel contenenti HSL con dox, e hanno confermato i loro risultati utilizzando modelli matematici.
Finalmente, per testare la versatilità della loro nanopiattaforma di idrogel, Hosoya, et al. incorporato nanoparticelle di silice mesoporosa (MSNP) nel sistema di idrogel. Le proprietà chimiche di MSNP consentono di confezionare diversi chemioterapici. Hanno testato se gli idrogel contenenti MSNP potrebbero fornire FITC in due diversi modelli di cancro, lo stesso modello di cancro al seno utilizzato in precedenza (EF43. fgf-4 ) e un modello per il cancro alla prostata. Hanno trovato un legame mirato con i due tumori e gli studi con il dox hanno mostrato una diminuzione delle dimensioni del tumore.
Questo lavoro dimostra una piattaforma di idrogel che non modifica le proprietà fisiche o chimiche di noti sistemi di nanocarrier come liposomi termosensibili o nanoparticelle di silice mesoporosa. Questa piattaforma consente il targeting, erogazione indotta dal calore, ed è sia versatile che riproducibile. Con ulteriori studi, questo sistema potrebbe essere un generale, metodo robusto per la somministrazione mirata di farmaci.
© 2016 Phys.org