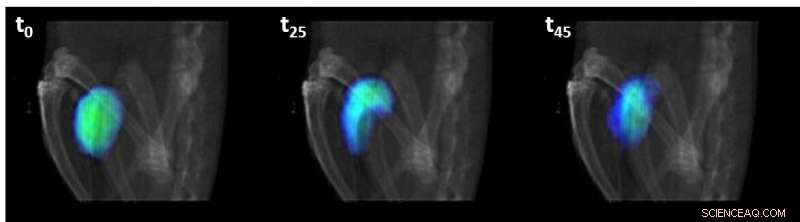
Imaging PET-TC ottenuto 0, 25 e 45 minuti dopo la consegna dei nanorobot in presenza di urea. Credito:Pedro Ramos, Cristina Simó / CIC biomaGUNE, IBEC, UAB
I nanobot sono macchine i cui componenti sono su scala nanometrica (un milionesimo di millimetro), e possono essere progettati in modo tale da avere la capacità di muoversi autonomamente nei fluidi. Nonostante siano ancora in fase di ricerca e sviluppo, si stanno compiendo progressi significativi verso l'uso dei nanorobot in biomedicina. Le loro applicazioni sono varie, dall'identificazione delle cellule tumorali al rilascio di farmaci in luoghi specifici del corpo. I nanorobot alimentati da enzimi catalitici sono tra i sistemi più promettenti perché sono completamente biocompatibili e possono fare uso di "carburanti" già disponibili nel corpo per la loro propulsione. Però, comprendere il comportamento collettivo di questi nanorobot è essenziale per avanzare verso il loro utilizzo nella pratica clinica.
Ora, in un nuovo studio pubblicato sulla rivista Robotica scientifica , ricercatori guidati dal professore di ricerca ICREA Samuel Sánchez e dal suo team "Smart Nano-Bio-Devices" presso l'Istituto di Bioingegneria della Catalogna (IBEC), insieme al gruppo Radiochemistry &Nuclear Imaging Lab del CIC biomaGUNE guidato da Jordi Llop e dall'Universitat Autònoma de Barcelona (UAB), sono riusciti a osservare in vivo il comportamento collettivo di un gran numero di nanorobot autonomi all'interno della vescica di topi viventi utilizzando l'etichettatura degli isotopi radioattivi.
"Il fatto di essere stati in grado di vedere come i nanorobot si muovono insieme, come uno sciame, e di seguirli all'interno di un organismo vivente, è importante, poiché milioni di loro sono necessari per trattare patologie specifiche come, Per esempio, tumori del cancro, "dice Samuel Sanchez, investigatore principale presso IBEC.
"Abbiamo dimostrato per la prima volta che i nanorobot possono essere monitorati in vivo attraverso la tomografia a emissione di positroni (PET), una persona molto sensibile, tecnica non invasiva utilizzata in ambiente biomedico, "dice Jordi Llop, ricercatore principale presso il laboratorio di radiochimica e imaging nucleare del CIC biomaGUNE.
Per fare questo, i ricercatori hanno prima condotto esperimenti in vitro, monitoraggio dei nanorobot tramite microscopia ottica e tomografia a emissione di positroni (PET). Entrambe le tecniche hanno permesso loro di osservare come le nanoparticelle si mescolavano con i fluidi ed erano in grado di migrare, collettivamente, seguendo percorsi complessi. I nanorobot sono stati quindi somministrati per via endovenosa a topi e, finalmente, introdotto nelle vesciche di questi animali. Poiché i nanorobot sono rivestiti con un enzima chiamato ureasi, che usa l'urea dell'urina come combustibile, nuotano collettivamente inducendo flussi di fluido all'interno della vescica.
Movimenti collettivi simili a stormi di uccelli o banchi di pesci
Il team di scienziati ha scoperto che la distribuzione dei nanodispositivi nella vescica dei topi era omogenea, il che indica che il movimento collettivo era coordinato ed efficiente. "I nanorobot mostrano movimenti collettivi simili a quelli che si trovano in natura, come uccelli che volano in stormi, o gli schemi ordinati che seguono i banchi di pesci, " spiega Samuel Sánchez, Professore di ricerca ICREA presso IBEC. "Abbiamo visto che i nanorobot che hanno ureasi sulla superficie si muovono molto più velocemente di quelli che non lo fanno. È, perciò, una prova di concetto della teoria iniziale che i nanorobot saranno in grado di raggiungere meglio un tumore e penetrarlo, "dice Jordi Llop, ricercatore principale presso CIC biomaGUNE.
Questo studio dimostra l'elevata efficienza di milioni di dispositivi nanoscopici per muoversi in modo coordinato in ambienti sia in vitro che in vivo, un fatto che costituisce un progresso fondamentale nella corsa dei nanorobot a diventare i protagonisti chiave di terapie e trattamenti altamente precisi. Le future applicazioni in medicina di questi dispositivi su nanoscala sono promettenti. È stato inoltre dimostrato "che il movimento di questi dispositivi può essere monitorato utilizzando tecniche di imaging che possono essere applicate all'ambiente in vivo, in altre parole, possono essere applicati negli animali da esperimento e offrono il potenziale per il trasferimento all'uomo, " dice Cristina Simò, uno dei primi autori dello studio e ricercatore nel gruppo CIC biomaGUNE.
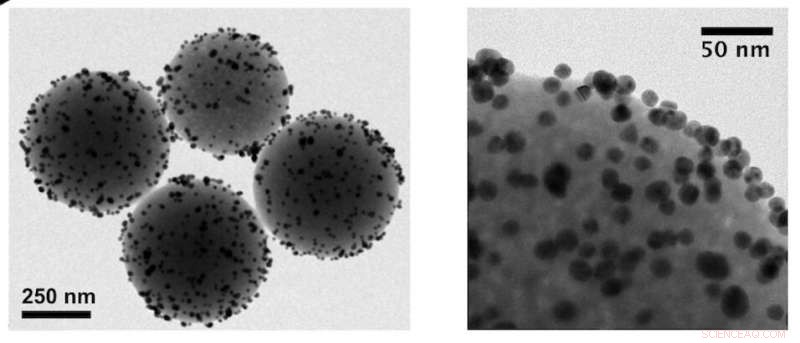
Le nanoparticelle sferiche avevano un diametro medio di 507,8 ± 3,4 nanometri e una distribuzione stocastica delle nanoparticelle d'oro sulla superficie. Credito:Hortelao et al., Sci. Robot. 6, eabd2823 (2021)
"Questa è la prima volta che siamo in grado di visualizzare direttamente la diffusione attiva di nanorobot biocompatibili all'interno di fluidi biologici in vivo. La possibilità di monitorare la loro attività all'interno del corpo e il fatto che mostrino una distribuzione più omogenea potrebbe rivoluzionare il nostro modo di intendere somministrazione di farmaci a base di nanoparticelle e approcci diagnostici, "dice Tania Patino, autore corrispondente dell'articolo.
Gli sciami di nanobot potrebbero essere particolarmente utili in mezzi viscosi, dove la diffusione dei farmaci è spesso limitata da una scarsa vascolarizzazione, come nel tratto gastrointestinale, l'occhio, o le articolazioni. "Infatti, poiché diversi enzimi possono essere incorporati nei minuscoli motori, i nanorobot potrebbero essere adattati in base alla parte all'interno dell'organismo, adattare il dispositivo al combustibile accessibile nell'ambiente in cui devono muoversi, " conclude il professor Sánchez.