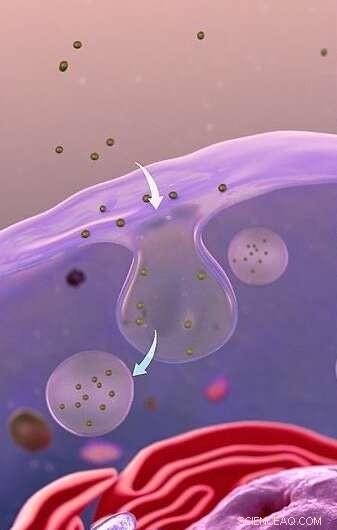
Per entrare in una cellula, le nanoparticelle possono essere inghiottite dalla membrana che circonda la cellula, formando vescicole simili a bolle:l'endocitosi. Credito:adattato da www.scientificanimations.com CC BY-SA 4.0
I nostri corpi hanno sviluppato barriere formidabili per proteggersi dalle sostanze estranee:dalla nostra pelle, alle nostre cellule e ogni componente all'interno delle cellule, ogni parte del nostro corpo ha strati protettivi. Queste difese, sebbene essenziali, rappresentano una sfida significativa per i farmaci e le terapie, come i vaccini, che devono superare molteplici barriere per raggiungere i loro obiettivi.
Sebbene queste barriere siano di vitale importanza nella scienza farmaceutica e nella progettazione di farmaci, molto è ancora sconosciuto su di esse e su come superarle.
In uno studio recente, i ricercatori della Xi'an Jiaotong-Liverpool University e della Nanjing University in Cina, e della Western Washington e della Emory University negli Stati Uniti, hanno fatto luce sul motivo per cui la somministrazione di farmaci alle cellule può essere così difficile.
Superare le barriere
Con i vaccini COVID-19, a cui sono stati iniettati centinaia di milioni di persone, l'mRNA deve essere racchiuso all'interno di bolle di grasso protettive - nanoparticelle lipidiche - in modo che possa passare attraverso le difese del corpo e raggiungere l'obiettivo previsto nelle nostre cellule.
Alcuni tipi di cellule, come le cellule staminali, le cellule immunitarie e le cellule nervose, hanno barriere particolarmente difficili da superare, quindi il rilascio di particelle in queste cellule è ancora più impegnativo.
Nello studio, pubblicato sulla rivista ACS Nano , i ricercatori hanno combinato tecniche di microscopia all'avanguardia per monitorare la consegna di nanoparticelle, che sono spesso utilizzate per la somministrazione di farmaci, nelle cellule staminali in tempo reale.
I loro risultati suggeriscono che, in alcuni tipi di cellule, le nanoparticelle vengono "intrappolate" all'interno di vescicole simili a bolle e quindi viene impedito di raggiungere l'obiettivo previsto.
Il team ha utilizzato le loro scoperte per creare un modello matematico in grado di prevedere quanto sarà efficiente la consegna di nanoparticelle nelle cellule e aiutare la progettazione di future terapie.
Il Dr. Gang Ruan, un corrispondente autore dello studio, afferma:"Abbiamo suddiviso il processo di consegna delle particelle nelle cellule in singoli passaggi, in modo da poter visualizzare ogni passaggio e creare una finestra sui meccanismi utilizzati da queste cellule per proteggersi .
"Per progettare metodi di somministrazione migliorati per le terapie, abbiamo bisogno di una comprensione quantitativa di come interagiscono parti della cellula e le nanoparticelle. Come disse una volta un grande bioingegnere che conoscevo, se dovessi progettare un aeroplano, dovresti analizzare l'aerodinamica di ogni parte prima di costruire l'aereo.
"Trovando il collo di bottiglia nella consegna di nanoparticelle nelle cellule, i nostri risultati apriranno la strada a terapie più mirate e innovative che utilizzano la consegna su misura, potenzialmente per i singoli pazienti".
In consegna
In precedenza, l'imaging del rilascio di nanoparticelle nelle cellule era limitato a causa della velocità rapida e della piccola scala richieste. Tuttavia, il team multidisciplinare è stato in grado di utilizzare i diversi campi di competenza per creare modi innovativi per superare questi ostacoli. Hanno combinato due tipi di analisi al microscopio, precedentemente utilizzate solo separatamente, per consentire loro di studiare l'intero processo di consegna.
Xuan Yang, che condivide la paternità principale dello studio con il dottor Xiaowei Wen, afferma:"Siamo stati in grado di tracciare il movimento delle nanoparticelle pixel per pixel, in tempo reale, e quindi visualizzare il movimento delle nanoparticelle attraverso barriere di membrana e quando sono entrati in ogni compartimento delle cellule staminali".
Sebbene il processo di consegna delle nanoparticelle in queste cellule sia complesso e composto da diversi meccanismi, visualizzando e quindi modificando chimicamente ogni fase del processo, il team ha identificato la fase critica che impedisce la consegna delle nanoparticelle ai loro bersagli cellulari.
Per entrare in una cellula, le nanoparticelle possono essere inghiottite dalla membrana che circonda la cellula, formando vescicole simili a bolle. In molti tipi cellulari, le nanoparticelle sfuggirebbero da queste bolle una volta all'interno della cellula. Tuttavia, in alcune cellule extra-protette, come le cellule staminali utilizzate in questo studio, le nanoparticelle sembrano rimanere intrappolate all'interno delle vescicole e non sono in grado di fuggire. Ciò significa che non possono entrare nella cella e raggiungere il loro obiettivo.
I ricercatori combinano le loro osservazioni e analisi in un modello matematico in grado di prevedere l'efficienza e la rapidità con cui le particelle passerebbero attraverso ogni fase della consegna ed entrerebbero in una cellula.
"Il nostro modello può essere utilizzato per prevedere quale sarà la concentrazione delle nanoparticelle, in una particolare posizione nella cellula, in un determinato momento", afferma il dott. Wen.
"Il metodo generale di questo modello può essere utilizzato per incorporare diversi tipi di nanoparticelle e cellule per comprendere meglio i meccanismi di consegna utilizzati per passare nelle cellule. Ad esempio, prevedere quanto bene le nanoparticelle lipidiche nei vaccini COVID-19 consegneranno l'mRNA in una cellula ."
Il dottor Steven Emory, che è anche un corrispondente autore dello studio, aggiunge:"Essere in grado di mappare le diverse componenti e i meccanismi interni che compongono i percorsi di consegna in tempo reale porta a capire come controllare questi percorsi. Ciò potrebbe apri alcune cose davvero eccitanti in termini di terapia.
"Ci auguriamo che i nostri nuovi strumenti e la nostra comprensione abbiano creato un punto d'appoggio iniziale per il sistema, da dove noi e altri ricercatori possiamo iniziare a scalare e iniziare a esplorare". + Esplora ulteriormente