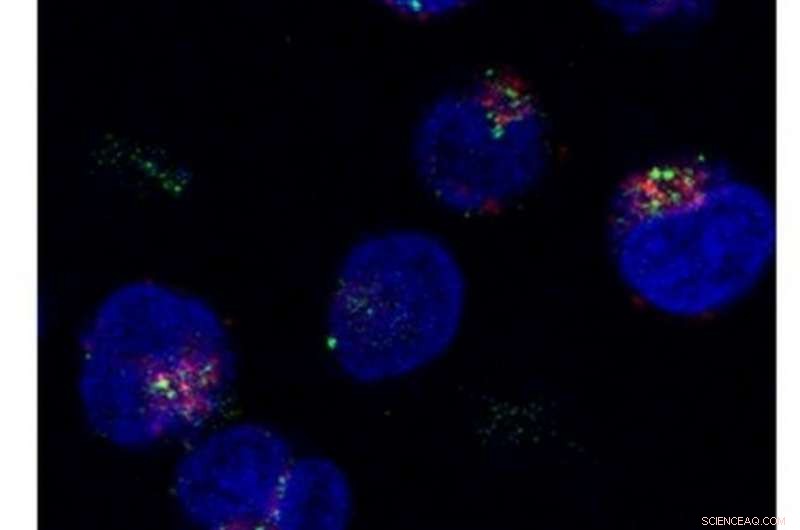
Imaging microscopico dettagliato che mostra la distribuzione intracellulare dei dendrimeri modificati con Phe e CHex carbossi-terminali nelle cellule T. Credito:Chie Kojima, Università della Prefettura di Osaka
I linfociti T, noti anche come linfociti, hanno ruoli importanti in varie reazioni immunitarie. Tuttavia, ci sono solo pochi rapporti sui sistemi di consegna nei linfociti T.
La professoressa associata Chie Kojima e i suoi colleghi del Dipartimento di Chimica Applicata, Graduate School of Engineering, Osaka Prefecture University (OPU), collaborando con il Professor Ikuo Fujii e Ikuhiko Nakase del Dipartimento di Scienze Biologiche, Graduate School of Science, OPU, si sono esibiti uno studio sperimentale che costruisce un sistema di rilascio sensibile al pH nelle cellule T e nei loro sottoinsiemi utilizzando dendrimeri carbossi-terminali (molecole polimeriche ramificate altamente ordinate) contenenti fenilalanina (Phe) e anidride dell'acido idrofobico (anidride cicloesandicarbossilica, CHex), come PAMAM- CHex-Phe e PAMAM-Phe-CHex. Questi dendrimeri hanno mostrato una maggiore associazione con le cellule T derivate dagli splenociti, il che suggerisce che l'effetto idrofobico influenza significativamente l'associazione dei dendrimeri con le cellule immunitarie.
L'associazione delle cellule T di questi dendrimeri è stata esaminata a pH e temperature diversi utilizzando l'ordinamento cellulare attivato dalla fluorescenza, in cui sono stati utilizzati splenociti murini colorati con un anticorpo anti-CD3. Insieme a questo, l'associazione di PAMAM-CHex-Phe e PAMAM-Phe-CHex con alcune linee cellulari di coltura e sottoinsiemi di cellule T, come cellule T helper CD4-positive (CD3+CD4+), cellule T killer CD8- positive (CD3 Sono stati esaminati anche +CD8+) e cellule T attivate (CD3+CD69+). Al fine di confermare l'internalizzazione di questi dendrimeri nei linfociti T, Assoc. La prof.ssa Kojima e i suoi collaboratori hanno utilizzato l'imaging microscopico confocale per osservare la distribuzione intracellulare di PAMAM-CHex-Phe e PAMAM-Phe-CHex.
Assoc. Il Prof. Kojima afferma che "sebbene i linfociti T svolgano ruoli importanti in varie reazioni immunitarie, ci sono solo pochi rapporti sui sistemi di rilascio nei linfociti T. In questo studio, abbiamo applicato i dendrimeri Phe-modificati a un sistema di rilascio di farmaci sensibile al pH in Cellule T. Sono stati sintetizzati dendrimeri con diversi aminoacidi e anidridi acide ed è stata studiata la loro associazione sensibile al pH con le cellule T e i loro sottoinsiemi".
Questo studio sperimentale dell'Assoc. Il Prof. Kojima ei suoi collaboratori hanno presentato con successo i risultati in termini di a) Sintesi e sensibilità al pH dei dendrimeri carbossi-terminali portatori di Phe; b) associazione pH-reattiva dei dendrimeri carbossi-terminali recanti Phe con cellule T e sottoinsiemi di cellule T comprendenti cellule T attivate; c) Interiorizzazione di PAMAM-Phe-CHex e PAMAM-CHex-Phe in cellule T.
Conclude che i loro "risultati hanno mostrato che i dendrimeri modificati con Phe e CHex hanno un potenziale di consegna ai linfociti T e ai loro sottoinsiemi. Questo giocherà un ruolo chiave nell'immunoterapia del cancro".
Nell'immunoterapia del cancro è necessaria l'attivazione delle cellule T helper residenti nei linfonodi e delle cellule T killer, nonché la soppressione delle cellule T regolatorie localizzate nei tessuti tumorali. Quindi, in base alle proprietà reattive al pH, i risultati (dendrimeri) ottenuti da Assoc. La prof.ssa Kojima ei suoi collaboratori sono importanti per lo sviluppo di nanopiattaforme per la consegna diretta ai linfociti T per controllare le funzioni dei linfociti T, utili per l'immunoterapia del cancro.
L'articolo è stato pubblicato nel Journal of Materials Chemistry B . + Esplora ulteriormente