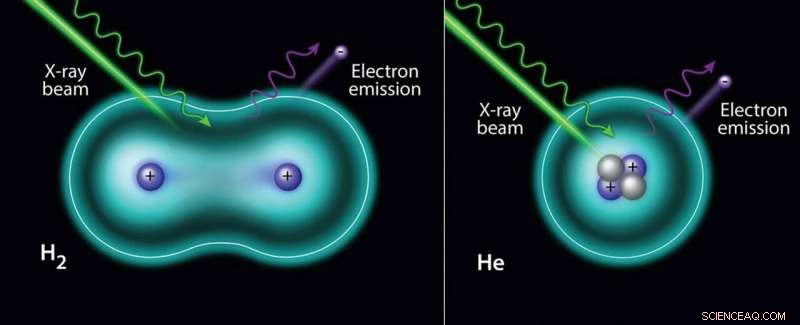
Il raggio di raggi X induce la foto-espulsione di un elettrone dall'idrogeno (a sinistra) e dall'elio (a destra). Credito:Dipartimento dell'Energia degli Stati Uniti
Per la prima volta gli scienziati hanno misurato la struttura vibrazionale degli atomi di idrogeno ed elio mediante raggi X. I risultati smentiscono l'idea sbagliata che sia impossibile ottenere spettri di spettroscopia fotoelettronica a raggi X (XPS) di idrogeno ed elio, i due elementi più leggeri della tavola periodica. Si pensava che questo fosse il caso a causa delle basse probabilità di espulsione di elettroni da questi elementi indotte dai raggi X.
L'ineguagliabile luminosità del fascio della National Synchrotron Light Source-II aumenta significativamente la probabilità che un fotone entri in collisione con un atomo di gas a pressioni ambientali. La linea di luce consente di utilizzare XPS per studiare direttamente i due elementi più abbondanti nell'universo.
Anche, questo lavoro aiuta a descrivere i limiti di XPS, aprendo un ambito più ampio per una delle tecniche più utili nella scienza dei materiali.
La spettroscopia fotoelettronica a raggi X (XPS) è una delle tecniche più potenti nella scienza dei materiali. Però, la letteratura è piena di affermazioni che affermano che è impossibile utilizzare XPS per studiare i due elementi più leggeri e più abbondanti nell'universo, idrogeno ed elio.
Questo lavoro ha dimostrato che gli spettri fotoelettronici a raggi X a pressione ambiente di idrogeno ed elio possono essere ottenuti quando viene utilizzata una sorgente di raggi X sufficientemente luminosa, come alla National Synchrotron Light Source II.
Nel caso del gas elio, lo spettro mostra un picco simmetrico dal suo unico orbitale. Nel caso di molecole di gas idrogeno, si osserva un picco asimmetrico, che è legato ai diversi possibili modi vibrazionali dello stato finale. La struttura vibrazionale della molecola di idrogeno è evidente nell'H 2 spettro 1s.