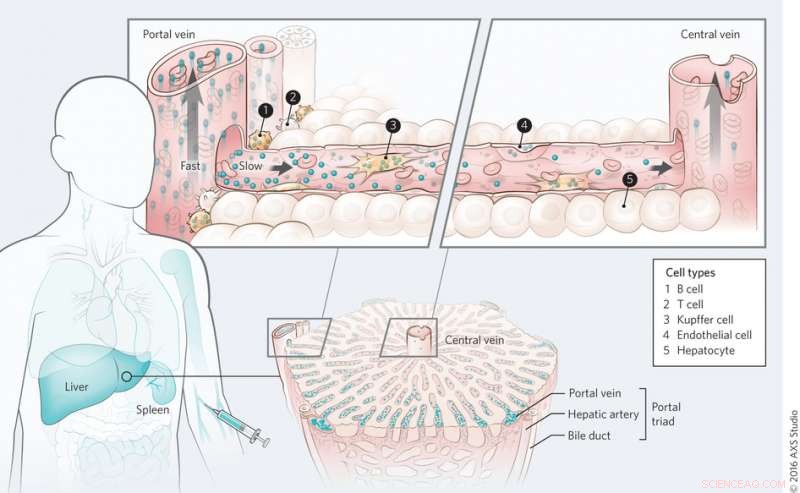
Meccanismo di trasporto dei nanomateriali nel fegato. Credito:(c) Kim M. Tsoi, et al. Materiali della natura (2016) doi:10.1038/nmat4718
(Phys.org)—Una delle maggiori sfide per realizzare il potenziale delle terapie mirate è impedire ai nanomateriali di accumularsi nel fegato o nella milza. Il fegato e la milza fanno parte del sistema dei fagociti mononucleati. Il suo compito è quello di filtrare le tossine dal flusso sanguigno. Sfortunatamente, nel fare il suo lavoro, impedisce anche alle nanoterapie di raggiungere il loro obiettivo.
Per superare questo ostacolo un gruppo di ricercatori di diverse istituzioni di Toronto ha condotto calcoli a livello di organo e sub-organo, in vitro, e studi in vivo utilizzando punti quantici, nanoparticelle d'oro, e nanoparticelle di silice per comprendere meglio il sistema dei fagociti mononucleari e il meccanismo con cui vengono sequestrate le nanoparticelle. Hanno scoperto che la velocità del flusso sanguigno, fenotipo cellulare, e la posizione fisica nel fegato giocano tutti un ruolo nell'assorbimento delle nanoparticelle. Suggeriscono che il lavoro futuro dovrebbe riguardare non solo la progettazione di nanoparticelle, ma una specie di precondizionamento del fegato. Il loro lavoro appare in Materiali della natura .
Le nanoparticelle possono essere funzionalizzate in modo tale che la particella colpisca un particolare tipo di cellula. Questo è molto promettente per il cancro e altre terapie mirate. Però, quando le nanoterapie vengono testate nel corpo, la nanoparticella viene eliminata dal flusso sanguigno tramite il sistema dei fagociti mononucleati (MPS). Questo vale per tutti i tipi di nanoparticelle.
Tsoi, et al. ha condotto analisi di organi interi e sub-organi per comprendere meglio come il sistema MPS sequestra le nanoparticelle. Per i loro esperimenti, si sono concentrati su nanoparticelle "dure" non degradabili:punti quantici, nanoparticelle d'oro, e nanoparticelle di silice.
A livello dell'intero organo, Tsoi, et al. scoperto che i punti quantici vengono prima cancellati dalle cellule vicino alla triade portale e che c'è un gradiente di clearance attraverso la sinusoide epatica durante il primo passaggio. Il sangue scorre nel fegato attraverso la triade portale ed esce attraverso la vena centrale. Ciò è stato osservato anche con nanoparticelle d'oro indipendentemente dalla funzionalizzazione della superficie, anche se l'adsorbimento delle proteine sembrava svolgere un ruolo nell'assorbimento delle nanoparticelle.
La prossima area di indagine è se la velocità del flusso sanguigno gioca un ruolo nel sequestro delle nanoparticelle. Il flusso sanguigno rallenta una volta che colpisce il fegato (da 10-100 cm s -1 a 200-800 μm s -1 ). Tsoi, et al. ha sviluppato un modello matematico per descrivere il flusso sanguigno all'interno del fegato e la probabilità di sequestro di nanoparticelle. Hanno quindi confrontato i loro risultati computazionali con i risultati degli studi di citometria con i ratti che sono stati trattati con punti quantici nel test per l'accumulo di nanoparticelle. In particolare, mentre l'avvezione è l'influenza dominante sul flusso sanguigno nel corpo, la diffusione è l'influenza dominante nel fegato. Hanno scoperto che il fegato era 10 2 a 10 3 volte più probabilità di sequestrare i nanomateriali e che la dimensione delle particelle ha avuto un ruolo:più grande è la particella, più è probabile che sia stato assorbito dal fegato.
A livello di sub-organo, Tsoi, et al. ha esaminato quali tipi di cellule svolgono il ruolo più importante nell'assorbimento delle nanoparticelle. Gli studi per determinare l'assorbimento cellulare dei punti quantici hanno mostrato che le cellule di Kupffer hanno adsorbito il maggior volume di punti quantici, come previsto. Però, ciò che è stato sorprendente è stato il numero di particelle interiorizzate dai linfociti B. Le cellule B sembrano svolgere un ruolo molto più importante nell'assorbimento delle nanoparticelle di quanto si pensasse una volta, sebbene le cellule di Kupffer siano ancora le cellule chiave nella rimozione delle nanoparticelle. Altri tipi di cellule, comprese le cellule endoteliali, ha anche svolto un ruolo nella rimozione delle nanoparticelle.
Prossimo, Tsoi, et al. hanno testato se l'architettura degli organi influisce sull'assorbimento delle nanoparticelle nel fegato studiando il processo di sequestro nella milza. Hanno scoperto che delle nanoparticelle che sono state rimosse dalla milza, quasi tutti si trovavano nella regione della polpa rossa. È qui che il flusso sanguigno diminuisce rispetto al flusso in tutto il corpo. Mentre alcune nanoparticelle risiedevano nella milza, i macrofagi della milza hanno internalizzato meno nanoparticelle rispetto alle cellule di Kupffer all'interno del fegato. Ciò è stato confermato da studi comparativi in vitro e in vivo, e dimostra che il tipo di cellula dell'architettura d'organo gioca un ruolo nell'assorbimento delle nanoparticelle.
Questa ricerca fornisce importanti spunti su come superare l'assorbimento di nanoparticelle da parte dell'MPS. In genere i ricercatori si concentrano sulla progettazione delle nanoparticelle, ma questo studio suggerisce che l'ambiente corporeo gioca un ruolo importante nel sequestro delle nanoparticelle. Gli autori suggeriscono di manipolare l'ambiente ospite come strategia complementare all'ottimizzazione delle nanoparticelle. I test preliminari mostrano che due possibili strade stanno cambiando la velocità del flusso sanguigno attraverso il fegato e cambiando il fenotipo di alcune cellule in modo che non siano inclini all'assorbimento di nanomateriali.
© 2016 Phys.org