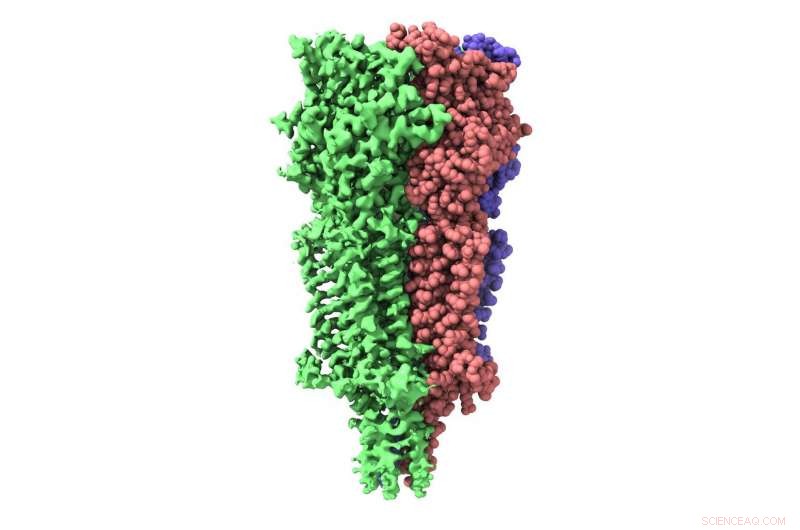
Vista generale del recettore 5-HT3, che è composto da 5 subunità. Credito:Hugues Nury, IBS/CNRS/ESRF
A novembre 2017, un microscopio crioelettronico Titan Krios (cryo-EM) è stato inaugurato all'ESRF, il sincrotrone europeo, Francia. I dati raccolti su questa funzionalità cryo-EM in a Natura pubblicazione che descrive il ciclo di attivazione di un recettore della serotonina preso di mira da farmaci contro la nausea indotta da chemioterapia e radioterapia.
Grazie a cryo-EM, i ricercatori possono ora congelare le biomolecole in azione, comprese proteine di membrana molto importanti in diverse conformazioni, e visualizzare ciascuno di questi a risoluzione atomica. Cryo-EM consente quindi ai ricercatori di produrre istantanee che rivelano la dinamica delle proteine quando interagiscono con altre molecole, informazioni che sono cruciali sia per una comprensione di base della chimica della vita che per lo sviluppo dei farmaci.
La ricerca in Natura è il risultato di una collaborazione internazionale di scienziati dell'Istituto di biologia strutturale (unità di ricerca mista IBS CEA-CNRS-Università Grenoble Alps), l'Istituto Pasteur, l'Università della Lorena (Francia), l'Università di Copenaghen (Danimarca), l'Università dell'Illinois (USA) e la società di biotecnologie Theranyx. Il focus della carta, con i dati dell'ESRF cryo-EM, è il ciclo di attivazione del recettore 5-HT3, appartenente alla famiglia dei recettori della serotonina. Questi recettori sono ben noti per influenzare processi biologici e neurologici come ansia, appetito, umore, nausea, sonno e termoregolazione, tra gli altri. A differenza degli altri recettori della serotonina, che sono recettori accoppiati a proteine G, 5-HT3 è un canale ionico dipendente dal neurotrasmettitore e cambia la sua conformazione durante l'attivazione. È presente nel cervello, così come nel sistema nervoso enterico, il sistema nervoso periferico che guida il tratto digestivo.
5-HT3 è un obiettivo per i farmaci e le aziende farmaceutiche lo hanno studiato a lungo. Quando i pazienti sono sottoposti a chemioterapia e/o radioterapia, spesso soffrono di nausea e vomito come effetti collaterali. Infatti, le sostanze chimiche utilizzate nel trattamento del cancro innescano un aumento della segnalazione della serotonina, che a sua volta attiva 5-HT3 per aprire il suo canale ionico, che poi provoca nausea.
"Il recettore è stato ampiamente studiato per la sua importanza, ma non è stato fino a poco tempo che vi abbiamo avuto accesso su scala atomica, grazie alla criomicroscopia elettronica, tra le altre tecniche, " spiega Hugues Nury, autore principale dell'articolo e scienziato del CNRS presso l'IBS.
I risultati pubblicati in Natura mostrano il recettore 5-HT3 in quattro diverse conformazioni. Le immagini di tre di questi sono state ottenute presso il Center for Cellular Imaging and Nano Analytics in Svizzera, mentre il quarto, che finalmente ha permesso una piena comprensione del meccanismo di attivazione di 5-HT3, è stato ottenuto presso l'ESRF. Una delle conformazioni è inibita grazie al legame di farmaci antinausea e antivomito ampiamente utilizzati in chemioterapia. Le immagini ottenute del recettore possono quindi portare alla progettazione di farmaci antinausea più efficaci per il trattamento di pazienti sottoposti a terapia per tumori.
"Questi risultati contribuiscono alla nostra conoscenza su come si comportano i recettori 5-HT3. Forniscono un quadro per la miriade di mutazioni descritte in letteratura:ora possiamo guardare dove sono, quali sono i movimenti in queste zone, e talvolta perché le mutazioni hanno alterato la funzione del recettore. Ora vediamo anche le tasche di rilegatura in dettagli inediti, che può aiutare lo sviluppo di farmaci futuri, " spiega Hugues Nury.