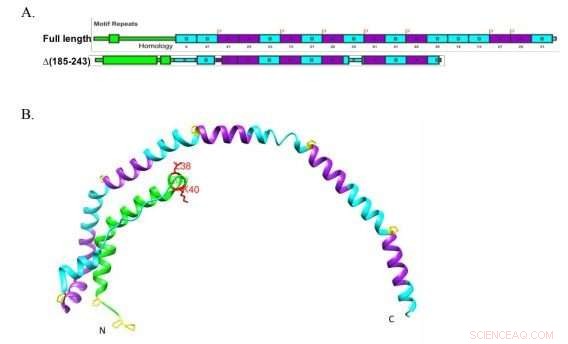
I ricercatori della Boston University hanno utilizzato una versione troncata di Apolipoprotein A-I, mostrato qui, determinare in modo definitivo che la proteina deve legarsi al trasportatore lipidico ABCA1 per iniziare a formare lipoproteine ad alta densità, le particelle di "colesterolo buono" che trasportano il colesterolo al fegato per lo smaltimento. Credito:Liu et al. JLR 2018
Olio e acqua non si mescolano. Ma il nostro sangue acquoso è pieno di diversi tipi di lipidi idrofobici, compreso il colesterolo. Per viaggiare attraverso il flusso sanguigno, quei lipidi devono fare l'autostop su un portatore anfipatico. In un recente articolo in Journal of Lipid Research , gli scienziati della Boston University segnalano un progresso nella nostra comprensione meccanicistica di come si forma uno di questi vettori.
"Le lipoproteine sono come barche che trasportano e rimuovono carichi di sostanze grasse da e verso le nostre cellule, "ha detto David Atkinson, presidente del dipartimento di fisiologia e biofisica presso la Boston University School of Medicine e autore senior della JLR carta.
Il sottoinsieme di quelle "barche" che trasportano il colesterolo e altri lipidi al fegato da altre parti del corpo sono chiamate lipoproteine ad alta densità (HDL, alias "colesterolo buono"). L'HDL può rimuovere il colesterolo dalle cellule distali, come i macrofagi nelle pareti delle arterie, dove l'accumulo di colesterolo può portare ad attacchi di cuore e consegnarlo alle cellule del fegato, un processo noto come trasporto inverso del colesterolo. Il fegato smaltisce il colesterolo in eccesso convertendolo in acidi biliari secreti nell'intestino tenue.
Secondo Atkinson, un biofisico, la maggior parte di ciò che si sa sulla formazione di HDL proviene da esperimenti che prendono una virata biologica cellulare. In questi tipi di studi, Egli ha detto, "Puoi vedere (formazione HDL) accadere, e puoi quantificare cosa succede, ma non capisci le interazioni di guida che lo fanno accadere. È qui che si concentra la mia ricerca".
Le particelle HDL sono costruite su una proteina impalcatura chiamata apolipoproteina A-I (apoA-I). Si pensa che l'ApoA-I raccolga colesterolo e fosfolipidi dalla membrana cellulare. Atkinson e il suo team volevano capire meglio come funziona quel processo.
ApoA-I dipende da una proteina trasportatrice lipidica, chiamato ABCA1, che pompa il colesterolo dal lembo interno a quello esterno della membrana cellulare. Poiché il colesterolo che ABCA1 trasferisce di solito finisce per essere legato all'apoA-I, alcuni ricercatori sospettavano che ci fosse un'interazione fisica tra apoA-I e ABCA1. Nel frattempo, altri hanno sostenuto che colesterolo e fosfolipidi potrebbero altrettanto bene diffondersi passivamente e legarsi all'apoA-I. E gli esperimenti disponibili, la maggior parte dei quali era basata sulla reticolazione, non ha risolto il dibattito.
"Anche se dimostri che l'apoA-I si lega alla superficie cellulare, in realtà non sai che è legato ad ABCA1. È solo legato alla superficie cellulare, " Ha spiegato Atkinson. Quindi ha chiesto al suo team di vedere se potevano "dimostrare che l'interazione sta effettivamente accadendo nei componenti isolati".
Il gruppo, guidato dallo studente laureato Minjing Liu, e supportato dal Dr. Xiaohu Mei e dal Dr. Haya Herscovitz, utilizzato apoA-I isolato e ABCA1 per testare un'interazione fisica. Sono stati in grado di mostrare l'immunoprecipitazione dell'apoA-I con ABCA1 purificato.
Il laboratorio aveva precedentemente progettato un mutantapoA-I con un piccolo movimento in più in una regione di cerniera già flessibile. Per questo studio, hanno usato il mutante per dimostrare che una maggiore flessibilità aumenta la lipidazione dell'apoA-I, o la formazione di HDL nascente. Il team non ha ancora testato se il mutante extra-flessibile si leghi meglio ad ABCA1 o se il legame di una delle due forme di apoA-I attivi ABCA1.
Ma su una cosa, Atkinson è certo. "È l'interazione ApoA-I/ABCA1 che consente quindi la formazione di particelle HDL nascenti mentre i componenti della membrana vengono trasportati fuori da ABCA1, " ha detto Atkinson.
L'aumento del trasporto inverso del colesterolo potrebbe un giorno essere un modo per ridurre l'aterosclerosi e le malattie cardiache. Atkinson è ottimista sulla promessa di comprendere meglio i processi fisiologici. "La ricerca traslazionale potrebbe essere in voga, ma ricorda che se non fai ricerche fondamentali sulla scoperta di base, non avrai niente da tradurre, " Egli ha detto.