Le molecole d'acqua legate più vicine al minerale hanno una struttura rigida, struttura simile al ghiaccio e non può muoversi in disposizioni che consentono reazioni chimiche. Le molecole d'acqua più lontane dalla superficie del minerale hanno un minor vincolo, struttura simile a un liquido e può organizzarsi per promuovere la reattività. Credito:Laboratorio di scienze molecolari ambientali
Un team di ricercatori guidati dallo scienziato computazionale del PNNL Simone Raugei ha rivelato nuove intuizioni su come questo complesso enzima svolge il suo lavoro, scoprendo che la formazione apparentemente dispendiosa di idrogeno ha uno scopo essenziale. La loro carta, "L'analisi computazionale critica illumina il meccanismo di eliminazione riduttiva che attiva la nitrogenasi per N 2 riduzione, " è stato pubblicato nel Atti dell'Accademia Nazionale delle Scienze nel novembre 2018. I coautori di Raugei sono Lance Seefeldt, che detiene un incarico congiunto presso PNNL e Utah State University, e Brian Hoffman della Northwestern University.
La nitrogenasi può convertire l'azoto in ammoniaca a temperatura ambiente e pressione atmosferica. Industria, d'altra parte, si affida al processo Haber-Bosch, una tecnica secolare che utilizza alte temperature e pressioni. I combustibili fossili in genere forniscono l'energia per questo processo, ecco perché la produzione industriale di ammoniaca da sola rappresenta oltre l'1% delle emissioni totali di carbonio legate all'energia del mondo. Capire cosa conferisce alla nitrogenasi il suo muscolo che spezza i legami può portare a nuovi, idee stimolanti per la progettazione di catalizzatori sintetici per produrre ammoniaca.
Per ogni molecola di azoto trasformata in ammoniaca, la nitrogenasi produce almeno una molecola di idrogeno (H 2 ), che è "uno dei misteri più enigmatici della nitrogenasi, " ha detto Raugei. "Invece di produrre solo ammoniaca, produci anche questo sottoprodotto. Perché è necessario?"
I ricercatori hanno scoperto che questo fenomeno aiuta effettivamente la nitrogenasi ad affrontare i forti legami dell'azoto. "La natura ha trovato una soluzione accoppiando la produzione di idrogeno, che sprigiona energia, con scissione di azoto, che richiede energia, " Ha detto Raugei. "E 'l'equilibrio totale."
Per arrivare ai risultati, il team ha utilizzato una combinazione di metodi teorici e sperimentali. Raugei ha condotto calcoli di chimica quantistica su modelli del nucleo dell'enzima, basandosi sulla guida di Seefeldt e Hoffman, che sono esperti sulla biochimica della nitrogenasi. I loro dati sperimentali hanno aiutato a informare i calcoli, e viceversa.
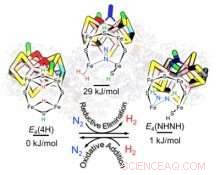
I ricercatori si sono concentrati sul nucleo catalitico della nitrogenasi, composto da ferro, molibdeno e zolfo (FeMo-co). Durante l'evento catalitico, quando FeMo-co ha acquisito un numero critico di elettroni e protoni (H+) sotto forma di due idruri a ponte (Fe-H-Fe) nella sua fascia periferica, generazione di un H 2 legato a FeMo-co e suo spostamento di N 2 fornisce il dare e avere di energia per innescare la riduzione dell'azoto, i ricercatori hanno scoperto.
"Eravamo molto ben posizionati per raggiungere questa svolta perché abbiamo combinato le informazioni sperimentali sulla nitrogenasi con le informazioni computazionali, " Disse Raugei. "Quella era la chiave."
I ricercatori cercano di estendere la ricerca esaminando i dettagli fini dell'accumulo di elettroni e protoni nel sito attivo della nitrogenasi ed esattamente come l'N 2 legame è rotto per formare ammoniaca.