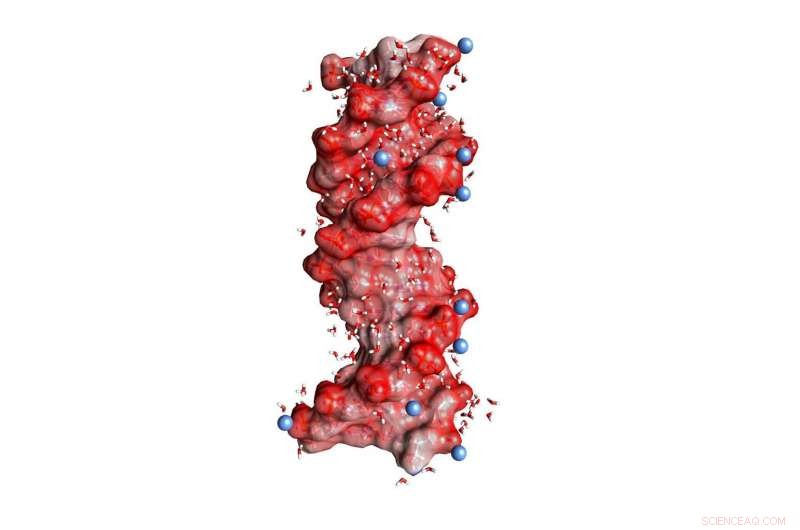
Fig. 1:Doppia elica del DNA immersa nell'acqua (piccole molecole angolate, non in scala). Le sfere rosso scuro sulla superficie dell'elica rappresentano gli atomi di ossigeno delle unità PO2 caricate negativamente, le sfere blu caricano positivamente gli ioni nell'ambiente. Credito:MBI Berlino
Coppie di gruppi fosfato caricati negativamente e ioni magnesio positivi rappresentano una caratteristica strutturale chiave del DNA e dell'RNA incorporati nell'acqua. Le vibrazioni dei gruppi fosfato sono state ora stabilite come sonde selettive di tali coppie di contatto e consentono una mappatura delle interazioni e della struttura sulle scale temporali ultraveloci della dinamica molecolare.
DNA e RNA sono polimeri carichi che codificano le informazioni genetiche in una struttura a doppia elica e agiscono come attori chiave nella biosintesi delle proteine. Le loro cariche negative si trovano nella spina dorsale molecolare, che consiste di fosfato ionico (PO 2- ) e dei gruppi zuccherini (Figura 1). La stabilizzazione delle strutture macromolecolari di DNA e RNA richiede una compensazione di forti forze elettriche repulsive tra i gruppi fosfato ugualmente carichi da parte di ioni opposti, cioè., Carica positiva. In tale contesto, magnesio (Mg 2+ ) sono particolarmente importanti in quanto non solo stabilizzano la struttura, ma mediano anche il riconoscimento di partner di legame esterni e agiscono come centri catalitici. Inoltre, i cambiamenti della struttura macromolecolare tramite processi di ripiegamento dinamico sono collegati a un riarrangiamento di ioni positivi incorporati nel guscio d'acqua circostante.
Gli ioni positivi sono disposti in diverse geometrie attorno al DNA e all'RNA:nelle cosiddette geometrie site-bound o contact-pair, uno ione positivo si trova a diretto contatto con un atomo di ossigeno di un gruppo fosfato. In contrasto, la cosiddetta atmosfera ionica esterna è costituita da ioni positivi separati da almeno uno strato di molecole d'acqua dai gruppi fosfato. Il ruolo funzionale delle diverse geometrie e le interazioni sottostanti sono lungi dall'essere compreso. Una visione più profonda a livello molecolare richiede sonde altamente sensibili che consentano di discernere le diverse geometrie ioniche senza disturbarle, e per mappare la loro dinamica sulla scala temporale ultraveloce dei moti molecolari.

Fig. 2:In alto:Struttura molecolare di una coppia di ioni di contatto costituita da dimetilfosfato (DMP) e uno ione magnesio Mg2 incorporato in acqua. Le frecce indicano gli allungamenti dei legami fosforo-ossigeno nella vibrazione asimmetrica di stiramento della PO2. In basso:spettri infrarossi bidimensionali (2D-IR) della vibrazione asimmetrica di stiramento PO2 misurata in un tempo di attesa T=500 fs dopo l'eccitazione vibrazionale. La risposta vibrazionale è mostrata in funzione dell'eccitazione infrarossa e delle frequenze di rilevamento ed è costituita da un componente P1 da molecole DMP senza uno ione magnesio nelle vicinanze e dal contributo P2 da coppie di ioni di contatto. Quest'ultimo è spostato a frequenze più alte a causa dell'interazione tra PO2- e Mg2. Credito:MBI Berlino
In una recente pubblicazione, i ricercatori del Max Born Institute (MBI) dimostrano che le vibrazioni dei gruppi fosfato rappresentano sonde sensibili e non invasive di geometrie ioniche in un ambiente acquatico. Dimetilfosfato (DMP, (CH 3 O)2PO 2- ), un sistema modello consolidato per la spina dorsale del DNA e dell'RNA, è stato preparato in acqua liquida con un eccesso di Mg 2+ ioni (Figura 2, top) e studiato mediante spettroscopia vibrazionale non lineare nel dominio del tempo dei femtosecondi (1 fs =10 -15 S). Gli esperimenti utilizzano la spettroscopia infrarossa bidimensionale (2-D-IR), un metodo più sofisticato per analizzare le interazioni e le strutture ioniche sulla scala temporale intrinseca dei moti molecolari fluttuanti.
La mappa degli esperimenti Mg 2+ ioni a diretto contatto con un PO 2- gruppo tramite una caratteristica distinta nello spettro 2-D-IR (Figura 2, parte inferiore). L'interazione con il Mg 2+ lo ione sposta il PO . asimmetrico 2- allungando la vibrazione ad una frequenza che è più alta che in assenza di Mg 2+ ioni. La forma della linea e l'evoluzione temporale di questa nuova funzionalità rivelano fluttuazioni della geometria della coppia ionica di contatto e del guscio d'acqua incorporato su una scala temporale di centinaia di femtosecondi mentre la coppia di contatto stessa esiste per tempi molto più lunghi (~10 -6 S). Un'analisi teorica approfondita mostra che il sottile equilibrio delle forze elettrostatiche attrattive (Coulomb) e delle forze repulsive dovute all'interazione di scambio quanto-meccanico governa la posizione di frequenza della vibrazione del fosfato.
La capacità della spettroscopia 2-D-IR di caratterizzare l'interazione fosfato-ione a corto raggio in soluzione fornisce un nuovo strumento analitico che integra le tecniche strutturali attualmente disponibili. Un'estensione di questo nuovo approccio al DNA e all'RNA e al loro ambiente ionico è molto promettente e dovrebbe fornire nuove informazioni sulle forze che stabilizzano le strutture di equilibrio e guidano i processi di ripiegamento.