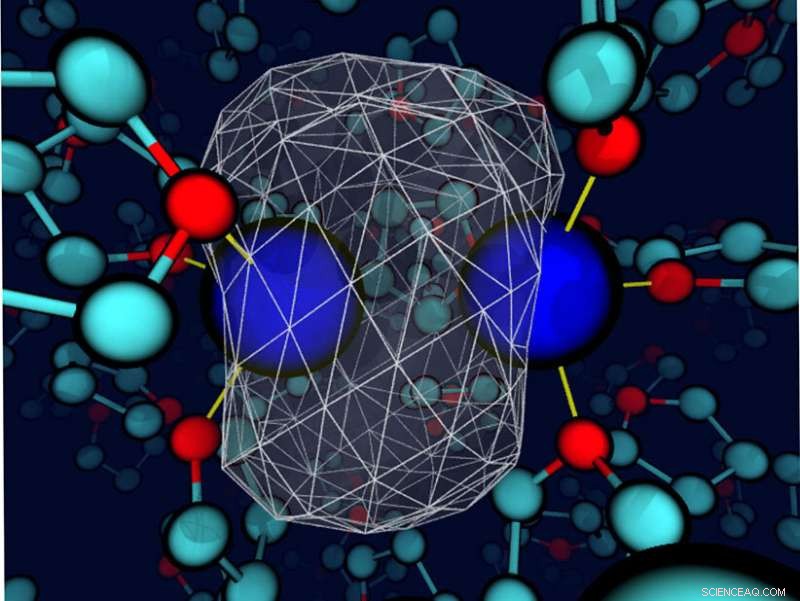
Una "istantanea" rivela che il solvente tetraidrofurano circostante deforma la densità di elettroni di legame attorno a un soluto di sodio. I nuclei di sodio sono sfere blu; la densità degli elettroni di valenza è rappresentata come una superficie bianca trasparente con una rete metallica bianca che racchiude la maggior parte della densità di carica. I legami tra il sodio e i vicini siti di ossigeno del solvente sono sottili linee gialle. Credito:Devon Widmer, Università della California, Los Angeles
Metti qualche mandorla intera in un barattolo pieno di nocciole. Scuotere. Le noci rimbalzano l'una contro l'altra, ma non reagiscono. È così che alcune persone pensano alle reazioni che avvengono all'interno dei liquidi. I soluti (mandorle) reagiscono tra loro in un mare di solventi (nocciole). Ma un nuovo studio mostra che questo non è sempre il caso delle vere reazioni chimiche. Nelle giuste condizioni, il solvente può cambiare l'identità chimica del soluto.
Molte reazioni chimiche, in particolare quelli rilevanti per mantenere in vita persone e piante, accadere in soluzione. Questa ricerca mostra che in molte di queste reazioni, il solvente non è un semplice spettatore. Ciò significa riorganizzare le aspettative e i modelli computazionali. Poiché le stesse regole potrebbero essere applicate nei laboratori di chimica, i ricercatori potrebbero dover selezionare i propri solventi con maggiore cura. I solventi potrebbero controllare o modificare l'identità chimica del soluto.
Sebbene in alcuni casi i solventi siano accuratamente selezionati, i liquidi sono spesso considerati semplicemente un mezzo per consentire ai reagenti di incontrarsi. Però, il solvente può svolgere un ruolo più importante. Qui, i ricercatori hanno scoperto che quando il solvente e il soluto interagiscono (energicamente nello stesso ordine di un legame idrogeno), il solvente può controllare la dinamica del legame e l'identità chimica di semplici soluti. I ricercatori sono giunti a questa conclusione studiando un dimero di sodio nel solvente debolmente polare tetraidrofurano. Le interazioni di legame tra il solvente e gli atomi di sodio hanno portato a stati di coordinazione unici. Questi stati hanno dovuto attraversare una barriera di energia libera, essenzialmente subendo una reazione chimica, interconvertire. Ulteriore, ogni stato di coordinamento aveva le proprie dinamiche e firme spettroscopiche. Sebbene i chimici siano da tempo consapevoli dell'influenza dei solventi in alcuni casi, questa ricerca evidenzia il valore di un'attenta selezione del solvente per creare un ambiente specifico in determinati sistemi chimici in fase condensata.