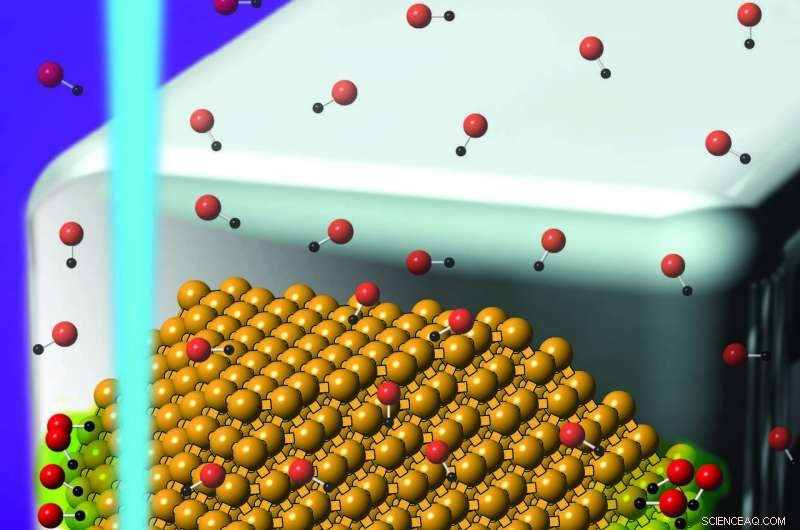
L'illustrazione mostra la posizione di una reazione chimica sulle nanoparticelle d'oro mediata da plasmoni superficiali localizzati:oscillazioni di gruppi di elettroni sulla superficie della nanoparticella. I plasmoni (verdi) fungono da catalizzatori che permettono la reazione, in cui coppie di monossido di carbonio (linee bianche) si trasformano in atomi di carbonio (rosso) e ossigeno (nero) a temperatura ambiente. Le palline d'oro rappresentano le nanoparticelle d'oro. Credito:K. Dill/NIST
I ricercatori del NIST hanno esplorato con dettagli senza precedenti una nuova generazione di catalizzatori che consentono alcune reazioni chimiche, che normalmente richiedono calore elevato, procedere a temperatura ambiente. I catalizzatori a risparmio energetico utilizzano la luce solare o un'altra fonte di luce per eccitare i plasmoni di superficie localizzati (LSP):oscillazioni di gruppi di elettroni sulla superficie di alcune nanoparticelle metalliche, come l'oro, argento e alluminio. L'energia derivata dalle oscillazioni LSP guida le reazioni chimiche tra le molecole che aderiscono alle nanoparticelle.
Gli scienziati avevano precedentemente dimostrato che l'idrogeno molecolare può essere suddiviso nei suoi singoli atomi dall'energia generata dalle oscillazioni dell'LSP. Il team del NIST ha ora scoperto una seconda reazione mediata da LSP che procede a temperatura ambiente. In questa reazione, Gli LSP eccitati nelle nanoparticelle d'oro trasformano due molecole di monossido di carbonio in carbonio e anidride carbonica. La reazione, che normalmente richiede una temperatura minima di 400 gradi C., svolge un ruolo importante nella conversione del monossido di carbonio in materiali a base di carbonio ampiamente utilizzati come i nanotubi di carbonio e la grafite.
Sondando le nanoparticelle con un fascio di elettroni e combinando i dati con simulazioni, i ricercatori del NIST hanno individuato i siti sulle nanoparticelle d'oro in cui si sono verificate le reazioni. Hanno anche misurato l'intensità degli LSP e mappato il modo in cui l'energia associata alle oscillazioni variava da un luogo all'altro all'interno delle nanoparticelle. Le misurazioni sono passaggi chiave nella comprensione del ruolo degli LSP per l'avvio di reazioni a temperatura ambiente, mitigando la necessità di riscaldare i campioni.
Wei-Chang Yang del NIST e del NanoCenter dell'Università del Maryland, insieme a Henri Lezec e Renu Sharma e altri collaboratori, descrivere il loro lavoro nel 15 aprile Materiali della natura .
Gli scienziati hanno fatto affidamento su depositi di depositi di carbonio solido, uno dei prodotti della reazione del monossido di carbonio che hanno studiato, come marcatori per le posizioni esatte sulle nanoparticelle d'oro in cui ha avuto luogo la reazione. Il team ha scoperto che la reazione si è concentrata nell'intersezione dove le molecole di monossido di carbonio aderiscono preferenzialmente alle nanoparticelle d'oro e dove l'ampiezza del campo elettrico associato agli LSP era più alta. Sebbene molti LSP possano essere eccitati dalla luce solare, il team ha scelto un fascio di elettroni per innescare le oscillazioni e ha studiato la reazione del monossido di carbonio in un microscopio elettronico a scansione a trasmissione che può funzionare in un ambiente a temperatura ambiente.
Le scoperte, dice Sharma, gettare le basi per la ricerca di altri sistemi che sfruttino direttamente la luce solare per generare LSP in nanoparticelle per guidare reazioni chimiche a temperatura ambiente. Riducendo il consumo di energia, tali sistemi potrebbero avere un enorme impatto sull'industria e sull'ambiente.