
Piega il tuo nanocubo! Sebbene i nanocubi utilizzati nel progetto di ricerca si costruiscano da soli, puoi piegare il tuo usando questo modello. Ogni X gialla rappresenta i luoghi in cui i ricercatori dell'Università di Tokyo hanno utilizzato atomi diversi con diversi livelli di polarizzabilità. Credito:Shuichi Hiraoka, CC-BY-ND
Il processo di costruzione di un minuscolo cubo ha rivelato alcuni dei misteri fondamentali di come le molecole si legano insieme negli ambienti naturali. I ricercatori sperano di applicare questa conoscenza a progetti futuri che progettano strutture complesse che possono imitare la vita.
Quando due molecole circondate da acqua si muovono l'una verso l'altra, parte della loro attrazione iniziale è talvolta dovuta alla forza chimica di respingere l'acqua:l'effetto idrofobico.
Una volta che le molecole sono vicine l'una all'altra, ma non ancora formalmente vincolato, diventa importante una forza molto più debole:la forza di dispersione.
"Il nostro sogno è controllare la forza di dispersione e fornire un semplice principio di progettazione per utilizzare la forza di dispersione per costruire complesse strutture autoassemblanti, " ha detto il professor Shuichi Hiraoka, capo del laboratorio in cui è stata eseguita la ricerca presso il Dipartimento di Scienze di base dell'Università di Tokyo.
Le forze di dispersione sono un tipo di forze di van der Waals, alcune delle interazioni chimiche più deboli conosciute in natura. Sebbene debole, le forze di van der Waals sono importanti; aiutano i gechi a salire sui muri e sono stati precedentemente identificati nel 2018 dallo stesso gruppo di ricerca come un blocco delle molecole a forma di ingranaggio o fiocco di neve dei nanocubi autoassemblanti.
Misurazione della forza di dispersione in condizioni naturali, come quando le molecole sono in soluzione con acqua, è stato impossibile. La forza è così debole che non può essere identificata separatamente dalle altre forze in gioco.
Però, in nuovi esperimenti, il team di ricerca ha usato i loro nanocubi autoassemblanti come strumenti per amplificare le differenze nella forza di dispersione.
Le molecole che compongono i lati dei cubi sono state modificate per contenere atomi selezionati per la loro polarizzabilità, intendendo la loro reattività al campo elettrico circostante. Ogni nanocubo completamente assemblato conteneva 18 di quegli atomi polarizzabili.
L'effetto combinato di 18 atomi è stato sufficiente per creare differenze misurabili nella forza di dispersione a seconda dell'atomo polarizzabile attaccato.
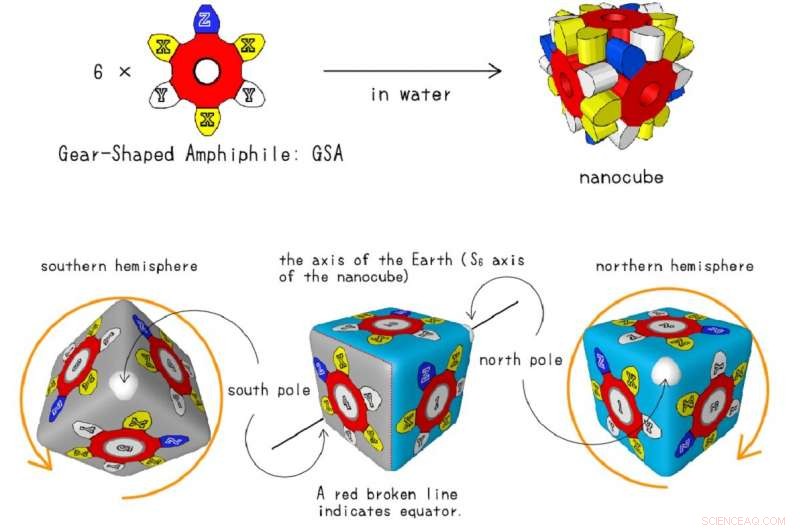
Il nanocubo completamente assemblato è rappresentato in questa illustrazione. Ogni X gialla è un luogo in cui i ricercatori dell'Università di Tokyo hanno utilizzato diversi atomi selezionati per la loro polarizzabilità. L'effetto combinato di 18 atomi a polarità variabile in ciascun nanocubo ha permesso ai ricercatori di misurare le differenze nella forza di dispersione. Credito:Shuichi Hiraoka, CC-BY.
La forza di dispersione viene calcolata matematicamente dopo aver utilizzato una tecnica chiamata calorimetria isotermica di titolazione per misurare la quantità di calore rilasciato quando le molecole si legano insieme.
Atomi più polarizzabili hanno creato forze di dispersione più forti e hanno reso i nanocubi più stabili. A seconda del valore stimato dell'effetto idrofobico, la forza di dispersione contribuisce da 0,6 a 2,2 volte più forza attrattiva e stabilità al cubo rispetto all'effetto idrofobico.
I ricercatori hanno in programma di utilizzare questa conoscenza su atomi più polarizzabili che creano forze di dispersione più forti per progettare future strutture molecolari artificiali con forme più complesse e funzioni aumentate.
"Per esempio, potremmo progettare molecole con aree superficiali di legame più grandi e posizionare atomi polari lungo i bordi per migliorare la stabilità complessiva attraverso l'attrazione delle forze di dispersione, " disse Hiraoka.
Risolvere un mistero nella progettazione di farmaci
Hiraoka afferma che le misurazioni per i nanocubi costruiti con idrogeno normale rispetto al deuterio, l'isotopo "pesante" dell'idrogeno, dovrebbe essere rilevante per la teoria della progettazione dei farmaci. La ricerca di altri gruppi aveva portato a rapporti contrastanti tra i chimici sul fatto che lo scambio di idrogeno con il deuterio due volte più pesante e più grande avrebbe creato una forza di dispersione più forte.
Come regola generale, gli atomi più grandi sono più polarizzabili e i ricercatori hanno avuto nuovi dati che indicano che una maggiore polarizzabilità ha portato a forze di dispersione più forti. Però, in alcuni casi l'idrogeno più piccolo produce effettivamente una forza di dispersione più forte del deuterio pesante, ma altri rapporti hanno mostrato la differenza opposta o trascurabilmente piccola tra i due atomi.
"Nei nostri esperimenti, la differenza entropia-entalpia è completamente bilanciata. L'energia libera rilasciata dai nanocubi con idrogeno o deuterio è essenzialmente identica, quindi potrebbe non esserci alcuna differenza tra loro, " disse Hiraoka.
Una differenza essenziale tra la ricerca precedente e questi esperimenti è che il team di UTokyo ha utilizzato una condizione più realistica di essere in soluzione con l'acqua e ha amplificato l'effetto utilizzando il design del nanocubo.