Credito:Università RUDN
Un chimico della RUDN University ha scoperto quattro nuovi composti stabili che possono essere ottenuti nella reazione dello iodio con lo ioduro di metilammonio:l'uso di queste sostanze consentirà la produzione di pannelli solari in perovskite senza reagenti tossici e preverrà i sottoprodotti durante la produzione. L'articolo è pubblicato su The Journal of Physical Chemistry Letters .
Le perovskiti ibride a base di piombo sono utilizzate nelle moderne celle solari come strato che assorbe la luce. Ma sono instabili all'umidità, e le tecnologie esistenti richiedono l'uso di soluzioni e solventi tossici. Ciò complica la tecnologia e la rende potenzialmente pericolosa.
La soluzione al problema potrebbe essere metodi senza solventi, questo è, l'uso di fusi piuttosto che soluzioni, ad esempio, applicando un poliioduro fuso su una sottile pellicola di piombo metallico. Però, ci sono pochi studi affidabili sulla chimica dei poliioduri. I ricercatori hanno studiato le proprietà del metilammonio (CH 3 NH 3 ) e composti di iodio per trovare varianti di composti adatti all'uso nella produzione di celle solari a perovskite.
I composti del sistema metilammonio ioduro (MA) e iodio si sciolgono a temperatura ambiente e formano liquidi ionici, ovvero si sciolgono composti esclusivamente da ioni. Questi liquidi precursori possono essere applicati uniformemente su grandi superfici, portando la produzione industriale di celle solari modulari basate su perovskiti ibride per il mercato commerciale.
I liquidi a base di poliioduri fondono a temperatura ambiente solo in presenza di grandi cationi organici nella composizione. Il chimico della RUDN University Victor Khrustalev ha spiegato questa differenza con il fatto che il catione metilammonio ha un grande momento di dipolo ed è in grado di formare un gran numero di legami idrogeno. A piccole dimensioni di cationi, questo porta ad un aumento dell'entropia durante la fusione, che abbassa la temperatura di fusione.
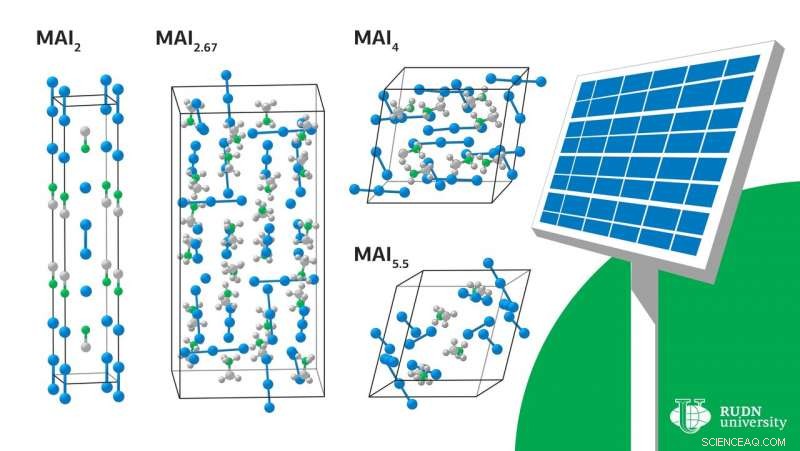
A determinate condizioni, cristalli di varia composizione iniziano ad evolversi dal liquido-MAI 2 , MAI 2.67 , MAI 4 è MAI 5,5 . Per determinare le condizioni in cui vi è una fusione, gli scienziati hanno effettuato un calcolo teorico dell'entalpia e dell'entropia della formazione di questi cristalli. Per tutti i composti tranne MAI 2 , la reazione per ottenere un composto con un contenuto di iodio inferiore dipendeva esclusivamente dal contributo di entropia. Gli emisti hanno spiegato che l'aumento dell'entalpia durante la transizione a composti con un contenuto di iodio più elevato è dovuto all'indebolimento dell'interazione dei cationi con gli anioni a causa della distribuzione di una piccola carica negativa su un grande anione poliioduro. Un simile aumento dell'entropia è dovuto alla complessità dei polianioni e all'indebolimento dei legami tra di loro.
Questi dati termodinamici ci hanno permesso di definire e generalizzare i valori sperimentali dei confini in cui può esistere il fuso.
I chimici hanno anche scoperto che tali effetti si verificano in composti simili con il catione formamidina (FA
+
=HC(NH 2 ) 2 ) e polibromuri. Inoltre, la composizione mista (MABr 3 ) 0.15 (FAI 3 ) 0,85 dimostra proprietà liquide ioniche da -40 a 80 °C. Un punto di fusione così basso del precursore è favorevole per ottenere film sottili di perovskiti ibride miste che dimostrano le massime proprietà di assorbimento della luce.