
Credito:CC0 Dominio Pubblico
Gli scienziati del NUS hanno scoperto un nuovo meccanismo per la riduzione elettrochimica selettiva dell'anidride carbonica (CO 2 ) ad etanolo utilizzando catalizzatori compositi rame-argento (Cu-Ag).
Riduzione elettrochimica di CO 2 a combustibili e prodotti chimici, se alimentato da elettricità rinnovabile, è un passo avanti nella riduzione delle emissioni di carbonio. I materiali in rame (Cu) sono catalizzatori scelti per questo processo perché hanno le più alte attività elettrochimiche nei confronti dei prodotti multicarbonio. Però, la loro selettività verso l'etanolo (C 2 h 5 OH), un prezioso combustibile e materia prima chimica, è sempre inferiore rispetto all'etilene (C 2 h 4 ). La preferenza verso la produzione di etilene rispetto all'etanolo deriva dal meccanismo di dimerizzazione della CO per la produzione di C 2 molecole di CO 2 , dove la formazione di etilene, che ha una barriera energetica inferiore, è favorito rispetto all'etanolo.
Un gruppo di ricerca guidato dal Prof Yeo Boon Siang, Jason del Dipartimento di Chimica della NUS, in collaborazione con un team guidato dal Dr. Federico Calle-Vallejo dell'Università di Barcellona, ha dimostrato che un afflusso di molecole di CO, fornito da co-catalizzatori di argento (Ag), attiva un percorso meccanicistico altrimenti bloccato sul Cu che converte la CO 2 gas in etanolo.
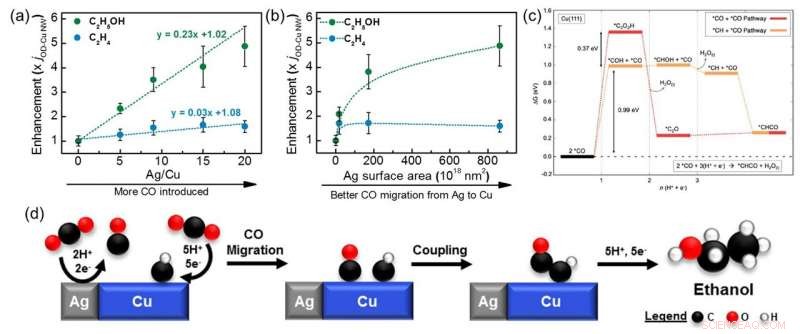
Grafici che mostrano come il miglioramento della produzione di etanolo (verde) ed etilene (blu) su compositi rame-argento (Cu-Ag) varia con diversi (a) rapporti Ag/Cu e (b) dimensioni delle particelle Ag. È stato osservato un miglioramento di cinque volte per l'etanolo, mentre l'etilene non è stato significativamente influenzato. (c) Diagramma del livello di energia che mostra le fasi di accoppiamento CO+CO (rosso) e CO+CH (arancione) su Cu (111). Per l'accoppiamento CO+CH è necessaria una barriera inferiore, rendendolo più favorevole rispetto allo step CO+CO. (d) Schema che mostra il meccanismo per la riduzione della CO2 ad etanolo su compositi Cu-Ag tramite l'accoppiamento CO+CH. Credito:Catalisi ACS
Una serie di catalizzatori compositi Cu-Ag, fabbricato da una miscela di nanofili di Cu derivati da ossido e polveri di Ag, sono stati testati per la loro CO . elettrochimica 2 attività di riduzione. Durante CO 2 riduzione, Ag converte CO 2 a CO e queste molecole di CO migrano verso i siti attivi di Cu per un'ulteriore riduzione in idrocarburi (etilene) e alcoli (etanolo). I ricercatori hanno variato il rapporto Ag/Cu e le dimensioni delle particelle Ag nei compositi per aumentare l'afflusso di CO dall'Ag ai siti attivi sul materiale Cu. I risultati sperimentali hanno mostrato che l'aumento dell'afflusso di CO ha migliorato la produzione di etanolo fino a cinque volte, con scarso impatto sulla produzione di etilene. Simulazioni teoriche sul meccanismo di reazione mostrano che invece della fase CO+CO che porta alla formazione di etilene, il CO+CH X era il passaggio dominante di formazione del legame C-C all'interfaccia Cu-Ag. L'etanolo era l'unico prodotto quando la reazione procede attraverso il CO+CH X fare un passo, che si è verificato su siti attivi diversi da quelli che hanno facilitato la formazione di etilene tramite il passaggio CO+CO.
Ulteriori piani derivanti da questa scoperta da parte del team di ricerca includono la massimizzazione dei siti attivi attraverso la progettazione del catalizzatore e la produzione potenziata utilizzando una configurazione di celle a flusso ad alto rendimento.
Il professor Yeo ha detto, "Il concetto che un percorso precedentemente chiuso può essere aperto da un afflusso di intermedi, come dimostrato in questo lavoro, apre nuove possibilità per scoprire nuovi meccanismi sintetici che prima potevano essere inaccessibili".