
Funzionalizzazione dei legami eterei. (A) Farmaci a piccole molecole contenenti porzioni di etere ciclico. Ph, fenile; AC, acetile; Bz, benzoile; glu, glucosio. (B) Scissione di C-O catalizzata da metalli di transizione tramite addizione ossidativa. R, alchile; M, Metallo di transizione; FG, gruppo funzionale; B2pin2, bis(pinacolato)diboro. (C) Inserimento di carbene in eteri attivati. (D) Derivati ciclici del boronato come candidati farmaci o reticolanti per materiali biomedici. (E) Questo lavoro:un inserimento diretto di boro catalizzato da Ni tramite un percorso di scissione e poi di rimbalzo. Credito:Scienza, 10.1126/science.abg5526
Il legame carbonio-ossigeno (C-O) negli eteri alchilici può essere scisso utilizzando metodi blandi per semplificare le sintesi chimiche elaborando robusti, precursori facilmente reperibili. In un nuovo rapporto ora su Scienza , Hairong Lyu e un gruppo di ricerca in chimica presso l'Università di Chicago e l'Università di Pittsburgh, Gli Stati Uniti hanno descritto in dettaglio come i dibromoborani hanno reagito con gli eteri alchilici in presenza di un catalizzatore di nichel (Ni) e di un riducente di zinco per inserire il boro nel legame CO. La successiva reattività ha influenzato la sostituzione ossigeno-azoto per semplificare la preparazione dei composti bioattivi in modo più ampio. Utilizzando studi meccanicistici, il team ha rivelato un percorso di scissione e poi di rimbalzo tramite catalisi tandem zinco/nichel.
Frazioni di etere
Le porzioni di etere si trovano comunemente nelle materie prime e nella chimica fine; Per esempio, gli eteri ciclici sono prevalenti in una gamma di molecole biologicamente importanti tra cui farmaci, agrofarmaci e prodotti naturali. Gli eteri agiscono anche come legami strutturali efficaci per proteggere i gruppi in sintesi organica grazie alla loro elevata stabilità chimica nei confronti degli acidi, basi, riducenti e ossidanti. Un metodo blando che modifica direttamente una porzione sostituendo l'ossigeno o inserendo un atomo interposto nel legame CO può convenientemente introdurre un nuovo gruppo funzionale in un'impalcatura esistente in un passaggio strategicamente importante. I chimici possono utilizzare eteri robusti come surrogati per gruppi chimici più sensibili che possono essere installati in seguito. Lyu et al. sono stati ispirati dai recenti progressi nella chimica del borylene per funzionalizzare i legami eterei inserendo una specie attiva di borylene.
Scissione dei legami etere alchilico
Convenzionalmente, i legami alchiletere possono essere scissi in condizioni dure e fortemente acide. Per stabilire un metodo pratico in questo lavoro, Lyu et al. cercato di evitare forti riducenti, catalizzatori costosi e condizioni di reazione forzata. Lo studio è quindi iniziato con 2, 3-diidrobenzofurano come sottostato etereo modello e dibromomesitilborano (MesBBr 2 ) come reagente di boro. Il gruppo voluminoso ha impedito la dimerizzazione delle specie di boro ridotto per migliorare la stabilità del prodotto di inserimento del boro per l'isolamento. Il catalizzatore di nichel combinato e la polvere di zinco erano i più efficaci. Il team ha infine ottenuto il prodotto di inserimento del boro desiderato 2H-benzoxaborin (etichettato 3a) con una resa del 90% in soluzione di toluene a 60 gradi Celsius. Il percorso di reazione era nettamente diverso; hanno utilizzato un complesso tetraedrico Ni (II) stabile all'aria abbreviato (molecola di Cat 1) e hanno confermato la sua struttura utilizzando la cristallografia a raggi X per evidenziarne la superiorità rispetto ad altri precatalizzatori di Ni o altri metalli. In assenza di Cat1, hanno notato una resa inferiore all'1% di 2H-benzoxaborin e un intermedio alchil bromuro con apertura dell'anello (abbreviato come 4a) per formarsi con una resa elevata. Anche altri complessi di nichel hanno dato il prodotto desiderato, anche se con una resa molto inferiore. Lyu et al. ha notato un'efficienza simile utilizzando un catalizzatore di nichel generato in situ (abbreviato come L1). Dato il ruolo critico del catalizzatore di nichel, il team ha anche esaminato altri ligandi a base di azoto. I ligandi monodentati hanno agito meglio dei ligandi bidentati (etichettati da L1 a L7 e confrontati con L8 a L12). Per esempio, 3-metil piridina (L5) ha mostrato una reattività leggermente inferiore, mentre la maggior parte delle altre monopiridine (L2, L3, L4 e L6) così come l'ossazolina (abbreviato L7) erano relativamente meno efficaci. Hanno anche usato la polvere di zinco come catalizzatore essenziale e hanno notato la progressione della reazione di inserimento del boro a una bassa velocità di reazione a temperatura ambiente.
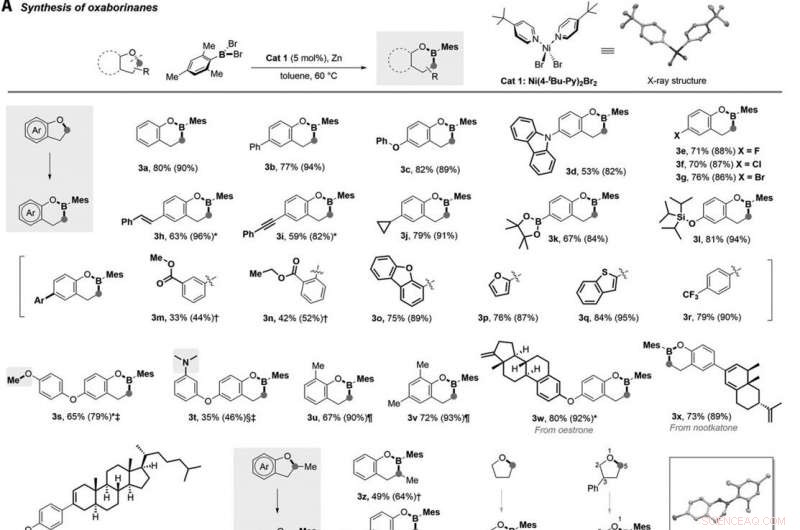
Borilazione catalizzata da nichel di eteri ciclici. (A) Sintesi di ossaborinani tramite borilazione diretta di eteri ciclici a cinque membri. Me, metile; Ar, arile. (B) Sintesi di oxaborepan tramite borilazione diretta di eteri ciclici a sei membri. Ts, tosile. (C) Sintesi di ossaborolani e azaborolidina tramite borilazione diretta di cicloossabutani e azetidina. (D) Sintesi dell'ossazaborolidina tramite borilazione diretta della 4-fenil-morfolina. (E) Sintesi di acidi borinici tramite borilazione diretta di eteri lineari. Le reazioni sono state condotte con 0,2 mmol di etere, 0,24 mmol MesBBr2, 0,01 mmol Cat 1, e 1 mmol di polvere di zinco in 0,5 ml di toluene a 60°C sotto azoto per 24 ore. Vengono fornite rese isolate dopo cromatografia su gel di silice; i numeri tra parentesi sono i rendimenti della risonanza magnetica nucleare prima della purificazione. *La reazione è stata condotta a 80°C. La reazione è stata condotta a 100°C. È stato utilizzato ‡0,2 mmol MesBBr2. §La reazione è stata condotta a 130°C. Ni (PMe3)2Cl2 (0,01 mmol) è stato utilizzato come catalizzatore, e la reazione è stata condotta a 130°C per 18 ore. Il tempo di reazione è stato di 36 ore. Credito:Scienza, 10.1126/science.abg5526 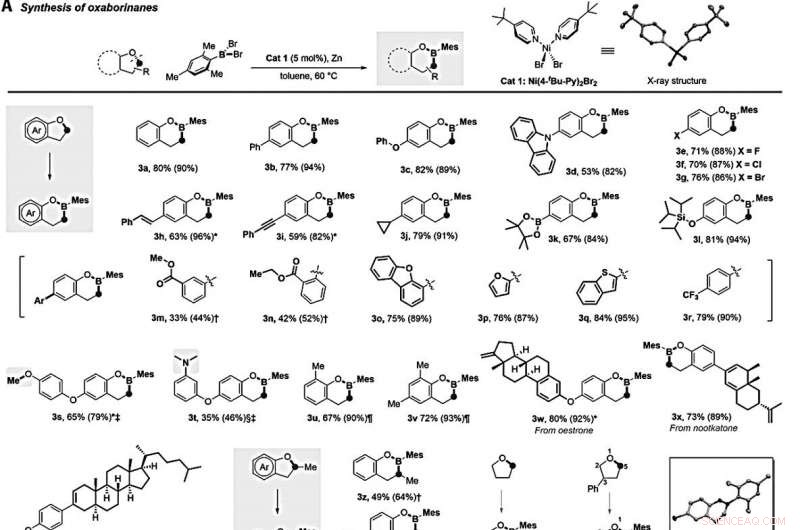
Lyu et al. esaminato lo scopo dell'etere per la reazione di inserimento del boro. Ad esempio, una gamma di 2 sostituiti, 3-diidrobenzofurani hanno reagito con MesBBr 2 (dibromomesitylborane) in modo uniforme per formare i prodotti di inserimento del boro desiderati con rese da buone a eccellenti. Per esempio, substrati contenenti alogeni compreso il fluoro (F), il cloro (Cl) e il bromo (Br) sono stati sottoposti ad accoppiamenti incrociati catalizzati da nichel per formare 2H-benzoxaborine (etichettate da 3e a 3g) con una resa superiore al 70%. Tra una miriade di molecole così formate, il team ha notato la tolleranza di entrambe le parti di pinacol boronato e silil etere durante questa reazione. Ulteriori esperimenti di controllo mostreranno come il cloruro alchilico primario sia pienamente compatibile, mentre il bromuro alchilico primario era parzialmente compatibile nelle condizioni di reazione. Inoltre, il fluoruro alchilico primario non è stato tollerato a causa delle sue forti interazioni boro-fluoruro. Lyu et al. quindi derivati complessi substrati da prodotti naturali terpenici che hanno subito la reazione di inserimento del boro e hanno consegnato i prodotti desiderati in 3 volte o più. Inoltre, il tetraidrofurano ha anche fornito il previsto prodotto di inserimento del mono boro (etichettato come 3ab) con una resa del 69%. Quando il team ha utilizzato il 3-fenil-tetraidrofurano asimmetrico come partner di accoppiamento, l'inserimento del boro è avvenuto regioselettivamente nella posizione meno ingombrante per indicare l'influenza degli sterici.
Inserimento del boro in molecole più complesse.
Lyu et al. inoltre condotto l'inserimento di boro in ossetani più tesi, anche, per fornire una voce agli oxaborolani a cinque membri (etichettati da 3ai a 3aj). La selettività compromessa ha portato a prodotti collaterali lineari. Dal punto di vista della praticità sintetica, il team ha mostrato come il legame B-Mes (boro-mesityl) potrebbe facilmente subire un'idrolisi in un vaso tramite l'aggiunta di acqua in metanolo per fornire i corrispondenti prodotti di idrossile boronato che sono più stabili nell'aria. Gli scienziati hanno funzionalizzato boronato ciclico da 2 prontamente disponibili, 3-diidrobenzofurani in un unico passaggio per sviluppare analoghi di un farmaco antifungino approvato noto come tavaborolo e crisaborolo, un farmaco approvato per il trattamento della dermatite.
Elaborazione sintetica. (A) Rapido accesso ai boronati ciclici tramite idrolisi one-pot. I prodotti di boronato (da 5a a 5c) sono sostanzialmente più stabili nei confronti dell'aria e dell'umidità. (B) Ulteriore funzionalizzazione del prodotto di borilazione tramite derivatizzazione del legame C-B. Bn, benzile. (C) Modifica O-to-N per accedere a pirrolidine e piperidine da tetraidrofurani e tetraidropirani, rispettivamente. (D) Tre approcci per l'espansione dell'anello a un carbonio di eteri ciclici. DIAD, diisopropil azodicarbossilato. (E) Sintesi semplificata del farmaco antipertensivo nebivololo. Per i protocolli di reazione dettagliati. Credito:Scienza, 10.1126/science.abg5526
Altre reazioni
La frazione di boro nei prodotti di inserimento potrebbe anche essere convenientemente convertita in vari altri gruppi funzionali. Ad esempio, il team potrebbe trattare il prodotto grezzo (3a) 2H-benzoxaborin, con acqua ossigenata per ottenere 1, 2-tirosolo (6a) in ottima resa. L'accoppiamento Suzuki-Miyaura della molecola 3a con bromo-benzene ha formato in modo efficiente o-fenilfenolo (etichettato come 7a). Il metodo ha anche consentito reazioni di espansione dell'anello a un carbonio efficienti e ha fornito un'espansione dell'anello a ritenzione di boro. Durante gli esperimenti, la natura del gruppo alchilico nella reazione di accoppiamento e il ruolo del catalizzatore di nichel sono stati fondamentali per comprendere le fasi successive della formazione del legame carbonio-boro.
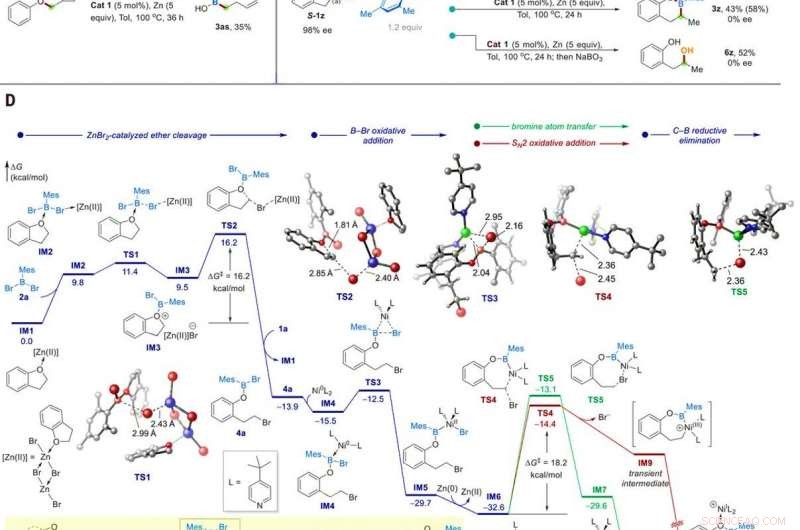
Studi meccanicistici. (A) Identificazione dell'intermedio di reazione. (B) Esperimento dell'orologio radicale. (C) Esperimenti di controllo con un substrato ee al 98%. (D) Profilo energetico calcolato della borilazione catalitica dell'etere 1a. I calcoli sono stati eseguiti su M06/SDD-6311+G(d, p)/SMD(toluene)//B3LYP-D3/SDD-6-31G(d) livello di teoria. Il riquadro mostra la catalisi tandem Zn/Ni proposta. Credito:Scienza, 10.1126/science.abg5526
Veduta
In questo modo, Hairong Lyu e colleghi hanno dimostrato un metodo per l'inserimento del boro in legami alchileteri sotto la catalisi di nichel e zinco. Poiché gli eteri sono sottostati prontamente disponibili e robusti, il metodo di inserimento del boro può anche semplificare la sintesi di complesse molecole bersaglio riducendo al minimo le manipolazioni del gruppo funzionale o proteggendo gli usi del gruppo. La distinta modalità di reazione rivelata dagli studi meccanicistici può avere implicazioni sulle reazioni di catalisi tandem acido/metallo di transizione di Lewis che vanno oltre questo lavoro.
© 2021 Science X Network