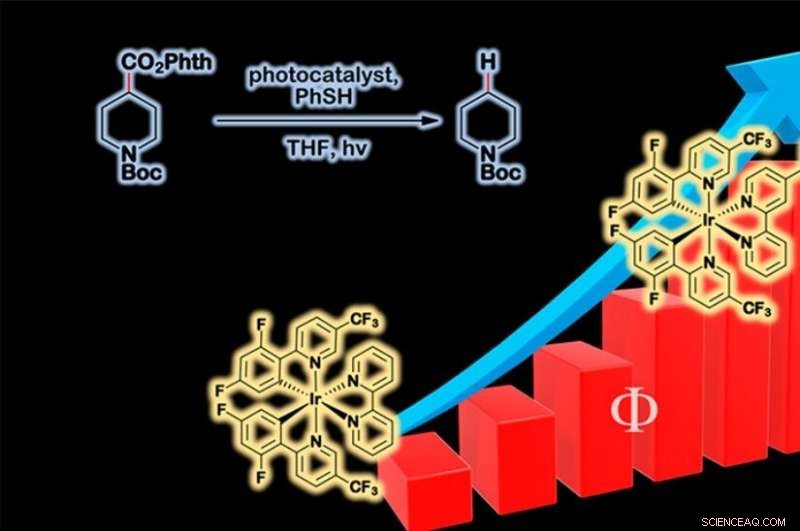
La resa quantica della reazione, è così che i ricercatori misurano l'efficienza di una reazione attivata dalla luce. Credito:Anna Zieleniewska.
Traendo ispirazione dalla fotosintesi e dal modo in cui può raggiungere un'elevata efficienza nelle piante, I professori reggenti Tom Moore e Ana Moore della School of Molecular Sciences dell'Arizona State University e i loro gruppi, insieme ai colleghi del Dipartimento di Chimica dell'Università di Princeton (tra cui i professori Gregory Scholes e Robert Knowles), hanno introdotto un catalizzatore bioispirato che allunga lo stato produttivo di alcune reazioni chimiche.
"Lavorare con i gruppi di Princeton di Knowles e Scholes ci ha dato nuove prospettive e applicazioni per il nostro bioispirato, sistemi fotosintetici artificiali, " ha detto Ana Moore. I professori reggenti Ana e Thomas Moore della School of Molecular Sciences dell'ASU. Credito immagine:Mary Zhu Scarica l'immagine completa
"In questo caso, abbiamo riprogettato un fotocatalizzatore importante nell'industria chimica utilizzando il principio del trasferimento di elettroni accoppiato a protoni (PCET) per fornire una migliore efficienza catalitica.
"Il PCET è ampiamente utilizzato nei catalizzatori naturali in cui sono essenziali percorsi di reazione a bassa energia che producono un singolo prodotto. È gratificante trovare un'applicazione pratica per i costrutti PCET che abbiamo sviluppato di recente. Migliorare l'efficienza catalitica delle reazioni che danno luogo a composti con specifiche l'attività farmacologica potrebbe contribuire a uno sviluppo più sostenibile di un'industria chimica più verde".
Il team ha impiegato PCET per manipolare il fotocatalizzatore al fine di rallentare la ricombinazione di carica, essenzialmente imitando il processo che mantiene la fotosintesi ronzante.
Il loro meccanismo blocca una fase elementare del processo di un fattore 24 rispetto a un composto di riferimento. PCET è una classe di reazioni che comportano il trasferimento di un elettrone e di un protone.
Al centro di questa ricerca collaborativa c'è un modello chimico, una sottostruttura PCET, sviluppato dai ricercatori qui all'ASU. Il modello è collegato a un complesso di iridio che riduce efficacemente la forza trainante della ricombinazione di carica, prolungando così lo stato attivo in cui può avvenire la chimica.
Il modello si basa sul complesso in evoluzione dell'ossigeno nella fotosintesi che si trova in ogni pianta, l'enzima che produce ossigeno per il mondo intero. Ci sono due amminoacidi vicino al complesso che evolve l'ossigeno - tirosina e istidina legate all'idrogeno - e questi due amminoacidi trasportano gli elettroni lontano dal complesso che evolve l'ossigeno, da un meccanismo PCET, in modo che l'enzima sia in grado di produrre ossigeno.
I Moore e i colleghi hanno realizzato questo modello, benzimidazolo-fenolo (BIP), che è chimicamente molto simile a quei due amminoacidi nella fotosintesi. Questo viene quindi utilizzato per controllare la direzione del trasferimento di elettroni nella catalisi.
La carta, "Ligand basato su PCET limita la ricombinazione di carica con un catalizzatore fotoredox Ir(III), " è stato appena pubblicato nel Giornale della Società Chimica Americana .
La ricerca combina contributi ai meccanismi di fotocatalisi dal laboratorio Knowles, spettroscopia risolta in tempo ultrarapido dal laboratorio Scholes, e il modello BIP dei laboratori di Thomas Moore e Ana Moore.
Centro di ricerca di frontiera energetica
La ricerca soddisfa una delle massime priorità per il gruppo Bioinspired Light-Escalated Chemistry (BioLEC) di Princeton, un Energy Frontier Research Center istituito nel 2018 e finanziato dal Dipartimento dell'Energia. BioLEC è diretto da Scholes, William S. Todd Professore di Chimica di Princeton e presidente del dipartimento.
"Questo è assolutamente dovuto al centro. Rob, Tom e Ana sono stati i promotori intellettuali di questa idea, " disse Scholes. "Ecco, abbiamo aggiunto un ulteriore "circuito" al fotocatalizzatore molecolare che ha soppresso la via di disattivazione. Il nostro circuito serve come una sorta di buffer, mantenendo le specie ad alta energia in posizione fino a quando il catalizzatore non può avviare la reazione chimica. Penso che sia una grande storia di successo".
"Lavorare con Rob e Greg e gli studenti e i postdoc del centro si è dimostrato ancora più eccitante e gratificante di quanto sperassimo quando l'idea è stata formulata per la prima volta per la proposta BioLEC, "dissero i Moore.
In natura, la fotosintesi si verifica quando una pianta assorbe la luce che genera una separazione di carica nel suo "centro di reazione". Questa reazione guida sia l'ossidazione dell'acqua che la fissazione dell'anidride carbonica nei combustibili utilizzati dall'impianto. La ricombinazione di carica essenzialmente cortocircuita il processo fotosintetico. Così, la natura ha evoluto modi per sostenere tale separazione utilizzando i cosiddetti relè redox.
I ricercatori hanno utilizzato questi relè molto redox nella loro indagine come componenti essenziali di una serie di segnali a breve distanza, veloci passaggi di trasferimento redox equivalenti che competono efficacemente con la ricombinazione di carica.
I processi evolutivi hanno selezionato questi relè redox dove attraverso il trasferimento di un elettrone e un protone tra due amminoacidi legati all'idrogeno, può fare trasferimenti davvero veloci che separano ulteriormente le spese.
Spostando rapidamente le cariche l'una dall'altra, impedisci quella ricombinazione di carica. Ciò porta all'efficienza della fotosintesi. I ricercatori hanno utilizzato questa idea.
La struttura del modello BIP sviluppato dai Moore è simile a quei due amminoacidi.
"Abbastanza sicuro, gli studi nel laboratorio di Scholes del catalizzatore riprogettato con il BIP hanno mostrato una durata maggiore per l'intermedio radicale reattivo e - ecco la prova nel budino - la resa della reazione è stata più che raddoppiata, " Tom Moore ha detto. "La natura utilizza PCET nella catalisi, e Madre Natura ne sa una o due sull'efficienza, chimica sostenibile".