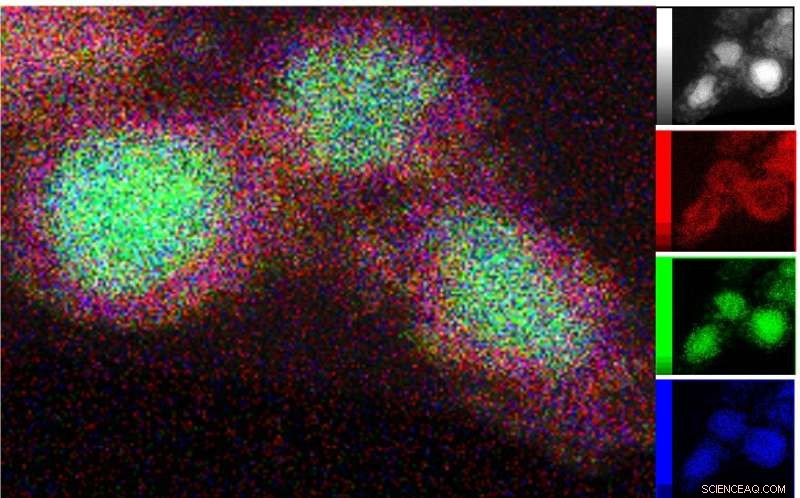
La microscopia elettronica a trasmissione (TEM) della fase cataliticamente attiva è stata combinata con la spettroscopia di raggi X a dispersione di energia per mappare la distribuzione di Ni (verde), Si (blu) e ossigeno (rosso) attorno alle strutture del guscio centrale. Credito:P. Menezes /HZB/TU Berlin
L'elettrolisi potrebbe essere un concetto familiare dalle lezioni di chimica a scuola:due elettrodi sono immersi nell'acqua e messi sotto tensione. Questa tensione fa sì che le molecole d'acqua si scompongano nei loro componenti e le bolle di gas salgono agli elettrodi:si forma ossigeno gassoso all'anodo, mentre si formano bolle di idrogeno al catodo. L'elettrolisi potrebbe produrre idrogeno in una CO2 -modo neutro:purché l'elettricità richiesta sia generata da forme di energia esenti da fossili come il sole o il vento.
L'unico problema è che queste reazioni non sono molto efficienti ed estremamente lente. Per velocizzare le reazioni si utilizzano catalizzatori, a base di metalli preziosi e rari come platino, rutenio o iridio. Per un uso su larga scala, tuttavia, tali catalizzatori devono essere costituiti da elementi ampiamente disponibili e molto economici.
Nanostrutture indotte chimicamente
Per accelerare la reazione di evoluzione dell'ossigeno all'anodo, i materiali a base di nichel sono considerati buoni candidati. Il nichel è resistente alla corrosione, poco tossico e anche poco costoso. Finora, tuttavia, i processi ad alta temperatura ad alta intensità energetica sono stati utilizzati principalmente per produrre materiali catalizzatori a base di nichel.
Un team guidato dal Dr. Prashanth Menezes (HZB/TU Berlin) ha ora trovato un modo "soft chemical" per produrre un catalizzatore efficiente a base di nanocristalli intermetallici di nichel-silicio.
"Abbiamo combinato l'elemento nichel con il silicio, il secondo elemento più abbondante nella crosta terrestre, e abbiamo ottenuto la nanostrutturazione tramite una reazione chimica. Il materiale risultante ha eccellenti proprietà catalitiche", afferma Menezes. Il cristallino Ni2 Si funge da precatalizzatore per la reazione di evoluzione dell'ossigeno alcalino all'anodo e subisce una trasformazione superficiale per formare nicke(ossi)idrossido come catalizzatore attivo in condizioni operative. Sorprendentemente, l'elettrolisi dell'acqua è stata ulteriormente accoppiata con una reazione di ossidazione organica a valore aggiunto in cui l'elettrosintesi di composti nitrilici di valore industriale è stata prodotta da ammine primarie con conversione selettiva e completa in condizioni miti. Tali metodi elettrosintetici possono aumentare la generazione di idrogeno al catodo e possono fornire contemporaneamente l'accesso a preziosi prodotti industriali all'anodo.
Più efficiente e stabile
Rispetto ai moderni catalizzatori a base di Nichel, Cobalto, Ferro, Rutenio e Iridio, il Ni2 nanoporoso Si è significativamente più attivo e rimane stabile per tempi di reazione più lunghi in condizioni di livello industriale. Per comprendere il comportamento di Ni2 Più in dettaglio, il team ha combinato diversi metodi di misurazione, tra cui analisi elementari, microscopia elettronica e moderne misurazioni spettroscopiche al BESSY II. "In futuro, anche gli elettrolizzatori industriali per acqua alcalina potrebbero essere dotati di un rivestimento di questo siliciuro di nichel nanoporoso", afferma Menezes.
La ricerca è stata pubblicata su Advanced Energy Materials . + Esplora ulteriormente