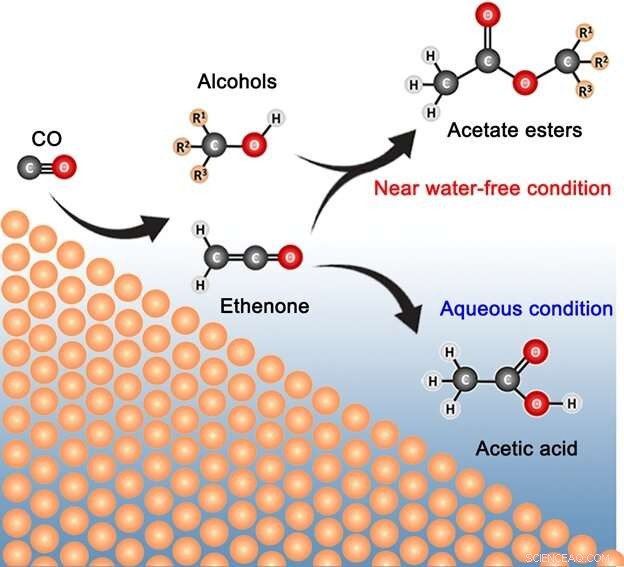
Visual mostra i processi coinvolti nella produzione di C3 – C6 esteri acetato dalla riduzione elettrocatalitica del monossido di carbonio in una cella di assemblaggio di elettrodi a membrana. Credito:Angewandte Chemie International Edition
I chimici della National University of Singapore hanno scoperto come gli esteri dell'acetato potrebbero essere elettro-sintetizzati dall'acqua e dal monossido di carbonio in modo ambientalmente sostenibile.
La riduzione elettrocatalitica dell'anidride carbonica o del monossido di carbonio utilizzando elettricità rinnovabile è un metodo di produzione verde promettente per la produzione di sostanze chimiche. Finora, utilizzando questo metodo è stata prodotta un'ampia gamma di prodotti carboniosi tra cui alcoli, idrocarburi e acidi carbossilici. È interessante notare che gli esteri, un'importante famiglia di composti organici, non si sono formati allo stesso modo. Ci sono molti usi per gli esteri, alcuni dei quali includono solventi e lubrificanti. Sono classicamente prodotti attraverso reazioni stechiometriche come l'esterificazione di Fischer. I reagenti di partenza sono in genere derivati da risorse fossili e dopo la reazione vengono generati rifiuti chimici, il che rende il processo poco rispettoso dell'ambiente.
Un gruppo di ricerca guidato dal Professore Associato Yeo Boon Siang (Jason) del Dipartimento di Chimica, NUS in collaborazione con il Dr. Sumit Verma e il Dr. Ramesha Ganganahalli della compagnia energetica internazionale Shell ha scoperto come C3 —C6 gli esteri acetato possono essere elettro-sintetizzati dal monossido di carbonio e dall'acqua utilizzando catalizzatori di rame in un gruppo di elettrodi a membrana. L'acetato di etile e l'acetato di propile possono essere prodotti con un'efficienza faradaica totale (FE) di circa il 22% e con una densità di corrente fino a 55 mA/cm 2 , insieme a quantità minori di acetato di metile e acetato di butile. Gli esteri sono stati prodotti tramite la reazione di addizione di etenone (H2 C=C=O) e alcoli prodotti durante la riduzione di CO. La condizione di reazione quasi priva di acqua e l'alto livello di pH locale svolgono un ruolo chiave nella formazione degli esteri.
NUS e Shell avevano concordato all'inizio dell'anno scorso di sviluppare congiuntamente processi per creare combustibili e prodotti chimici verdi per l'industria energetica.
Il professor Yeo ha affermato:"Questo lavoro è il risultato della collaborazione tra NUS e Shell per creare sostanze chimiche in modo sostenibile. Il nostro team è riuscito a sviluppare un processo elettrochimico per produrre esteri utilizzando materie prime rinnovabili come monossido di carbonio e acqua".
Basandosi sui risultati della ricerca del loro lavoro, il team di ricerca prevede di sviluppare catalizzatori con una maggiore efficienza di conversione degli esteri. + Esplora ulteriormente