I ricercatori dell'Università di Pittsburgh e della Drexel University di Filadelfia, insieme al Brookhaven National Laboratory, stanno lavorando per risolvere un mistero in più parti per rendere i trattamenti di disinfezione dell'acqua più sostenibili.
Le tecnologie scalabili di produzione elettrochimica di ozono (EOP) per disinfettare l’acqua sporca potrebbero un giorno sostituire i trattamenti centralizzati al cloro utilizzati oggi, sia nelle città moderne che nei villaggi remoti. Tuttavia, si sa poco sull'EOP a livello molecolare e su come le tecnologie che lo rendono possibile possano essere rese efficienti, economiche e sostenibili.
La loro ricerca, "Interplay between Catalyst Corrosion and Homogeneous Reactive Oxygen Species in Electrochemical Ozone Production", è stata pubblicata di recente sulla rivista ACS Catalysis .
L'autore principale è Drexel Ph.D. studente Rayan Alaufey, con il contributo di ricercatori di Drexel, tra cui il co-PI Maureen Tang, professore associato di ingegneria chimica e biologica, il ricercatore post-dottorato Andrew Lindsay, Ph.D. la studentessa Tana Siboonruang e Ezra Wood, professore associato di chimica; il co-PI John A. Keith, professore associato di ingegneria chimica e petrolifera e lo studente laureato Lingyan Zhao di Pitt; e Qin Wu di Brookhaven.
"Le persone hanno utilizzato il cloro per trattare l'acqua potabile sin dal 19° secolo, ma oggi comprendiamo meglio che il cloro potrebbe non essere sempre l'opzione migliore. L'EOP, ad esempio, può generare ozono, una molecola con circa lo stesso potere disinfettante del cloro, direttamente nell'acqua .
"A differenza del cloro che persiste stabilmente nell'acqua, l'ozono nell'acqua si decompone naturalmente dopo circa 20 minuti, il che significa che è meno probabile che danneggi le persone quando si consuma dall'acqua del rubinetto, quando si nuota in una piscina o quando si puliscono le ferite in un ospedale," ha spiegato Keith, che è anche R.K. Mellon Faculty Fellow in Energia presso la Swanson School of Engineering di Pitt.
"L'EOP per la disinfezione sostenibile avrebbe molto senso in alcuni mercati, ma per farlo richiede un catalizzatore sufficientemente buono e, poiché nessuno ha ancora trovato un catalizzatore EOP sufficientemente buono, l'EOP è troppo costoso e ad alto consumo energetico per un uso più ampio.
"Io e i miei colleghi abbiamo pensato che se fossimo riusciti a decodificare a livello atomico ciò che fa funzionare un catalizzatore EOP mediocre, forse avremmo potuto progettare un catalizzatore EOP ancora migliore."
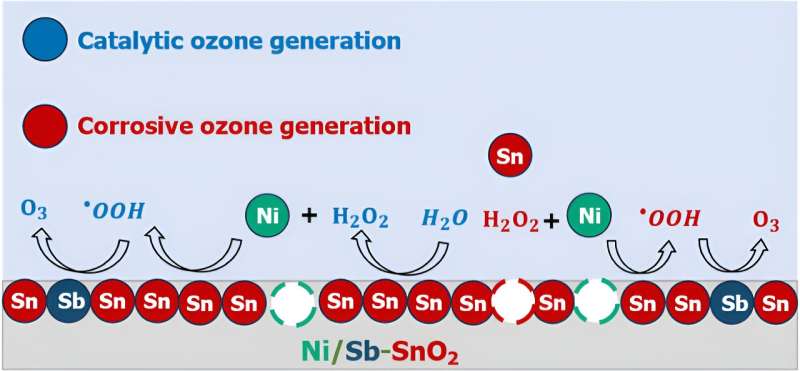
Risolvere il mistero del funzionamento dei catalizzatori EOP è cruciale per comprendere come progettare meglio uno dei catalizzatori EOP più promettenti e meno tossici conosciuti fino ad oggi:l'ossido di stagno drogato con nichel e antimonio (Ni/Sb–SnO2 , o NATO).
Qui, ha detto Keith, sta l'enigma:qual è il ruolo di ogni atomo nella NATO per aiutare l'EOP? L'ozono si sta formando cataliticamente nel modo in cui vogliamo, oppure si forma perché il catalizzatore si sta decomponendo e occorre lavorare in futuro per rendere i catalizzatori della NATO più stabili?
Sorprendentemente, i ricercatori hanno scoperto che probabilmente si tratta di un mix di entrambi.
Utilizzando analisi elettrochimiche sperimentali, spettrometria di massa e modelli computazionali di chimica quantistica, i ricercatori hanno creato una "trama su scala atomica" per spiegare come viene generato l'ozono sugli elettrocatalizzatori NATO.
Per la prima volta, hanno identificato che parte del nichel presente nella NATO probabilmente fuoriesce dagli elettrodi attraverso la corrosione e questi atomi di nichel, che ora galleggiano nella soluzione vicino al catalizzatore, possono promuovere reazioni chimiche che alla fine generano ozono.
"Se vogliamo realizzare un elettrocatalizzatore migliore, dobbiamo capire quali parti funzionano e quali non funzionano. Fattori come la lisciviazione di ioni metallici, la corrosione e le reazioni in fase di soluzione possono dare l'impressione che un catalizzatore funzioni in un modo quando in realtà funziona in un altro modo."
Keith ha osservato che identificare la prevalenza della corrosione e delle reazioni chimiche che si verificano lontano dal catalizzatore è un passo importante da chiarire prima che altri ricercatori possano perseguire miglioramenti all'EOP e ad altri processi elettrocatalitici.
Nella loro conclusione, notano:"Identificare o confutare l'esistenza di tali vincoli tecnologici fondamentali sarà fondamentale per qualsiasi futura applicazione dell'EOP e di altri processi di ossidazione elettrochimica avanzati."
"Sappiamo che il trattamento elettrochimico dell'acqua funziona su piccola scala, ma la scoperta di catalizzatori migliori lo porterà su scala globale. Il prossimo passo sarà trovare nuove combinazioni atomiche in materiali che siano più resistenti alla corrosione ma che promuovano anche un EOP economicamente e sostenibile ," ha detto Keith.
Ulteriori informazioni: Rayan Alaufey et al, Interazione tra la corrosione del catalizzatore e le specie omogenee di ossigeno reattivo nella produzione di ozono elettrochimico, catalisi ACS (2024). DOI:10.1021/acscatal.4c01317
Informazioni sul giornale: Catalisi ACS
Fornito dall'Università di Pittsburgh