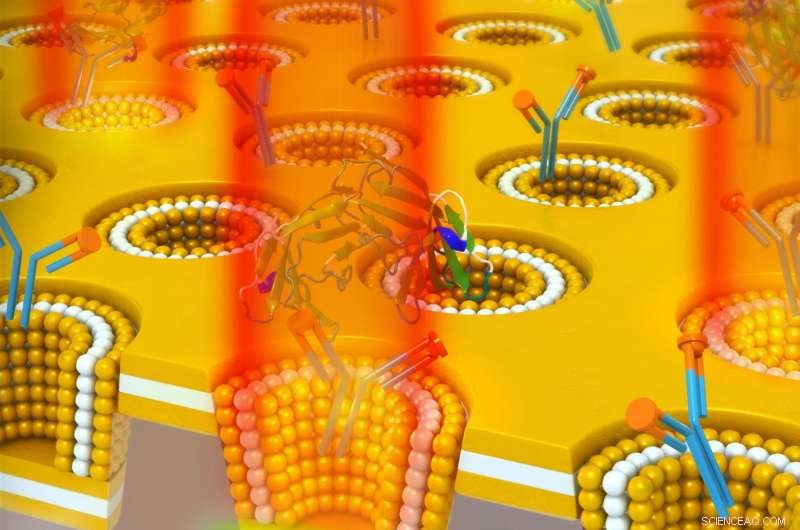
Un design di cavità plasmoniche nanocup metallo-isolante-metallo utilizzato per rilevare il biomarcatore del cancro CEA. La nanocavità porta all'accumulo di energia ottica che è accoppiata al campo lontano da un aumento dell'indice di rifrazione. Perciò, Il legame del CEA al suo anticorpo immobilizzato porta ad un sensibile aumento dell'intensità di trasmissione alla lunghezza d'onda di risonanza senza spostamento spettrale. Credito:Università dell'Illinois
Un nuovo sensore plasmonico sviluppato dai ricercatori dell'Università dell'Illinois a Urbana-Champaign servirà come affidabile rilevamento precoce di biomarcatori per molte forme di cancro e, infine, altre malattie.
Il sensore si è dimostrato affidabile per rilevare la presenza dell'antigene carcinoembrionario (CEA) biomarcatore del cancro fino alla grandezza di 1 nanogrammo per millilitro. La maggior parte degli esseri umani trasporta almeno alcune quantità di CEA con un intervallo medio di 3-5 nanogrammi per millilitro. I ricercatori hanno scelto di concentrarsi sul CEA perché la sua presenza in concentrazioni più elevate è un indicatore precoce di molte forme di cancro, compresi i tumori del polmone e della prostata.
"Il cancro è una delle principali cause di morte negli Stati Uniti poiché più della metà dei nuovi pazienti viene diagnosticata dopo che si è già diffusa, " Ha spiegato Ameen. "Questo mostra la gravità con cui questo problema deve essere affrontato e questo nuovo design di un sensore plasmonico aiuta a rilevare la minore concentrazione di CEA in uno stato precedente".
Il sensore plasmonico è un miglioramento dell'attuale metodo all'avanguardia per alcuni motivi. Primo, è stato in grado di migliorare il limite di rilevamento di almeno due ordini di grandezza. Infatti, la maggior parte dei metodi non è in grado di rilevare con precisione la presenza di CEA fino a quando non raggiunge una concentrazione più elevata.
In secondo luogo, perché funziona con molta meno strumentazione, è meno costoso e più portatile e non richiede quasi l'esperienza per fare una lettura. Significa anche che invece di aver bisogno di una fiala di sangue per un test, andrà bene una semplice puntura del dito. Questo aspetto sarà particolarmente importante per coloro che non vivono vicino a una struttura medica avanzata, compresi quelli nei paesi in via di sviluppo.
Il gruppo di ricerca è stato guidato da Logan Liu, e Lynford Goddard, professori associati di ingegneria elettrica e informatica con gli studenti Abid Ameen e Lisa Hackett che realizzano il progetto. Il team ha pubblicato i suoi risultati in Materiali ottici avanzati come articolo di copertina.
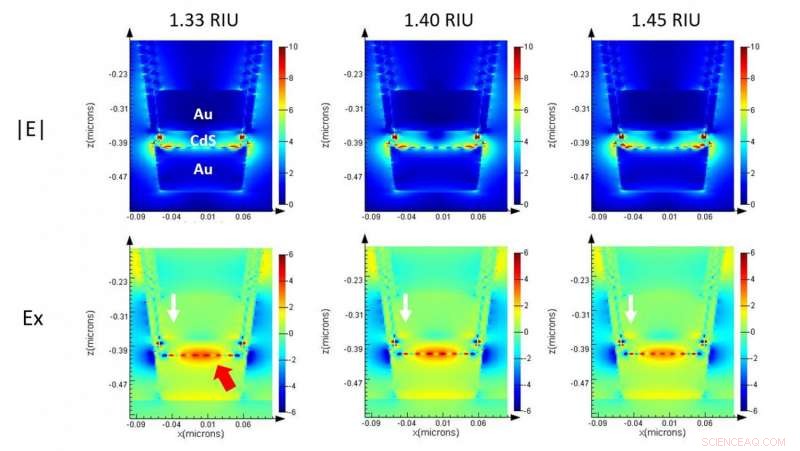
Simulazione elettromagnetica di un singolo nanocup su ML-nanoLCA che mostra l'intensità del campo nella sezione trasversale. Credito:Università dell'Illinois
Il dispositivo combina due metodi di rilevamento, che fino a quel momento non era stato possibile utilizzare insieme. Primo, utilizza una nanocavità multistrato 3D in un array di nanocup, che consente di immagazzinare la luce nella cavità composta da due strati metallici (in questo caso oro) che circondano uno strato isolante.
In secondo luogo, utilizza il rilevamento plasmonico, che rileva le interazioni luce-materia sensibili su scala nanometrica con le biomolecole sulla superficie del dispositivo. Produce un confinamento di campo potenziato e un campo localizzato potenziato. A causa della struttura plasmonica, la luce viene disaccoppiata in modo più efficiente al variare dell'indice di rifrazione circostante.
"Combinando le proprietà plasmoniche e le proprietà della cavità ottica insieme in un unico dispositivo, siamo in grado di rilevare una minore concentrazione di biomarcatore mediante il confinamento e la trasmissione della luce rispettivamente nello strato della cavità e dalla parte superiore del dispositivo, in base allo spessore dei multistrati e all'indice di rifrazione dello strato di cavità, "Amen ha spiegato.
"L'array nanocup fornisce una trasmissione ottica straordinaria, " aggiunse Hackett. "Se prendi una sottile pellicola di metallo e provi a far brillare la luce attraverso di essa, non ci sarà quasi nessuna luce trasmessa. Tuttavia, se metti una serie periodica di nanofori, o nel nostro caso una struttura a nanocup, allora quello che vedi è una condizione di risonanza dove ad una certa lunghezza d'onda, avrai un picco nella trasmissione attraverso questo dispositivo."
Poiché la risonanza cambia a una singola lunghezza d'onda e poiché le caratteristiche spettrali hanno posizioni di riferimento, l'eccitazione e il rilevamento possono essere eseguiti in modo affidabile senza alcuna attrezzatura specializzata. Con questo dispositivo, è possibile utilizzare una sorgente luminosa a LED al posto di un laser e una fotocellula o l'immagine di una telecamera al posto di uno spettrometro di fascia alta.
"Grazie alla nostra struttura plasmonica multistrato ad alte prestazioni, siamo stati in grado di diffondere in modo molto efficiente la luce nel campo lontano, " Hackett ha detto. "Quando si aumenta l'indice di rifrazione della regione di rilevamento, provoca l'accoppiamento dell'energia immagazzinata. Di solito quando si hanno questi tipi di sensori plasmonici rifrattometrici, hai uno spostamento nell'angolo o un cambiamento nella tua lunghezza d'onda quando la condizione di risonanza è soddisfatta. Nel nostro caso, perché abbiamo incorporato una nanocavità, abbiamo una lunghezza d'onda di risonanza fissa."
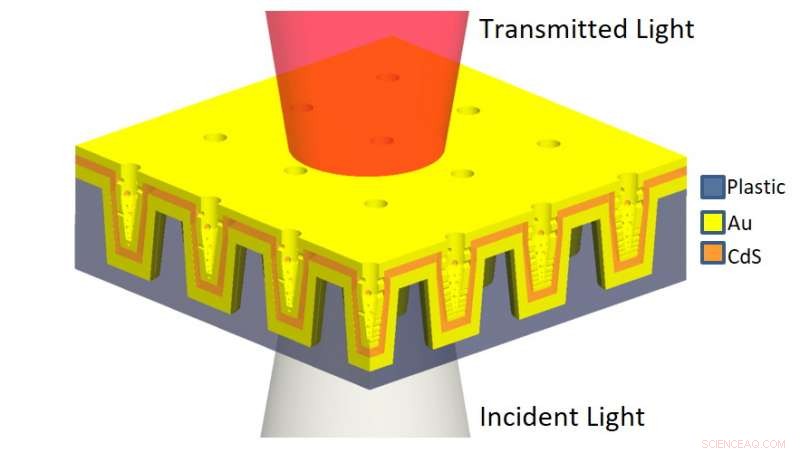
L'illustrazione schematica della nanoLCA multistrato (ML-nanoLCA) mostra la struttura multistrato e la direzione dell'illuminazione. Credito:Università dell'Illinois a Urbana-Champaign
All'aumentare della concentrazione di biomolecole (in questo caso CEA), così fa l'indice di rifrazione, che produce un aumento dell'intensità di trasmissione ad una lunghezza d'onda fissa che può essere facilmente rilevata.
"Ciò significa che in futuro possiamo prendere questo sensore, che abbiamo ottimizzato e incorporato con un LED e abbiamo la strumentazione più compatta, infatti nessuna strumentazione sofisticata, "Ha detto Ameen. "Ciò consente al rilevamento plasmonico ad alte prestazioni la capacità di andare verso sistemi di rilevamento portatili e sensori portatili su larga scala".
Per adesso, metodi di rilevamento per i biomarcatori del cancro vengono implementati in pazienti ad alto rischio, soprattutto malati di cancro in remissione. ci vuole tempo, attrezzature specializzate, e richiedono molta manodopera.
Nel futuro, però, a causa della portabilità e della natura economica di questo metodo, può essere somministrato più facilmente a qualsiasi paziente durante i controlli di routine. Ciò consentirebbe di trattare quelli con un'elevata concentrazione di CEA anche prima che le cellule tumorali si diffondano nel corpo.
"In questo momento il cancro viene rilevato più vicino allo stadio finale, " Ameen ha osservato. "Vogliamo rilevarlo il prima possibile. Il nostro dispositivo ci offre questa opportunità".
Sebbene questo studio abbia dimostrato il rilevamento in un piccolo campione di siero umano, il metodo potrebbe essere utilizzato per l'individuazione di altre malattie lungo la strada.
"Nel futuro, se sono molto convenienti e portatili, "Hackett ha detto, "sarebbe bello vedere le persone essere in grado di assumere un maggiore controllo sulla propria salute e monitorare qualcosa di simile da sole".